Clear Sky Science · he
בדיקות אימונוהדמיות דיגיטליות מבוססות תמונה הומוגנית עם סובלנות שגיאות גבוהה
מדוע חלקיקים זעירים ומצלמות חכמות חשובים
רבות מהבדיקות הרפואיות של היום דורשות מעבדה מלאה עם צוות מיומן או מציעות תשובות מהירות אך גסות על רצועה פשוטה. המאמר מציג דרך להשיג את הטוב משני העולמות: דיוק ברמת מעבדה מדגימת דם קטנה בעזרת חומרה פשוטה, כאשר רוב העיבוד הכבד נעשה באמצעות ניתוח תמונה חכם. על‑ידי מעקב אחרי התנהגות חלקיקי זהב זעירים בטיפת דם ומתן פרשנות לתמונות אלה על‑ידי תוכנת למידת מכונה, המחברים מפתחים מסלול למבחנים ביתיים וקליניים שקל להשתמש בהם וקשים לשיבוש.
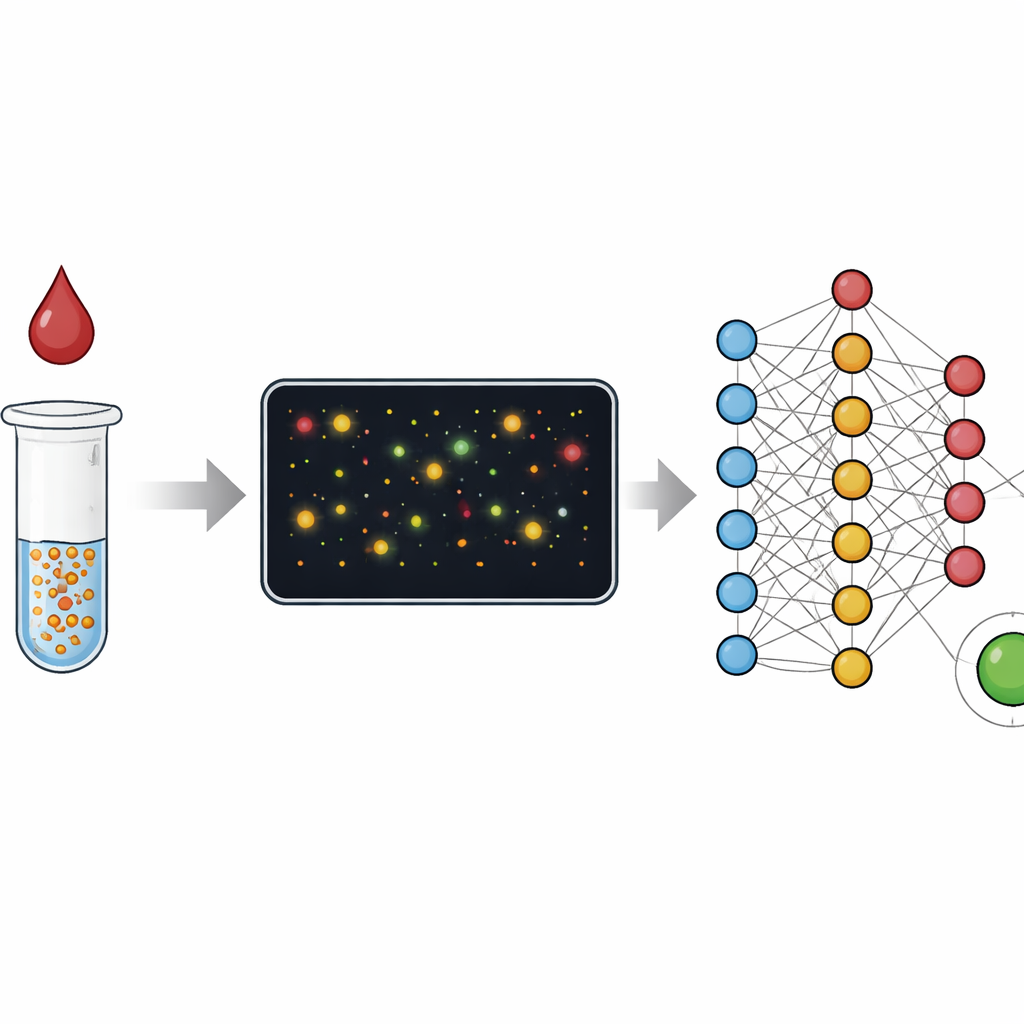
מצבעים לשיטות ספירה של חלקיקים
בדיקות דם מסורתיות כמו ELISA קוראות שינוי צבע ממוצע של מיליוני מולקולות בדרך שמזכירה שיפוט קהל לפי רמת הרעש הכוללת. בדיקות רצועה מהירות, או בדיקות זרימה צידיות, פועלות על עיקרון דומה ומחליפות דיוק במהירות ופשטות. במחקר זה החוקרים מתמקדים במקום זאת בחלקיקי זהב בודדים שמתאגדים כאשר הם מוצאים את המטרה בדגימה, כגון חלבון C‑תגובה הקשור לדלקת או נוגדנים נגד הווירוס הגורם ל‑COVID‑19. במקום למדוד רק את הצבע הגולמי של התמיסה, הם משתמשים במיקרוסקופיה בשדה כהה כדי להדגים שדות זעירים מלאים בחלקיקים ואשכולות, ואז מנתחים כל אחד מהם. המעבר מ"אנלוגי" של צבע ל"דיגיטלי" של ספירה מרחיב משמעותית את טווח הריכוזים שהבדיקה יכולה למדוד ומקל על זיהוי מקרים שבהם משהו התקלקל.
לראות דרך הבלגן בדגימות מהעולם האמיתי
דגימות דם אמיתיות הן עכורות: הן מכילות תאי דם אדומים, שברי רקמה, בועיות ומקורות מסיחים ויזואליים אחרים שיכולים לבלבל כללי עיבוד תמונה פשוטים. הצוות מראה תחילה שגם עם אלגוריתמים קונבנציונליים מכוילים ניתן להפיק קשר נקי וכמעט ליניארי בין גודל האשכול לרמות חלבון C‑תגובה, והם עושים זאת ישירות בדם מלא בלי להפריד את התאים. כדי להתמודד באופן שיטתי יותר עם ארטיפקטים, הם מאמנים מודל סגמנטציה המסווג כל פיקסל בתמונה כחלקיק ננו, תא, אבק או רקע. לאחר סינון כל מה שאינו חלקיקים אמיתיים, הם שוב משתמשים בגודל אשכול כקריאת פלט. בגישה ההיברידית הזו הם מסווגים נכון מעמד נוגדני COVID‑19 בסרומים מאוחסנים של מטופלים עם רגישות של 90% וספציפיות של 96%, אף על פי שהתמונות נאספו בתנאים שנועדו להיות חשופים לשגיאות.
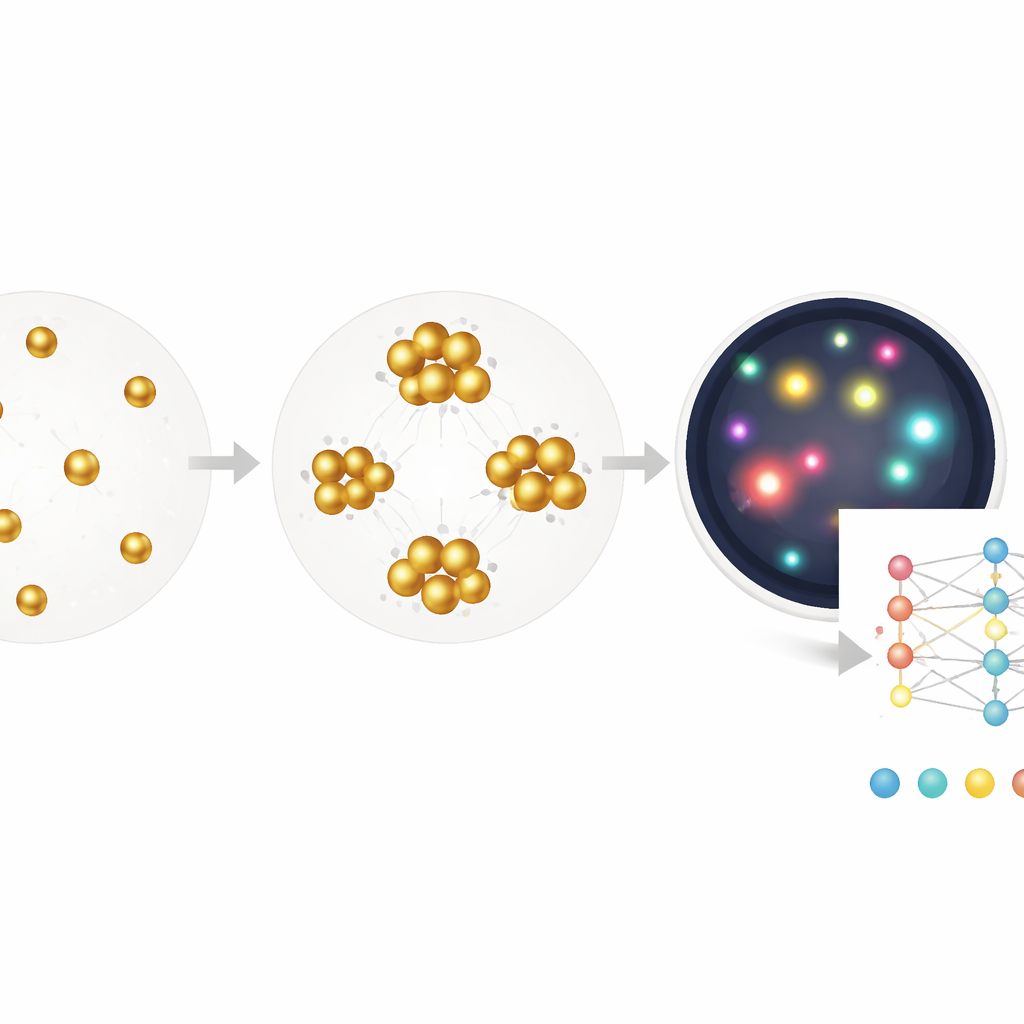
להניח למחשב לגלות מה חשוב
בעוד ששיטת הסגמנטציה מסייעת, היא עדיין נשענת על החלטות אנושיות לגבי אילו תכונות למדוד — למשל כמה גדול או בוהק אשכול צריך להיות. המחברים דוחפים קדימה על‑ידי אימון רשת עצבית עמוקה שממפה ישירות מתמונה גולמית לריכוז נוגדנים אנטי‑ויראליים, תוך שימוש רק בריכוז הידוע כתווית וללא סימוני פיקסל. המודל מקצה‑אל‑סוף הזה, המבוסס על ארכיטקטורת ResNet סטנדרטית, לומד בעצמו שילובים של רומזים: שינויי גוון עדינים, צפיפות, צורת אשכולות, רווחים ריקים ועוד. בבדיקה על דגימות חדשות הוא מעריך רמות נוגדנים על טווח של יותר משלוש וחצי סדרי גודל, עם סף גילוי המתקרב לזה של ערכת ELISA קלינית, תוך דרישה רק לשלב דגירה יחיד של 30 דקות ועבודה בנפחים זעירים.
לעצב בדיקות שניתן לכוונן כמו מיקרוסקופ
מעבר להצגת ניסוחים שעובדים, המחקר שואל גם עד כמה ניתן לדחוף עקרונית את גישת ספירת החלקיקים הדיגיטלית. באמצעות מסגרת מתמטית וסימולציות, המחברים מראים שרגישות בדיקות כאלה אינה קבועה; היא תלויה בכמה חלקיקים משמשים, עד כמה אחידים הם, וכמה טוב ניתן להבדיל בין חלקיקים יחידיים וזוגיים לפי הבהירות. על‑ידי כוונון כובעי הכניסה — ובמיוחד מספר החלקיקים ואיכותם — הם טוענים שבתיאוריה ניתן להגיע לריכוזים ניתנים לגילוי נמוכים מאוד, המוגבלים בעיקר על‑ידי סטטיסטיקת ספירה בסיסית. למידת מכונה מוסיפה דחיפה נוספת על‑ידי הגדלת כמות החלקיקים שניתן להשתמש בהם בביטחון ושיפור ההבחנה בין אירועי קשר אמיתיים לרעש אקראי.
למבחנים חכמים יותר וסלחניים יותר
בסך הכול, העבודה מציעה שזיווג של אופטיקה פשוטה עם ניתוח תמונה מתקדם יכול לספק מבחנים שמתחרים בשיטות מעבדה מובילות תוך מתן סובלנות לשינויי השימוש בעולם האמיתי. במקום לבנות חומרה מדויקת יותר ויותר, הגישה נשענת על המידע העשיר שכבר קיים בתמונות ומאפשרת לתוכנה למיין אות מהבלגן. עבור מטופלים ומערכות בריאות, הדבר יכול לומר יותר מבחני נקודת טיפול ובדיקות שניתן לבצע לבד לאיתור סמני דם ומחלות זיהומיות שכיחות, ללא צורך בכלים מורכבים או מפעילים מומחים.
ציטוט: McAffee, D.B., Hu, Q., Arnob, A. et al. Homogeneous image-based digital immunoassays with high error tolerance. npj Imaging 4, 30 (2026). https://doi.org/10.1038/s44303-026-00164-9
מילות מפתח: בדיקה אימונוהדמית דיגיטלית, הדמיית ננו־חלקיקים, אבחון בלימוד מכונה, בדיקות בנקודת הטיפול, נוגדנים ל‑SARS‑CoV‑2