Clear Sky Science · de
Homogene homogene, bildbasierte digitale Immunoassays mit hoher Fehlertoleranz
Warum winzige Partikel und smarte Kameras wichtig sind
Viele heutige medizinische Tests erfordern entweder ein komplettes Labor mit geschultem Personal oder liefern schnelle, aber grobe Antworten auf einem einfachen Teststreifen. Diese Arbeit stellt einen Weg vor, das Beste aus beiden Welten zu verbinden: Laborqualität aus einer kleinen Blutprobe mit einfacher Hardware, wobei der Großteil der Auswertung durch clevere Bildanalyse erfolgt. Indem die Autoren beobachten, wie winzige Goldpartikel in einem Blutstropfen reagieren, und maschinelles Lernen zur Interpretation dieser Bilder einsetzen, zeigen sie einen Pfad zu Heim‑ und Kliniktests, die sowohl leicht zu bedienen als auch schwer zu täuschen sind.
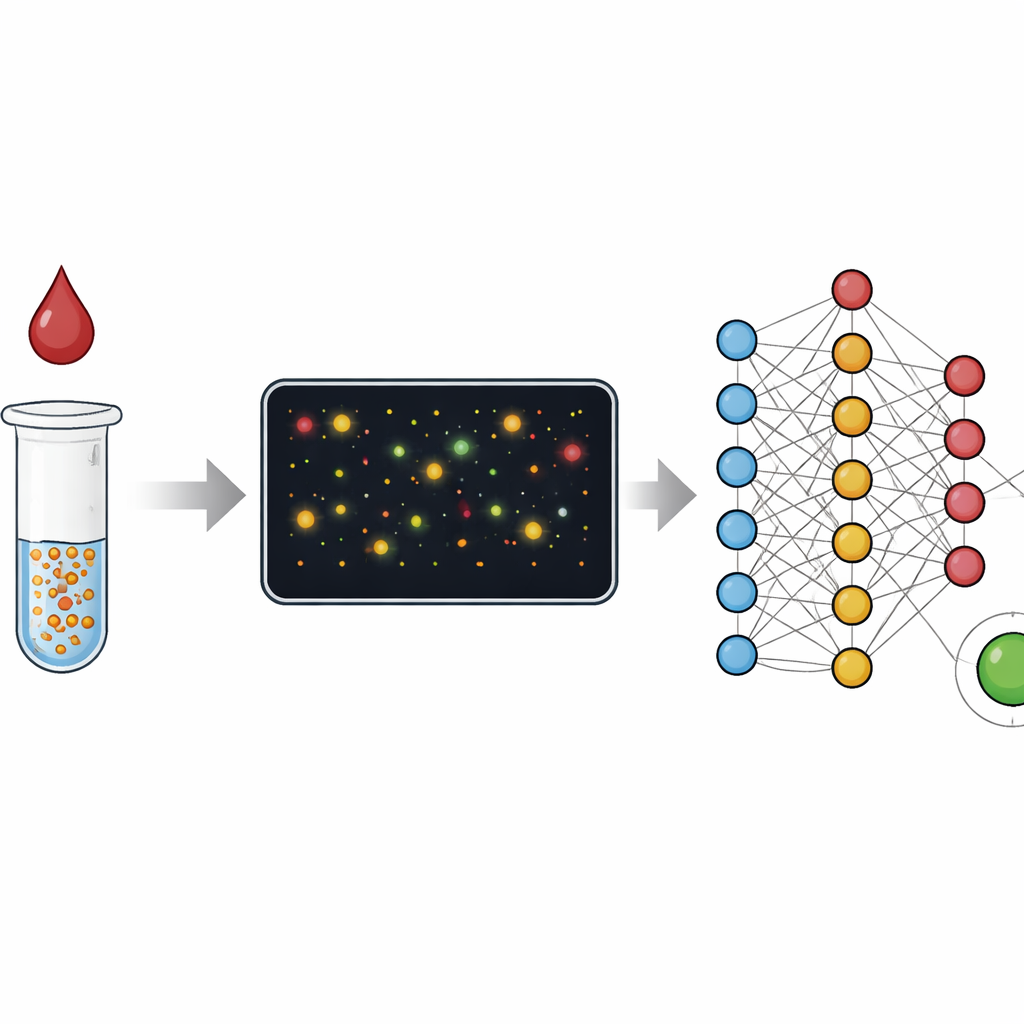
Von Farbänderungen zum Zählen von Partikeln
Traditionelle Bluttests wie ELISA messen eine mittlere Farbänderung von Millionen Molekülen in einer Vertiefung, ähnlich dem Beurteilen einer Menschenmenge anhand ihres Gesamtlärmpegels. Rasche Streifentests, sogenannte Lateral‑Flow‑Assays, beruhen auf einem ähnlichen Prinzip und tauschen Genauigkeit gegen Geschwindigkeit und Einfachheit. In dieser Studie konzentrieren sich die Forschenden stattdessen auf einzelne Goldnanopartikel, die sich verklumpen, wenn sie ihr Ziel im Probenmaterial finden, etwa C‑reaktives Protein, das mit Entzündungen verbunden ist, oder Antikörper gegen das Virus, das COVID‑19 verursacht. Anstatt nur die Gesamthelligkeit der Lösung zu messen, verwenden sie Dunkelfeldmikroskopie, um kleine Bildfelder voller Partikel und Cluster zu erfassen, und analysieren dann jedes einzelne. Dieser Wechsel von „analogem“ Farbmaß zu „digitalem“ Zählen erweitert die messbare Konzentrationsspanne erheblich und macht es einfacher, Fehlfunktionen zu erkennen.
Durch das Durcheinander in Proben aus der Praxis sehen
Echtes Blut ist unübersichtlich: Es enthält rote Blutkörperchen, Ablagerungen, Blasen und andere visuelle Störeinflüsse, die einfache Bildverarbeitungsregeln verwirren können. Das Team zeigt zunächst, dass sie selbst mit abgestimmten konventionellen Algorithmen eine saubere, nahezu lineare Beziehung zwischen Clustergröße und C‑reaktivem Protein erhalten können – und zwar direkt in Vollblut ohne Auftrennung der Zellen. Um Artefakte systematischer anzugehen, trainieren sie anschließend ein Segmentierungsmodell, das jedes Pixel im Bild als Nanopartikel, Zelle, Staub oder Hintergrund klassifiziert. Nach dem Herausfiltern aller nicht relevanten Klassen verwenden sie erneut die Clustergröße als Messgröße. Mit diesem hybriden Ansatz klassifizieren sie den COVID‑19‑Antikörperstatus in gelagerten Patientenseren mit 96 % Spezifität und 90 % Sensitivität korrekt, obwohl die Bilder unter absichtlich fehleranfälligen Bedingungen aufgenommen wurden.
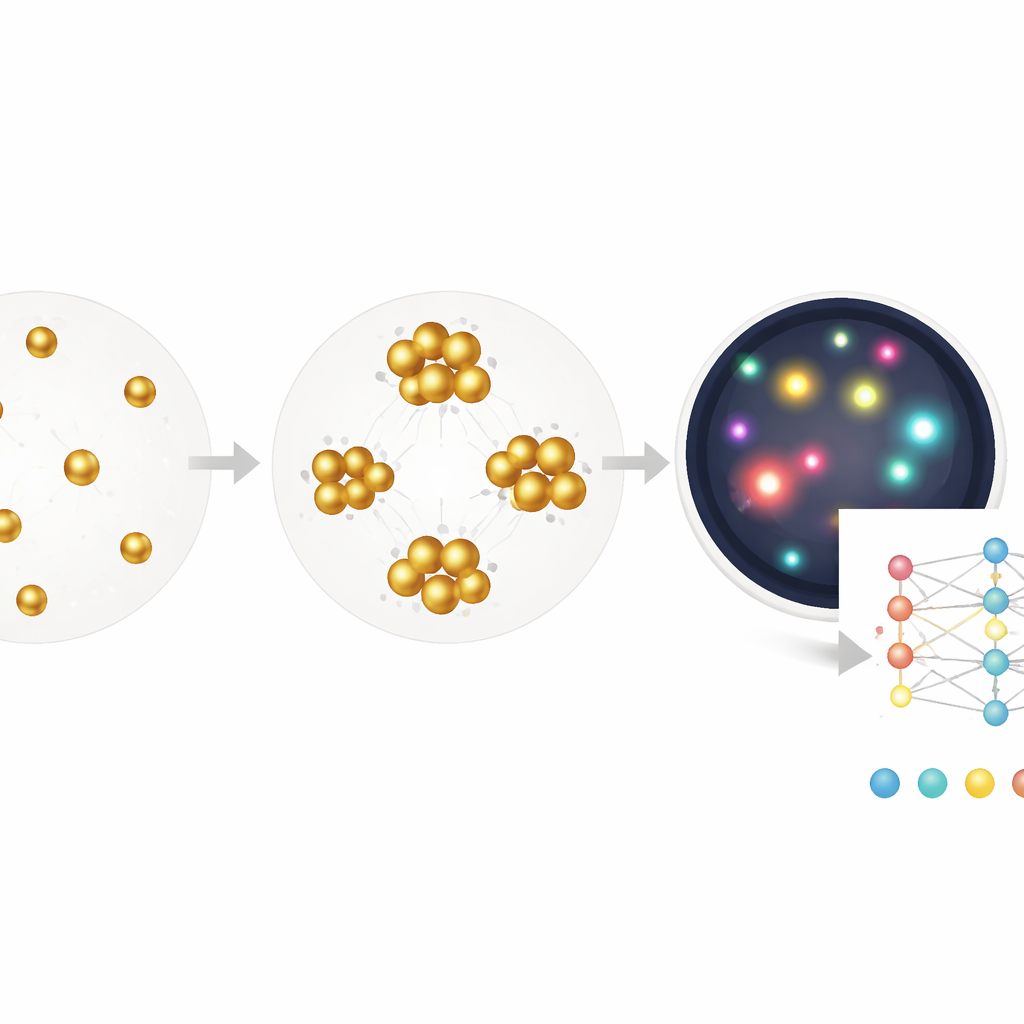
Den Computer entdecken lassen, was wichtig ist
Während die Segmentierungsmethode hilft, beruht sie noch auf menschlichen Entscheidungen darüber, welche Merkmale gemessen werden sollen – etwa wie groß oder hell ein Cluster sein muss. Die Autoren gehen weiter und trainieren ein tiefes neuronales Netzwerk, das direkt von einem Rohbild zur Konzentration antiviraler Antikörper gelangt, wobei als Label nur die bekannte Konzentration und keine Pixel‑level‑Annotationen verwendet werden. Dieses End‑to‑End‑Modell, aufgebaut auf einer Standard‑ResNet‑Architektur, lernt effektiv seine eigene Kombination von Hinweisen: subtile Farbverschiebungen, Dichte, Clusterform, leere Räume und mehr. Bei Tests an neuen Proben schätzt es Antikörperspiegel über einen Bereich von mehr als dreieinhalb Größenordnungen mit einer Nachweisgrenze, die an die eines klinischen ELISA‑Kits heranreicht, benötigt dabei jedoch nur eine einzelne 30‑minütige Inkubation und funktioniert mit sehr kleinen Volumina.
Tests entwerfen, die wie ein Mikroskop einstellbar sind
Über die Demonstration funktionierender Assays hinaus untersucht die Studie, wie weit dieses digitale Partikelzählen prinzipiell getrieben werden kann. Mittels eines mathematischen und simulativen Rahmens zeigen die Autoren, dass die Empfindlichkeit solcher Tests nicht festgelegt ist; sie hängt davon ab, wie viele Partikel verwendet werden, wie einheitlich sie sind und wie gut einzelne und gepaarte Partikel durch Helligkeit unterschieden werden können. Durch das Einstellen dieser Stellgrößen – insbesondere der Partikelanzahl und ihrer Qualität – argumentieren sie, dass man theoretisch extrem niedrige nachweisbare Konzentrationen erreichen kann, begrenzt vor allem durch fundamentale Zählstatistik. Maschinelles Lernen bringt einen weiteren Vorteil, indem es erhöht, wie viele Partikel zuverlässig genutzt werden können, und die Unterscheidung zwischen echten Bindungsereignissen und zufälligem Rauschen verbessert.
Hin zu intelligenteren, nachsichtigen Bluttests
Insgesamt legt die Arbeit nahe, dass die Kombination einfacher Optik mit fortgeschrittener Bildanalyse Tests liefern kann, die mit laborbasierten Referenzverfahren konkurrieren und gleichzeitig die Variabilität realer Anwendung tolerieren. Anstatt immer präzisere Hardware zu bauen, setzt der Ansatz auf die reichhaltigen Informationen, die bereits in Bildern vorhanden sind, und überlässt der Software das Sortieren von Signal und Störfaktoren. Für Patientinnen und Patienten sowie Gesundheitssysteme könnte das zuverlässigere Point‑of‑Care‑ und selbstanwendbare Tests für gängige Blutmarker und Infektionskrankheiten bedeuten, ohne dass komplexe Geräte oder Expertinnen und Experten erforderlich sind.
Zitation: McAffee, D.B., Hu, Q., Arnob, A. et al. Homogeneous image-based digital immunoassays with high error tolerance. npj Imaging 4, 30 (2026). https://doi.org/10.1038/s44303-026-00164-9
Schlüsselwörter: digitaler Immunoassay, Nanopartikel‑Bildgebung, Maschinelles Lernen Diagnostik, Punkt‑of‑Care‑Tests, SARS‑CoV‑2‑Antikörper