Clear Sky Science · pt
Imunoensaios digitais homogêneos baseados em imagens com alta tolerância a erros
Por que partículas minúsculas e câmeras inteligentes importam
Muitos dos testes médicos atuais exigem um laboratório completo com pessoal qualificado ou oferecem respostas rápidas, porém grosseiras, em uma tira simples. Este artigo apresenta uma forma de obter o melhor dos dois mundos: precisão de nível laboratorial a partir de uma pequena amostra de sangue usando hardware simples, com a maior parte do processamento feita por análise de imagem inteligente. Observando como partículas de ouro minúsculas se comportam em uma gota de sangue e permitindo que software de aprendizado de máquina interprete essas imagens, os autores mostram um caminho para testes domésticos e clínicos que são fáceis de usar e difíceis de enganar.
De mudanças de cor à contagem de partículas
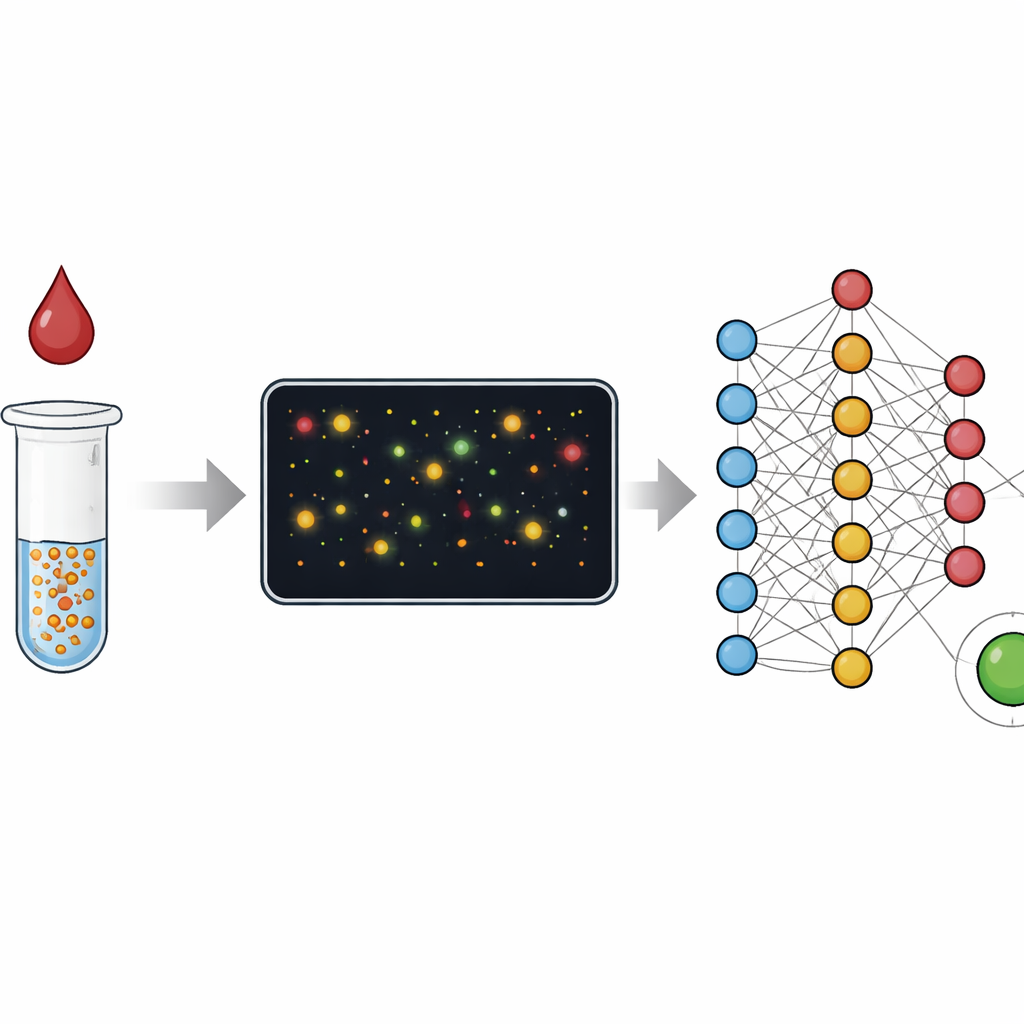
Testes tradicionais de sangue, como ELISA, medem uma mudança de cor média proveniente de milhões de moléculas em um poço, algo como avaliar uma multidão pelo nível geral de ruído. Testes rápidos em tira, ou ensaios de fluxo lateral, funcionam com a mesma ideia e trocam precisão por velocidade e simplicidade. Neste estudo, os pesquisadores focalizam em vez disso nanopartículas de ouro individuais que se aglomeram quando encontram seu alvo na amostra, como proteína C‑reativa associada à inflamação ou anticorpos contra o vírus que causa a COVID‑19. Em vez de medir apenas a cor global da solução, eles usam microscopia de campo escuro para imagear pequenos campos repletos dessas partículas e aglomerados, e então analisam cada um. Essa mudança do “analógico” da cor para a contagem “digital” amplia consideravelmente a faixa de concentrações que o teste pode medir e facilita identificar quando algo deu errado.
Enxergando através da bagunça em amostras do mundo real
Amostras de sangue reais são bagunçadas: contêm células vermelhas, detritos, bolhas e outras fontes de ruído visual que podem confundir regras simples de processamento de imagem. A equipe primeiro demonstra que, mesmo com algoritmos convencionais ajustados, é possível extrair uma relação limpa e quase linear entre o tamanho do aglomerado e os níveis de proteína C‑reativa, fazendo isso diretamente no sangue total sem centrifugar as células. Para lidar de forma mais sistemática com artefatos, eles treinam então um modelo de segmentação que rotula cada pixel da imagem como nanopartícula, célula, poeira ou fundo. Após filtrar tudo exceto as partículas verdadeiras, novamente usam o tamanho do aglomerado como leitura. Com essa abordagem híbrida, classificam corretamente o status de anticorpos contra COVID‑19 em soros de pacientes armazenados com 96% de especificidade e 90% de sensibilidade, mesmo com imagens coletadas em condições deliberadamente propensas a erros.
Deixando o computador descobrir o que importa
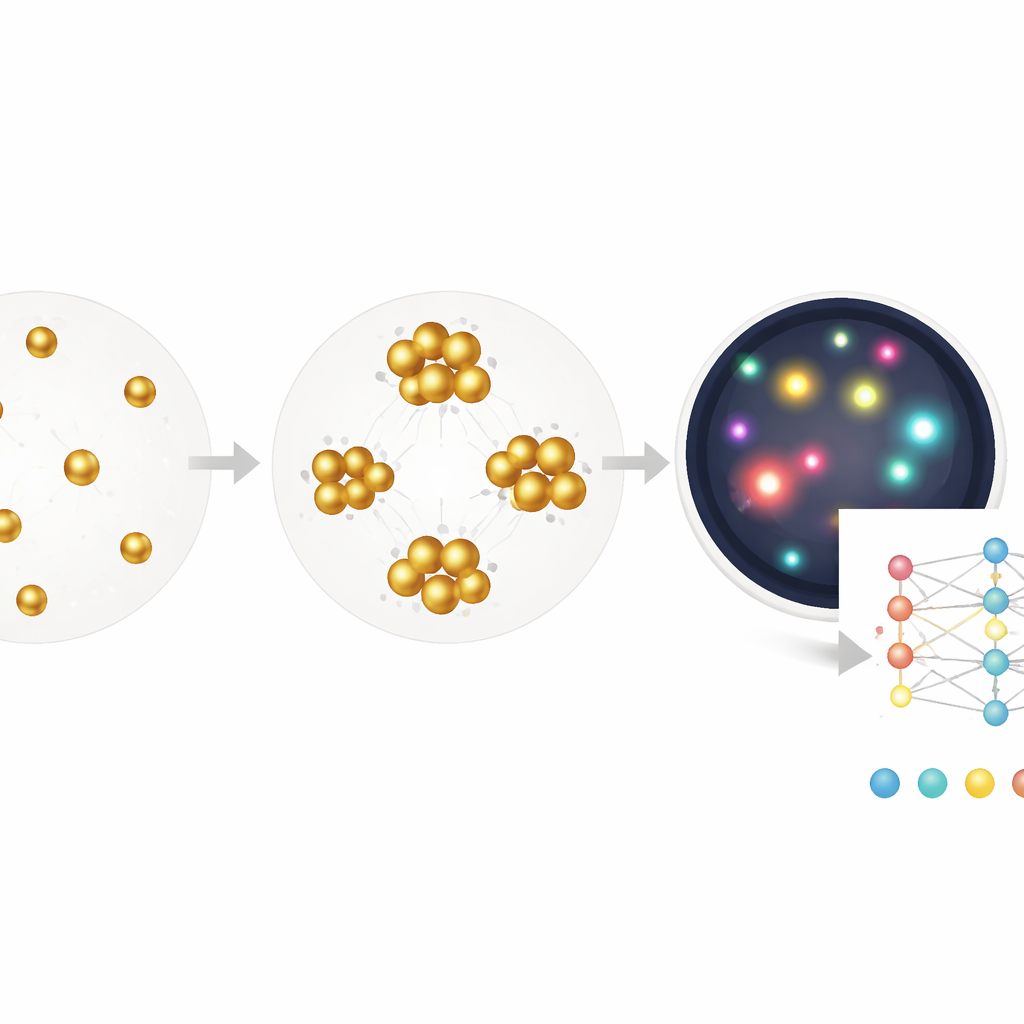
Embora o método de segmentação ajude, ele ainda depende de escolhas humanas sobre quais características medir — por exemplo, quão grande ou brilhante um aglomerado deve ser. Os autores avançam ao treinar uma rede neural profunda para ir diretamente de uma imagem bruta à concentração de anticorpos antivirais, usando apenas a concentração conhecida como rótulo e sem anotações a nível de pixel. Esse modelo de ponta a ponta, baseado em uma arquitetura ResNet padrão, aprende efetivamente sua própria combinação de sinais: sutis mudanças de cor, densidade, forma dos aglomerados, espaços vazios e mais. Ao ser testado em amostras novas, estima níveis de anticorpos numa faixa superior a três ordens e meia de magnitude, com um limite de detecção aproximando‑se do de um kit ELISA clínico, mas exige apenas uma única incubação de 30 minutos e funciona com volumes muito pequenos.
Projetando testes que podem ser afinados como um microscópio
Além de demonstrar ensaios funcionais, o estudo também investiga o quão longe esse tipo de contagem digital de partículas pode, em princípio, ser levado. Usando um arcabouço matemático e de simulação, os autores mostram que a sensibilidade desses testes não é fixa; ela depende de quantas partículas são usadas, de quão uniformes elas são e de quão bem partículas simples e pares podem ser distinguidas pela intensidade. Ajustando esses controles — especialmente o número de partículas e sua qualidade —, eles argumentam que, em teoria, é possível atingir concentrações detectáveis extremamente baixas, limitadas principalmente por estatísticas fundamentais de contagem. O aprendizado de máquina acrescenta outro ganho ao aumentar quantas partículas podem ser usadas com confiança e ao melhorar a discriminação entre eventos reais de ligação e ruído aleatório.
Rumo a testes sanguíneos mais inteligentes e permissivos
No conjunto, o trabalho sugere que emparelhar óptica simples com análise de imagem avançada pode oferecer testes que rivalizam com métodos laboratoriais de referência, enquanto toleram a variabilidade do uso no mundo real. Em vez de construir hardware cada vez mais preciso, a abordagem apoia‑se na rica informação já presente nas imagens e deixa o software separar sinal e ruído. Para pacientes e sistemas de saúde, isso pode significar testes ponto de atendimento e autoadministrados mais confiáveis para marcadores sanguíneos comuns e doenças infecciosas, sem a necessidade de instrumentos complexos ou operadores especializados.
Citação: McAffee, D.B., Hu, Q., Arnob, A. et al. Homogeneous image-based digital immunoassays with high error tolerance. npj Imaging 4, 30 (2026). https://doi.org/10.1038/s44303-026-00164-9
Palavras-chave: ensaio imuno digital, imageamento de nanopartículas, diagnósticos por aprendizado de máquina, testes ponto de atendimento, anticorpos SARS-CoV-2