Clear Sky Science · sv
En generativ förklarbar modell för förutsägelse av antimikrobiella peptider med bidirektionellt temporalt konvolutionellt neuralt nätverk
Kämpa mot infektioner och cancer med smarta peptider
Läkemedel som kan döda farliga mikrober och cancerceller utan att skada frisk vävnad är en långvarig dröm inom medicinen. Naturen producerar redan sådana molekyler: antimikrobiella peptider, små proteinfragment som bildar hål i mikrobiella membran och även kan modulera immunsystemet. Men att hitta de mest lovande peptiderna bland det enorma antalet möjliga aminosyrasekvenser är som att leta efter nålar i en höstack. Denna studie presenterar en kraftfull artificiell intelligens-ram, GAC-BiTCNN-AMP, som lär sig från stora biologiska datapooler för att förutsäga vilka peptider som sannolikt blir effektiva antimikrobiella medel och potentiella cancerterapier.
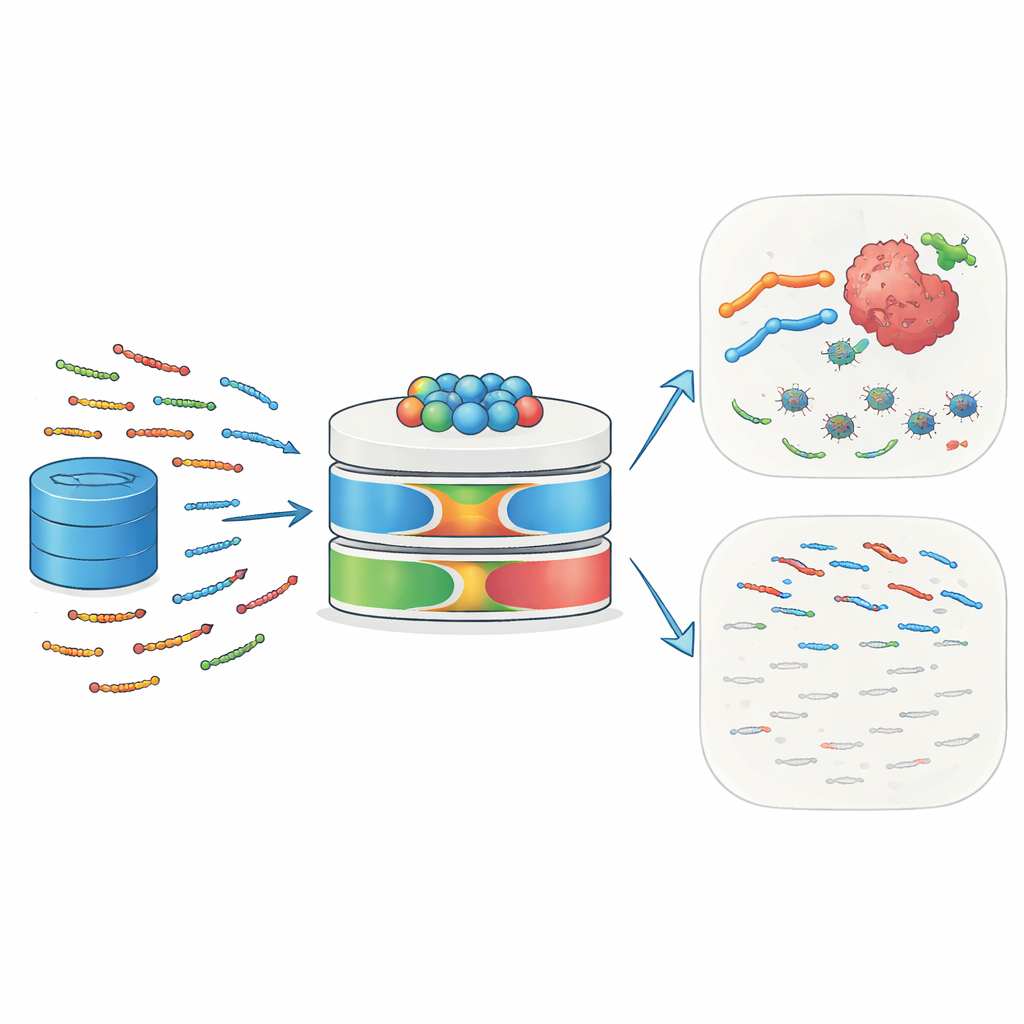
Naturens små livvakter
Antimikrobiella peptider (AMPs) är korta kedjor om 10 till 50 aminosyror som finns hos människor, djur, växter och mikrober. De fungerar som en första försvarslinje genom att binda till mikrobiella ytor, störa deras membran och utlösa celldöd. Många AMPs rekryterar också immunceller, påverkar inflammation och omformar den lokala vävnadsmiljön. Cancerceller, med sina ovanligt laddade och oordnade membran, kan vara särskilt sårbara för sådana peptider. Vissa välkända exempel—inklusive melittin och defensiner—har visat förmåga att döda tumörceller, göra dem mer känsliga för cytostatika eller strålning och stimulera immunrespons mot tumörer. Denna dubbla roll mot infektion och cancer gör AMPs till attraktiva kandidater för nästa generations precisionsläkemedel.
Varför traditionella förutsägningsverktyg inte räcker till
Trots deras potential är det fortfarande svårt att identifiera nya AMPs in silico. Tidigare datormodeller förlitade sig huvudsakligen på enkla sekvensmönster och klassiska maskininlärningstekniker. De ignorerade ofta rikare information om hur aminosyror interagerar över långa avstånd i ett protein, hur dessa sekvenser har utvecklats och vilka subtila fysikaliska egenskaper som gör en peptid både aktiv och selektiv. Många modeller använde begränsade eller redundanta träningsdata, hoppade över systematisk funktionsurval och erbjöd liten tolkbarhet—forskare kunde inte enkelt se vilka delar av indata som drev en förutsägelse. Som ett resultat var deras noggrannhet och förmåga att generalisera till nya peptider begränsade, och de hade svårt att fånga de mångsidiga biologiska roller AMPs kan spela.
Bygga en rikare bild från sekvenser
För att överbrygga dessa brister samlade författarna först en stor, noggrant filtrerad dataset från sex AMP-databaser och UniProt. De särskiljde aktiva peptider från inaktiva med strikta experimentella kriterier och minskade redundans så att nära besläktade sekvenser inte skulle blåsa upp prestandan. Därefter transformerade de varje peptidsekvens till flera kompletterande numeriska vyer. Tre toppmoderna proteinspråksmodeller—ProtTrans-T5, UniRep och ESM-2—användes för att generera högdimensionella inbäddningar som kodar kontext, långdistansberoenden och evolutionära mönster inlärda från miljontals proteiner. En anpassad deskriptor kallad PsePSSM-DCT lade till information om hur varje position i en sekvens tenderar att mutera under evolution och hur dessa mönster varierar jämnt längs sekvensen. Ett funktionsurvalssteg baserat på XGBoost destillerade sedan dessa rika representationer till de mest informativa komponenterna, skar bort brus samtidigt som signal bevarades.
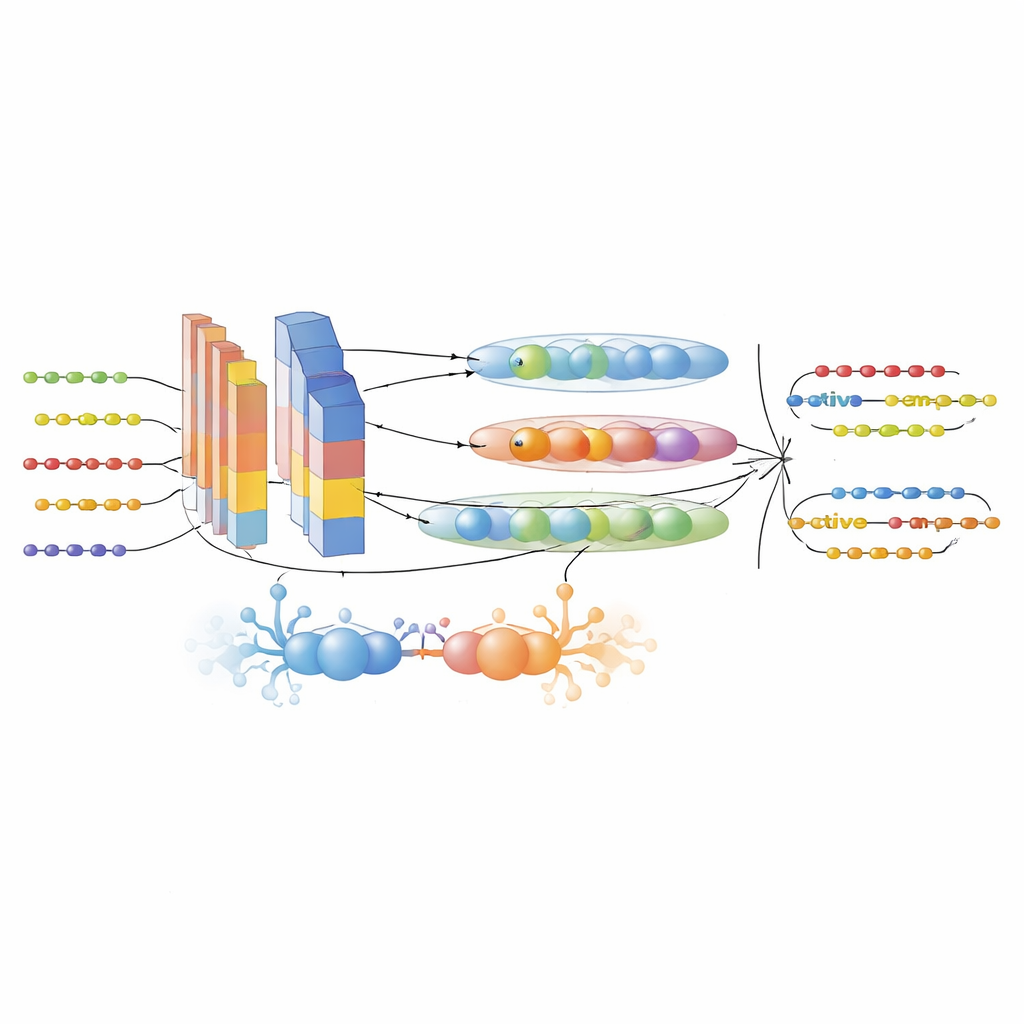
En hybrid AI-motor för peptidupptäckt
Kärnan i ramverket är GAC-BiTCNN-modellen, en hybrid djupinlärningsarkitektur särskilt anpassad för sekvensdata. Den kombinerar flera idéer: en generativ adversarial-modul som skapar realistiska syntetiska funktionsvektorer för att balansera och berika träningsuppsättningen; konvolutionslager som upptäcker lokala motiv; ett bidirektionellt temporalt konvolutionellt nätverk som fångar mönster både framåt och bakåt längs sekvensen; och kapselnätverk som grupperar relaterade funktioner i små vektor"kapslar", bevarande hierarkiska relationer. Varje typ av funktion—inbäddningar från språkmodeller och evolutionära deskriptorer—bearbetas i sin egen ström och fogas sedan samman. Modellen tränades och ställdes in med korsvalidering och testades därefter på en helt separat, tidsavskild dataset med nyare peptidposter för att minimera informationsläckage.
Prestanda, förklarbarhet och vad det betyder
GAC-BiTCNN-AMP uppnådde framstående prestanda: upp till omkring 97 % noggrannhet och nästan perfekta area-under-kurvan-värden i korsvalidering, och över 95 % noggrannhet på den oberoende testuppsättningen, vilket överträffade en rad befintliga AMP-prediktorer och även finjusterade transformer-enbart baslinjer. När de olika funktionstyperna kombinerades förbättrades resultaten ytterligare, vilket visar att var och en bidrar med komplementär kunskap om peptidbeteende. För att undersöka vad modellen hade lärt sig använde författarna SHAP, en populär teknik inom förklarbar AI, för att mäta hur olika latenta funktioner påverkade förutsägelserna. Även om dessa funktioner är abstrakta bekräftade analysen att modellen förlitar sig på en kompakt uppsättning diskriminerande, biologiskt meningsfulla mönster istället för slumpmässigt brus. I klara termer verkar systemet "titta" på rätt typer av signaler.
Vad detta betyder för framtida läkemedel
För icke-specialister är huvudpoängen att detta arbete tillhandahåller ett mycket träffsäkert, datadrivet filter för att sålla igenom enorma mängder peptidsekvenser och identifiera dem som mest sannolikt fungerar som effektiva antimikrobiella eller anticancer-agenter. Genom att blanda generativ modellering, flera proteinspråksmodeller och förklarbar djupinlärning erbjuder GAC-BiTCNN-AMP ett skalbart sätt att prioritera kandidater för laboratorietester, vilket potentiellt kan påskynda utvecklingen av nya behandlingar mot infektioner och cancer som är resistenta mot nuvarande terapier. Framtida utvidgningar kan inte bara förutsäga vilka peptider som fungerar, utan också vägleda designen av helt nya sekvenser skräddarsydda för potent effekt, selektivitet och säkerhet.
Citering: Ali, F., Khalid, M., Alsini, R. et al. A generative explainable model for antimicrobial peptide prediction using bidirectional temporal convolutional neural network. Sci Rep 16, 13801 (2026). https://doi.org/10.1038/s41598-026-43370-6
Nyckelord: antimikrobiella peptider, proteinspråksmodeller, djupinlärning, precisionsonkologi, Läkemedelsupptäckt