Clear Sky Science · he
מודל מוסבר גנרטיבי לחיזוי פפטידים אנטימיקרוביאליים באמצעות רשת עצבית עוקבת-זמנית דו-כיוונית
לחימה בזיהומים ובסרטן בעזרת פפטידים חכמים
תרופות היכולות להרוג מיקרואורגניזמים מסוכנים ותאי סרטן מבלי לפגוע ברקמות בריאות הן שאיפה ותיקה ברפואה. טבע כבר מייצר מולקולות כאלה: פפטידים אנטימיקרוביאליים, קטעי חלבון זעירים החודרים לממברנות של מיקרובים ולעיתים גם ממודלים את המערכת החיסונית. אך מציאת הפפטידים המבטיחים ביותר בתוך המרחב העצום של רצפי חומצות האמינו היא כמו חיפוש מחט בערימת שחת. המחקר הזה מציג מסגרת בינה מלאכותית עוצמתית, GAC-BiTCNN-AMP, שלומדת מתוך מאגרי ביולוגיה גדולים ומנבאת אילו פפטידים צפויים לשמש כסוכנים אנטימיקרוביאליים יעילים וכמועמדים טיפוליים נגד סרטן.
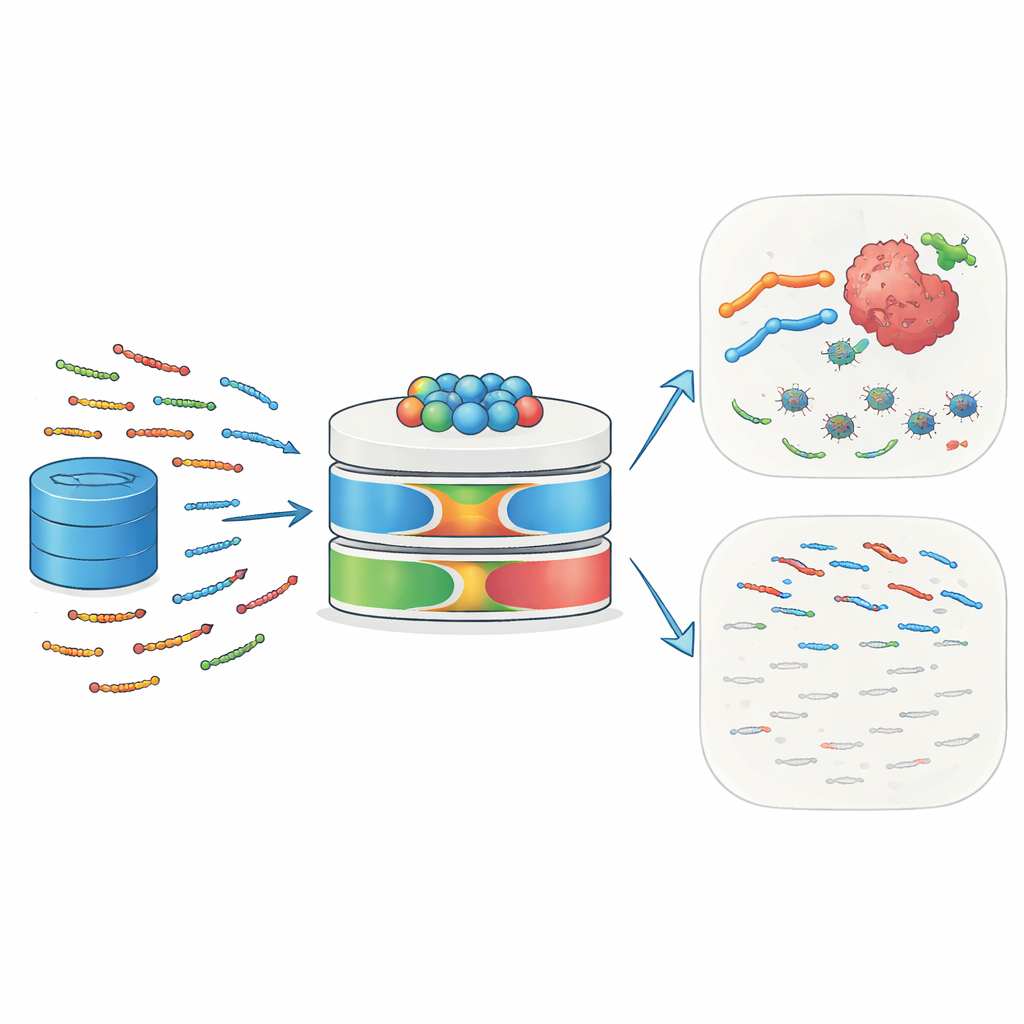
שומרי הגוף הזעירים של הטבע
פפטידים אנטימיקרוביאליים (AMPs) הם שרשרות קצרות של 10–50 חומצות אמינו הנמצאות באדם, בבעלי חיים, בצמחים ובמיקרובים. הם פועלים כקו ההגנה הראשון על ידי קשירה למשטחים מיקרוביאליים, שיבוש ממברנות והפעלת מוות תאי. רבים מה-AMPs גם מגייסים תאים חיסוניים, משפיעים על דלקת ומשנים את סביבת הרקמה המקומית. תאי סרטן, עם ממברנות בעלות מטען בלתי רגיל ומבנה לא מסודר, עשויים להיות פגיעים במיוחד לפפטידים כאלה. דוגמאות מוכרות — כולל מליטין ודפנסינים — הראו יכולת להרוג תאי גידול, להגביר רגישות לכימותרפיה או לקרינה ולגרות תגובות חיסוניות נגד הגידול. התפקיד המשולב הזה נגד זיהומים וסרטן הופך את ה-AMPs למועמדים אטרקטיביים לתרופות מדויקות בדור הבא.
מדוע כלי הניבוי המסורתיים אינם מספיקים
למרות ההבטחה, זיהוי AMPs באופן חישובי נשאר מאתגר. מודלים מחשביים מוקדמים הסתמכו בעיקר על דפוסי רצף פשוטים וטכניקות למידת מכונה קלאסיות. הם התעלמו לעיתים קרובות ממידע עשיר על אינטראקציות בין חומצות אמינו במרחקים ארוכים בחלבון, מאופן האבולוציה של הרצפים, ומהתכונות הפיזיקליות העדינות שהופכות פפטיד לאקטיבי ובעל סלקטיביות. מודלים רבים השתמשו בנתוני אימון מוגבלים או מיותרים, דילגו על בחירה שיטתית של תכונות וסיפקו מעט יכולת פרשנות — החוקרים לא יכלו בקלות לזהות אילו היבטים של הקלט הניעו את הניבוי. כתוצאה מכך, הדיוק ויכולת ההכללה שלהם לרצפים חדשים היו מוגבלים, והם התקשו ללכוד את תפקידי הביולוגיים המגוונים ש-AMPs יכולים למלא.
בניית תמונה עשירה יותר מתוך רצפים
כדי לצמצם פערים אלה, המחברים הרכיבו תחילה מאגר גדול ומסונן בקפידה משישה מאגרי AMP ו-UniProt. הם הבחינו בין פפטידים פעילים ללא-פעילים באמצעות קריטריונים ניסיוניים מחמירים והקטינו כפילויות כך שרצפים קרובים לא ינפחו את הביצועים. לאחר מכן המירו כל רצף פפטיד למספר תצוגות מספריות משלימות. שלושה מודלי שפה מתקדמים לחלבונים — ProtTrans-T5, UniRep ו-ESM-2 — שימשו ליצירת הצגות ממדיות-גבוהות המקודדות הקשר, תלות ארוכת טווח ודפוסי אבולוציה הנלמדים ממיליוני חלבונים. תיאורן מותאם בשם PsePSSM-DCT הוסיף מידע על נטיית המוטציה בכל מיקום ברצף וכיצד דפוסים אלה משתנים בצורה חלקה לאורך הרצף. שלב בחירת תכונות מבוסס XGBoost זיקק אז את הייצוגים העשירים הללו למרכיבים המידעיים ביותר, חותך רעש ושומר על אות.
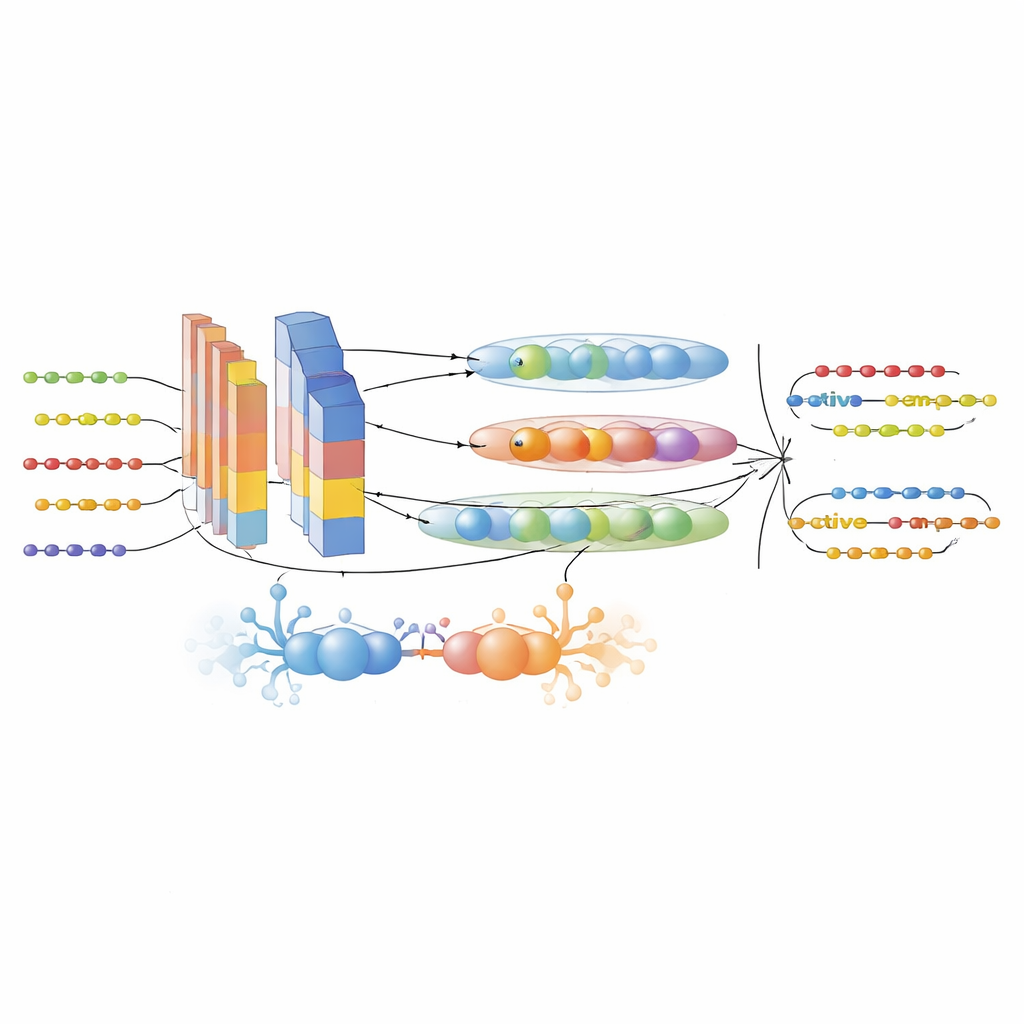
מנוע בינה מעורב לגילוי פפטידים
הלב של המסגרת הוא המודל GAC-BiTCNN, ארכיטקטורת למידת-עומק היברידית המתואמת במיוחד לנתוני רצף. היא משלבת כמה רעיונות: מודול אדרסרי גנרטיבי שיוצר וקטורי תכונה סינטטיים ריאליסטיים כדי לאזן ולעשיר את סט האימון; שכבות קונבולוציה שמגלות מוטיבים מקומיים; רשת קונבולוציה זמנית דו-כיוונית שתופסת דפוסים המתקדמים קדימה ואחורה לאורך הרצף; ורשתות קפסולות שמאגדות תכונות קשורות ל"קפסולות" וקטוריות קטנות השומרות על יחסים היררכיים. כל סוג של תכונה — הצגות ממודל השפה ותיאורים אבולוציוניים — מעובד בזרם נפרד ומשולב מאוחר יותר. המודל אומן וכוונן באמצעות צליבה (cross-validation) ונבדק על מאגר נתונים עצמאי, מופרד בזמן, של כניסות פפטיד חדשות כדי למזער דלף מידע.
ביצועים, אפשרות לפרשנות ומה משמעות הדבר
GAC-BiTCNN-AMP השיג ביצועים בולטים: עד כ־97% דיוק ונקודות שטח תחת העקומה קרובות למושלמות בצליבה, ולמעלה מ־95% דיוק במערך המבחן העצמאי, כשהוא עוקף מגוון מנבי AMP קיימים ואפילו בסיסים של טרנספורמרים מלאכית-התאמה. כאשר סוגי התכונות השונים שולבו, התוצאות השתפרו עוד יותר, מה שמראה שכל אחד מהם תורם ידע משלים על התנהגות הפפטיד. כדי לבחון מה המודל למד, המחברים השתמשו ב-SHAP, טכניקת explainable-AI פופולרית, למדידת השפעת תכונות לטנטיות שונות על הניבויים. למרות שהתכונות הללו מופשטות, הניתוח אישר שהמודל מסתמך על סט קומפקטי של דפוסים מבדילים ובעלי משמעות ביולוגית במקום על רעש אקראי. במילים פשוטות, המערכת נראית "מביטה" בסוגי האותות הנכונים.
מה משמעות הדבר עבור תרופות עתידיות
ללא-מומחים, המסקנה המרכזית היא שעבודה זו מספקת מסננת מדוייקת ומונעת-נתונים למיון מספרים עצומים של רצפי פפטידים כדי לזהות את אלה שמועמדים לפעילות אנטימיקרוביאלית או אנטי-סרטנית. על ידי שילוב דגמי גנרטיביים, מספר מודלי שפה לחלבונים ולמידת-עומק בעלת יכולת פרשנות, GAC-BiTCNN-AMP מציע דרך סקיילבילית לתעדוף מועמדים לניסויים במעבדה, ובכך עשוי להאיץ פיתוח טיפולים חדשים לזיהומים ולסרטנים העמידים לטיפולים קיימים. הרחבות עתידיות עשויות לא רק לחזות אילו פפטידים פועלים, אלא גם להנחות בעיצוב רצפים חדשים המותאמים לעוצמה, סלקטיביות ובטיחות.
ציטוט: Ali, F., Khalid, M., Alsini, R. et al. A generative explainable model for antimicrobial peptide prediction using bidirectional temporal convolutional neural network. Sci Rep 16, 13801 (2026). https://doi.org/10.1038/s41598-026-43370-6
מילות מפתח: פפטידים אנטימיקרוביאליים, מודלי שפה לחלבונים, למידת עומק, אונקולוגיה מדויקת, גילוי תרופות