Clear Sky Science · ja
双方向時系列畳み込みニューラルネットワークを用いた抗菌ペプチド予測のための生成的説明可能モデル
賢いペプチドで感染症とがんに挑む
危険な微生物やがん細胞を倒しつつ正常組織を傷つけない薬剤は、医療の長年の夢です。自然界には既にそのような分子が存在します:抗菌ペプチドは微生物膜に孔を開け、免疫系も調節する小さなタンパク質断片です。しかし、膨大な可能なアミノ酸配列の中から有望なペプチドを見つけることは干し草の中の針を探すようなものです。本研究は、GAC-BiTCNN-AMPという強力な人工知能フレームワークを紹介します。これは大規模な生物データから学習して、どのペプチドが抗菌剤や潜在的ながん治療薬として有望かを予測します。
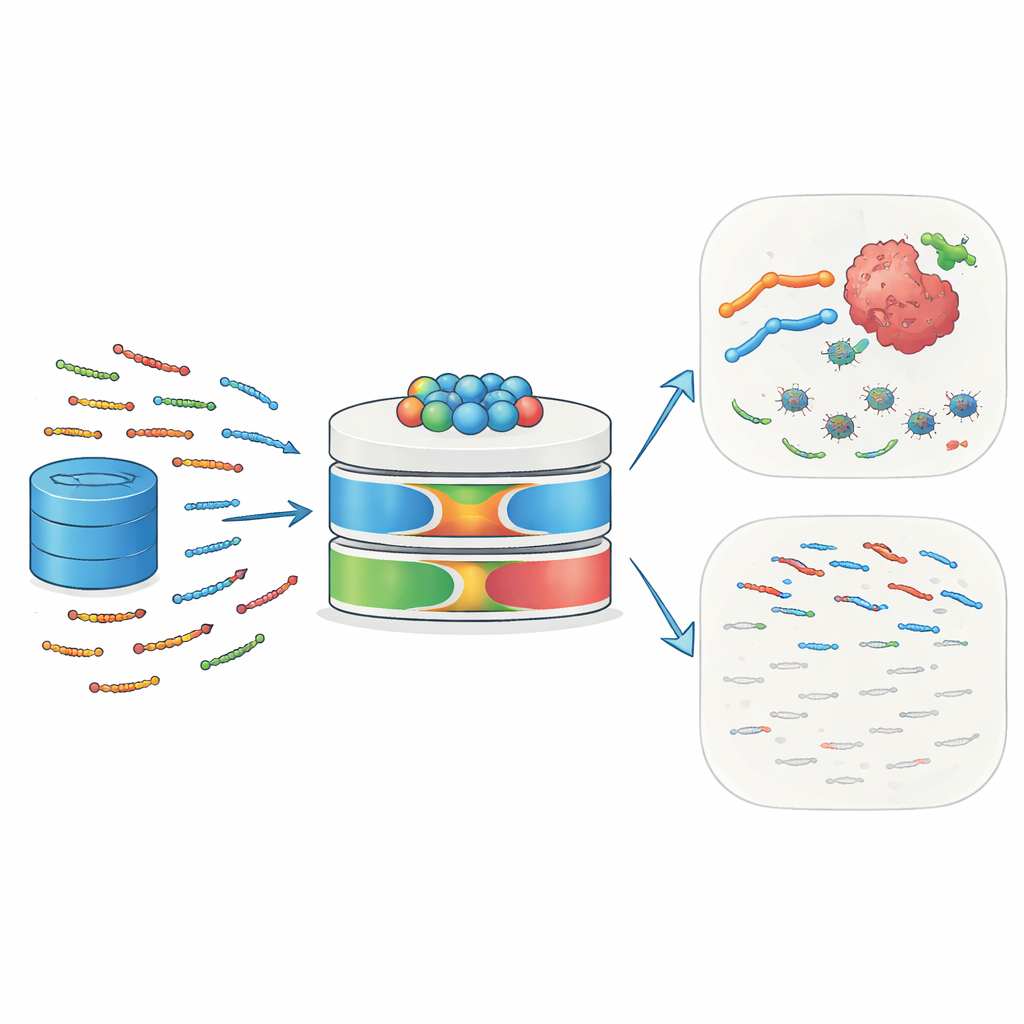
自然の小さな護衛
抗菌ペプチド(AMP)は、ヒトや動物、植物、微生物に見られる長さ10〜50の短いアミノ酸鎖です。これらは微生物表面に結合して膜を乱し、細胞死を誘導することで第一線の防御を担います。多くのAMPは免疫細胞を呼び寄せ、炎症に影響を与え、局所の組織環境を変化させます。電荷が偏り無秩序な膜を持つがん細胞は、こうしたペプチドに特に脆弱であることが多いです。メレチンやディフェンシンなどのよく知られた例は、腫瘍細胞を殺す、化学療法や放射線感受性を高める、腫瘍に対する免疫応答を刺激するといった能力を示しています。感染症とがんの双方に対するこの二重の役割が、AMPを次世代の精密医療候補として魅力的にしています。
従来の予測ツールが不足している点
有望ではあるものの、インシリコで新たなAMPを同定するのは依然として難しいです。従来の計算モデルは主に単純な配列パターンや古典的な機械学習手法に依存していました。これらはタンパク質内での長距離にわたるアミノ酸の相互作用、配列の進化的背景、活性と選択性に関わる微妙な物理的特徴といった豊富な情報を無視する傾向がありました。多くのモデルは限られた、あるいは冗長な訓練データを用い、体系的な特徴選択を省き、解釈可能性も乏しく—研究者がどの入力要素が予測を駆動しているかを容易に把握できませんでした。その結果、精度や新規ペプチドへの一般化能力が制約され、AMPが果たす多様な生物学的役割を捉えきれませんでした。
配列からより豊かな図を描く
これらのギャップを埋めるために、著者らはまず6つのAMPデータベースとUniProtから大規模で注意深くフィルタリングされたデータセットを構築しました。厳格な実験基準で活性ペプチドと非活性ペプチドを区別し、近縁な配列による性能の水増しを防ぐため冗長性を低減しました。次に各ペプチド配列を複数の補完的な数値表現に変換しました。最先端の3つのタンパク質言語モデル—ProtTrans-T5、UniRep、ESM-2—を用いて、文脈、長距離依存性、数百万のタンパク質から学んだ進化的パターンを符号化する高次元埋め込みを生成しました。カスタム記述子PsePSSM-DCTは、配列中の各位置が進化的にどのように変異しやすいか、またそのパターンが配列に沿ってどのように滑らかに変化するかに関する情報を付加しました。最後にXGBoostに基づく特徴選択ステップで、これら豊富な表現から最も情報量の多い成分を抽出し、ノイズを削ぎ落としつつ信号を保持しました。
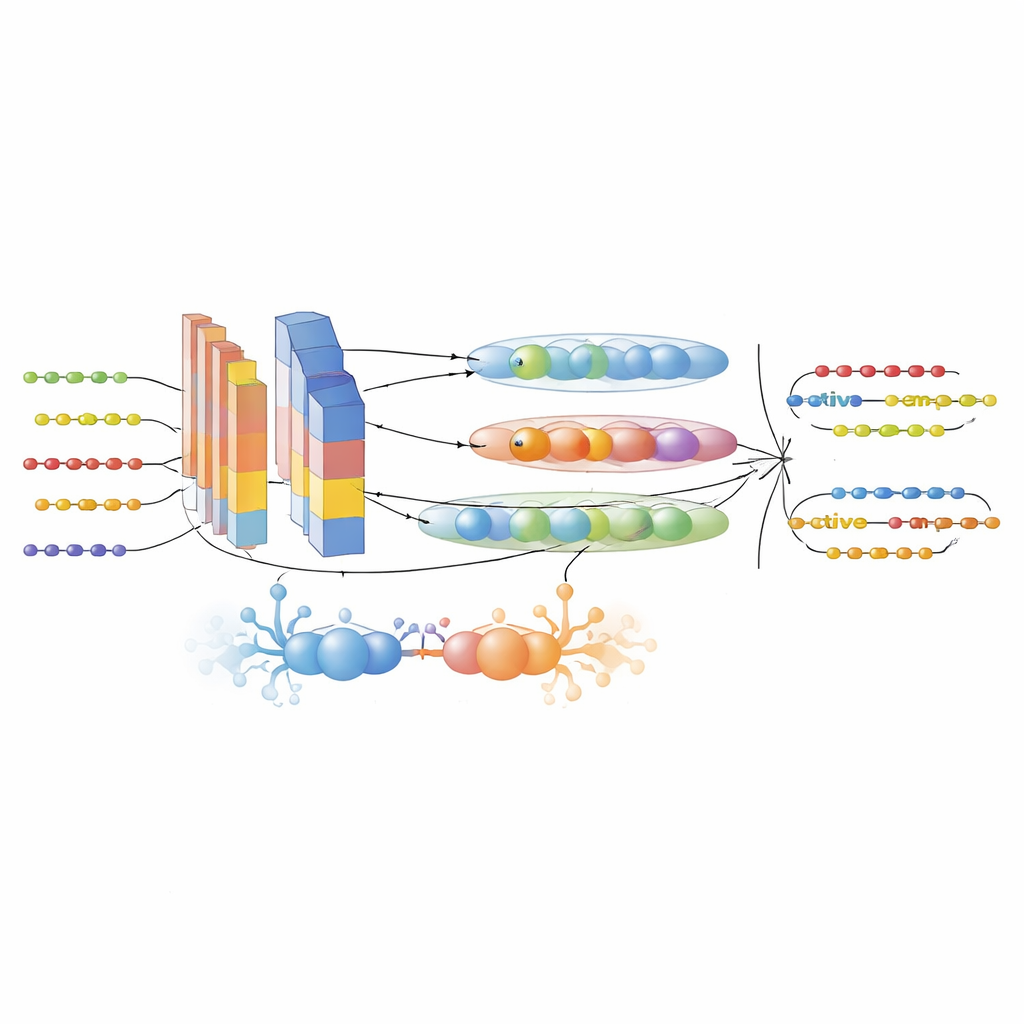
ペプチド探索のためのハイブリッドAIエンジン
フレームワークの中心はGAC-BiTCNNモデルであり、配列データに特化したハイブリッド深層学習アーキテクチャです。いくつかのアイデアを組み合わせています:訓練セットを均衡化し強化するために現実的な合成特徴ベクトルを生成する生成的敵対モジュール;局所的モチーフを検出する畳み込み層;配列に沿って順方向と逆方向の両方のパターンを捉える双方向時系列畳み込みネットワーク;関連する特徴を小さなベクトル「カプセル」にまとめ階層的関係を保持するカプセルネットワーク。それぞれの特徴タイプ—言語モデル埋め込みと進化的記述子—は個別のストリームで処理され、後で融合されます。モデルは交差検証で訓練・調整され、情報漏洩を最小にするために完全に別の時間的に分離された新しいペプチドエントリで構成された独立テストセットで評価されました。
性能、説明可能性、そしてその意義
GAC-BiTCNN-AMPは際立った性能を示しました:交差検証では約97%の精度とほぼ完全なAUCスコアを達成し、独立テストセットでも95%以上の精度を示し、既存のAMP予測器や単独でファインチューニングされたトランスフォーマーベースのベースラインを上回りました。異なる特徴タイプを組み合わせると結果はさらに向上し、それぞれがペプチドの挙動について補完的な知識を提供していることを示しました。モデルが学習した内容を調べるために、著者らはSHAPという代表的な説明可能AI手法を用いて、異なる潜在特徴が予測にどのように影響するかを測定しました。これらの特徴は抽象的ではあるものの、解析はモデルがランダムなノイズではなく、識別力の高い生物学的に意味のあるパターンのコンパクトなセットに依存していることを確認しました。平たく言えば、システムは「正しい種類の信号」を見ているようです。
将来の医薬品開発にとっての意味
専門外の方への要点は、本研究が膨大な数のペプチド配列をふるいにかけ、抗菌性あるいは抗がん性を持つ可能性が高い候補を高精度で選び出すデータ駆動型のフィルターを提供することです。生成モデル、複数のタンパク質言語モデル、説明可能な深層学習を組み合わせることで、GAC-BiTCNN-AMPは実験検証のための候補を優先順位付けするスケーラブルな手段を提供し、現行治療に耐性を示す感染症やがんに対する新薬開発を加速する可能性があります。将来の拡張では、どのペプチドが有効かを予測するだけでなく、効力、選択性、安全性を考慮した全く新しい配列設計を導くことも期待されます。
引用: Ali, F., Khalid, M., Alsini, R. et al. A generative explainable model for antimicrobial peptide prediction using bidirectional temporal convolutional neural network. Sci Rep 16, 13801 (2026). https://doi.org/10.1038/s41598-026-43370-6
キーワード: 抗菌ペプチド, タンパク質言語モデル, ディープラーニング, 精密医療(オンコロジー), 医薬品探索