Clear Sky Science · sv
Quemliclustat och kemoterapi med eller utan zimberelimab vid metastaserande pankreasadenokarcinom: en randomiserad fas 1‑studie
Varför denna studie är viktig
Bukspottkörtelcancer är en av de dödligaste cancerformerna, delvis därför att den ofta upptäcks först efter att den spridit sig och eftersom standardkemoterapi bara ger patienterna en kort förlängning av överlevnaden. Denna studie prövar en ny läkemedelsstrategi som inte bara syftar till att angripa tumörceller direkt, utan också att lätta en slags kemisk ”dimma” som hindrar immunsystemet från att hjälpa till. Genom att kombinera det riktade läkemedlet quemliclustat med rutinmässig kemoterapi, och ibland med en immunstimulerande antikropp, undersöker forskarna om de säkert kan förlänga överlevnaden och bättre utnyttja kroppens egna försvar.
En kemisk sköld runt tumören
Pankreastumörer skapar en ogästvänlig omgivning som gör det svårt för immunceller att utföra sitt arbete. När kemoterapi dödar cancerceller släpps en molekyl kallad ATP ut i omgivande vävnad. Ett enzym på cellers yta, känt som CD73, omvandlar snabbt ATP till adenosin, ett ämne som normalt lugnar inflammation och skyddar frisk vävnad. Inuti tumörer fungerar emellertid höga adenosinnivåer som en kemisk sköld, dämpar immunsvar och gör att cancerceller kan fortsätta leva. Det nya tablettlika läkemedlet quemliclustat blockerar CD73 i syfte att minska adenosin och göra tumörmiljön mindre välkomnande för cancer och mer inbjudande för immunceller. 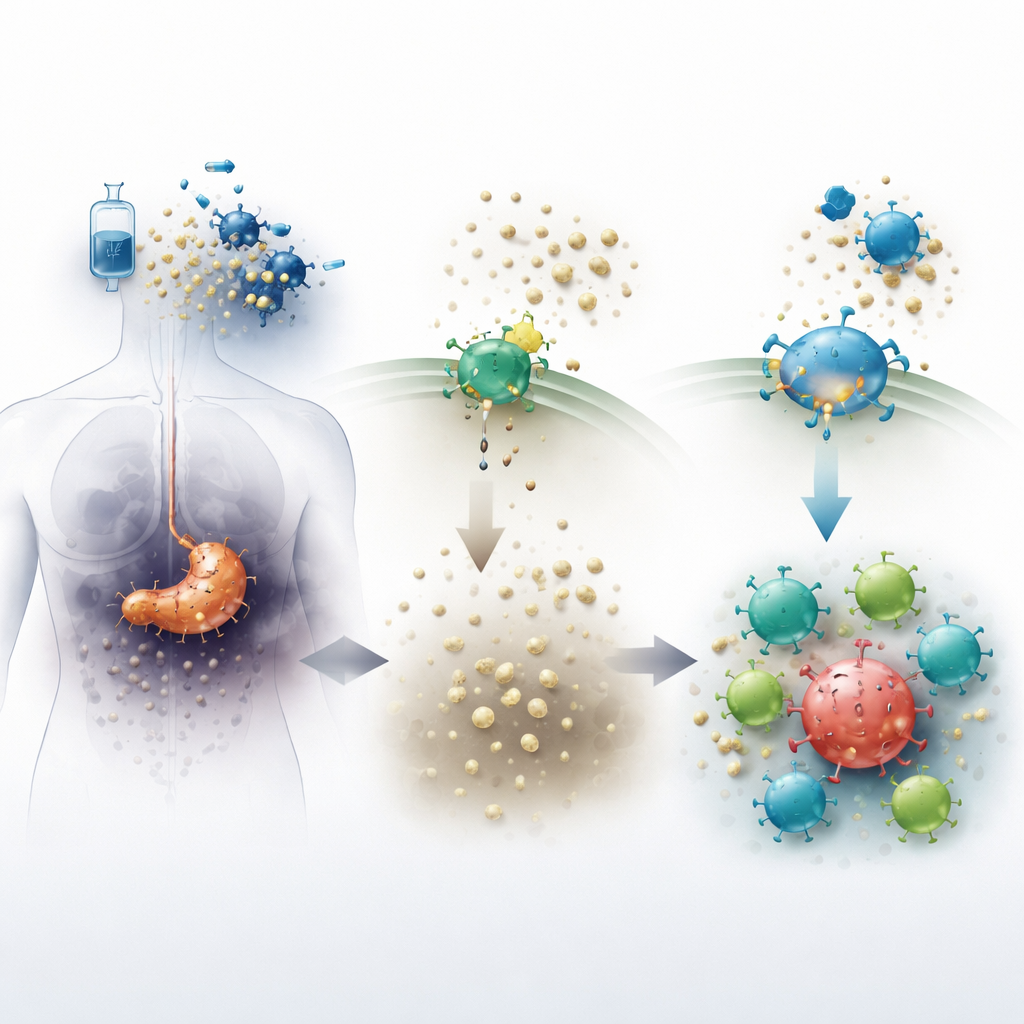
Testa en ny kombination hos patienter
ARC‑8‑studien rekryterade personer vars bukspottkörtelcancer redan hade spridit sig och som ännu inte fått behandling för metastaserande sjukdom. Alla deltagare fick en standardkemoterapikombination av gemcitabin och nab‑paklitaxel. I tidiga dosupptrappningsgrupper fick patienter också quemliclustat tillsammans med en immuncheckpoint‑antikropp kallad zimberelimab, som kan lossa molekylära bromsar på immunceller. Efter att en säker dos quemliclustat fastställts utvidgades studien till större grupper där patienterna slumpmässigt tilldelades kemoterapi plus quemliclustat antingen med eller utan zimberelimab. De huvudsakliga målen var att bedöma säkerhet och att söka tidiga tecken på nytta, såsom tumörminskning och överlevnad.
Säkerhet och tecken på överlevnad
I samtliga behandlingsarmar såg biverkningarna mycket lika ut som vad läkare förväntar sig av denna kemoterapiregim ensam, såsom trötthet, illamående och låga blodvärden. Allvarliga immunsystemrelaterade komplikationer var ovanliga, och de flesta allvarliga problemen kopplades till kemoterapin snarare än till de nya läkemedlen. När forskarna samlade patienter som fått den rekommenderade dosen av quemliclustat fann de att tumörer krympte hos ungefär en tredjedel av patienterna och förblev under kontroll hos omkring tre fjärdedelar. Medianen för total överlevnad nådde cirka 16 månader i denna grupp, vilket är märkbart längre än de ungefär 9–12 månader som setts i flera nyliga studier med enbart kemoterapi. En noggrann jämförelse med en ”syntetisk” kontrollgrupp uppbyggd från tidigare studier antydde en överlevnadsfördel på nästan sex månader för patienter som fick quemliclustat‑kombinationen.
Förstå hur läkemedlet omformar tumörmiljön
För att förstå varför vissa patienter drog mer nytta än andra tittade teamet på genaktivitetsmönster i tumörbiopsier och i laboratorieodlade celler. De fokuserade på en uppsättning gener kallad NR4A‑familjen, som aktiveras när adenosinnivåerna är höga. I odlingar ökade tillsatt adenosin eller dess föregångare NR4A‑generna i flera celltyper som finns i pankreastumörer, medan blockering av CD73 eller adenosinreceptorer höll ner denna signal. I patientprover ökade själva kemoterapin NR4A‑aktiviteten i många tumörassocierade celler, i linje med en våg av adenosin efter celldöd. Slående var att patienter vars tumörer från början hade högre NR4A‑nivåer tenderade att leva längre på quemliclustat‑terapin, men detta mönster höll inte i två externa studier där patienter fick liknande kemoterapi utan quemliclustat. 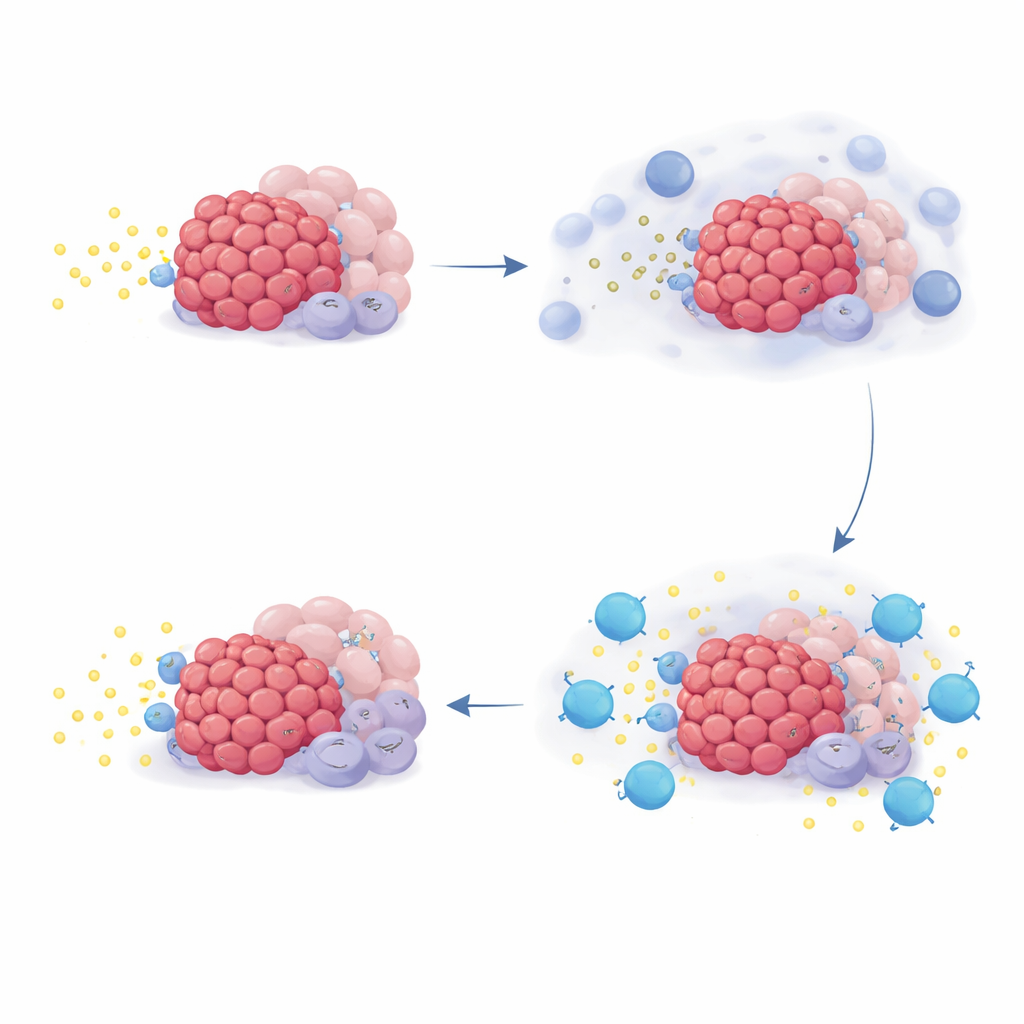
Återföra immunceller till striden
Avancerad avbildning av tumörskivor visade att områden med höga NR4A‑nivåer hade färre aktiverade mördart‑celler (CD8+ T‑celler) i närheten, vilket tyder på att adenosin skapar en gradient som håller dessa celler på avstånd. Hos patienter som hade biopsier tagna före och efter behandling minskade quemliclustat generellt NR4A‑signaler i tumörerna. De patienter som fick den största minskningen visade den starkaste ökningen i genmarkörer för T‑cellsnärvaro och aktivitet, och de hade också bäst total överlevnad, med mer än hälften fortfarande i livet efter två år. Tillsammans stöder dessa fynd idén att blockering av CD73 tunnar ut adenosin‑”dimmman”, vilket låter immunceller komma närmare cancerceller och angripa dem effektivare.
Vad detta kan innebära för patienter
Denna tidiga fas‑studie var främst designad för att pröva säkerhet och saknar en traditionell randomiserad kontrollgrupp med enbart kemoterapi, så resultaten kan ännu inte bevisa att quemliclustat förlänger livet. Ändå föreföll kombinationen vara tolererbar och gav överlevnadstider som står sig väl i jämförelse med tidigare studier. De biologiska analyserna knyter samman läkemedelsexponering, förändringar i tumörkemi och immunaktivering med patientresultat, vilket stärker argumentet att rikta in sig på adenosin är en lovande strategi. En större fas 3‑studie som nu pågår kommer att pröva om tillsats av quemliclustat till standardkemoterapi verkligen förbättrar överlevnaden för personer med metastaserande bukspottkörtelcancer.
Citering: Wainberg, Z.A., Manji, G.A., Bahary, N. et al. Quemliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1 trial. Nat Med 32, 1267–1277 (2026). https://doi.org/10.1038/s41591-026-04283-z
Nyckelord: bukspottkörtelcancer, tumörmikromiljö, immunterapi, adenosin‑vägen, klinisk prövning