Clear Sky Science · ru
Кемликлустат и химиотерапия с зимберелимабом или без него при метастатической аденокарциноме поджелудочной железы: рандомизированное исследование фазы 1
Почему это исследование важно
Рак поджелудочной железы — один из самых смертоносных видов рака, отчасти потому, что его чаще всего обнаруживают уже после распространения, а стандартная химиотерапия дает пациентам лишь небольшое дополнительное время. Это исследование проверяет новую лекарственную стратегию, направленную не только на прямое уничтожение опухолевых клеток, но и на ослабление некой химической «пелены», мешающей иммунной системе помогать. Сочетая таргетный препарат кемликлустат с обычной химиотерапией и иногда с антителом, усиливающим иммунитет, исследователи ставят вопрос, можно ли безопасно продлить выживание и лучше задействовать собственные защитные силы организма.
Химический щит вокруг опухоли
Опухоли поджелудочной железы создают враждебную среду, в которой иммунным клеткам трудно выполнять свою работу. Когда химиотерапия убивает раковые клетки, те выбрасывают в окружающую ткань молекулу ATP. Фермент на поверхности клеток, известный как CD73, быстро превращает ATP в аденозин — вещество, которое в норме помогает успокаивать воспаление и защищать здоровые ткани. Однако внутри опухолей высокий уровень аденозина действует как химический щит, подавляя атаку иммунитета и позволяя раковым клеткам выживать. Новый пероральный препарат кемликлустат блокирует CD73, стремясь снизить уровень аденозина и сделать опухолевую среду менее благоприятной для рака и более восприимчивой к иммунным клеткам. 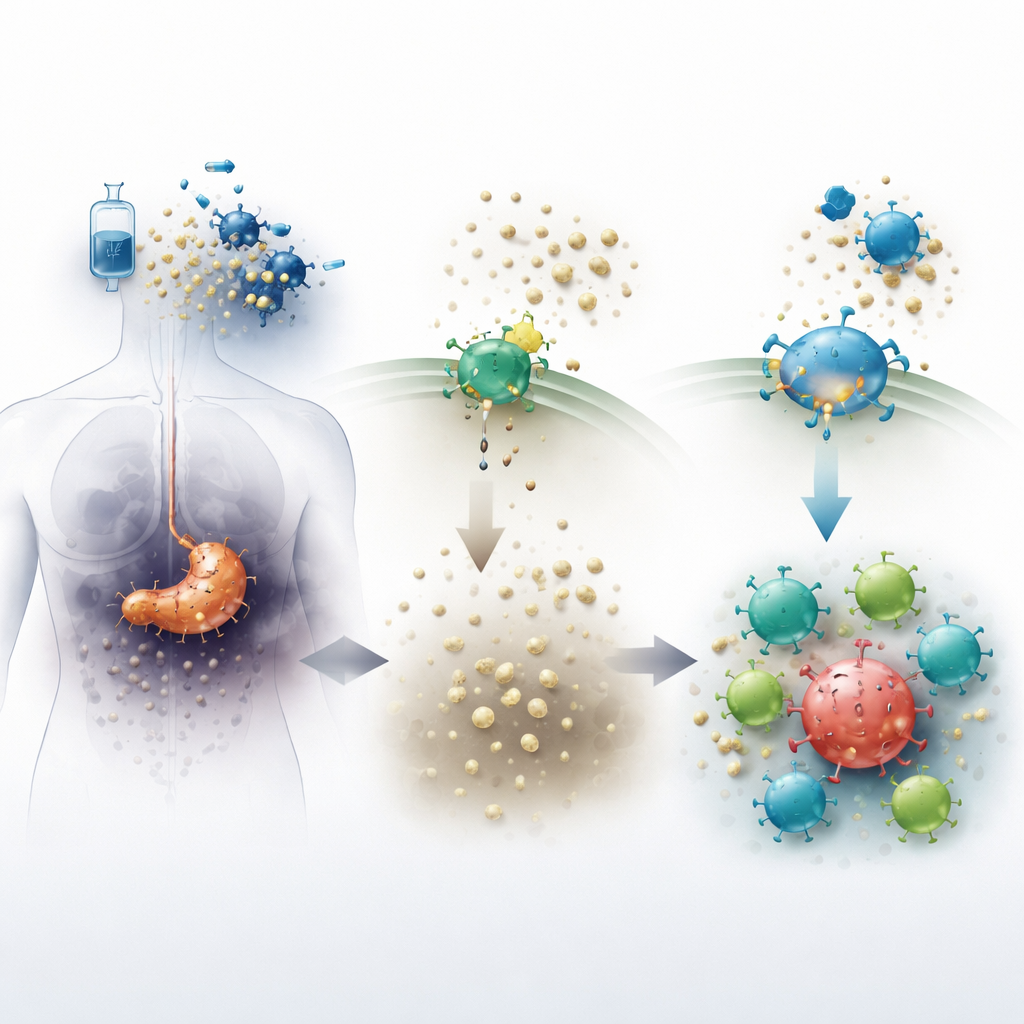
Испытание новой комбинации у пациентов
В исследование ARC‑8 были включены люди с уже распространённым раком поджелудочной железы, не получавшие ранее лечение метастатической болезни. Всем участникам назначали стандартную схему химиотерапии — гемцитабин в сочетании с наб‑паклитакселом. На ранних этапах подбора дозы пациенты также получали кемликлустат вместе с иммунной контрольной антителой зимберелимабом, которая может снимать молекулярные тормоза с иммунных клеток. После установления безопасной дозы кемликлустата исследование расширили: большие группы пациентов случайным образом распределяли на получение химиотерапии плюс кемликлустат либо с зимберелимабом, либо без него. Основные цели были — оценить безопасность и найти ранние признаки пользы, такие как уменьшение опухоли и показатель выживаемости.
Сигналы безопасности и выживания
Во всех лечебных группах побочные эффекты выглядели очень похоже на те, которые ожидают при этой химиотерапевтической схеме в одиночку — утомляемость, тошнота и снижение числа кровяных клеток. Серьёзные иммунно‑связанные осложнения встречались редко, а большинство тяжёлых проблем связывали с химиотерапией, а не с новыми препаратами. При объединении данных пациентов, получавших рекомендованную дозу кемликлустата, обнаружили, что опухоли уменьшились примерно у трети пациентов и оставались контролируемыми примерно у трёх четвертей. Медиана общей выживаемости в этой группе достигла примерно 16 месяцев, что заметно больше по сравнению с примерно 9–12 месяцами в нескольких недавних исследованиях только химиотерапии. Тщательное сравнение с «синтетической» контрольной группой, собранной из прежних исследований, предполагает преимущество в выживаемости почти на шесть месяцев для пациентов, получавших комбинацию с кемликлустатом.
Понимание того, как препарат перестраивает окружение опухоли
Чтобы выяснить, почему некоторые пациенты получали больше пользы, команда изучила модели активности генов в биоптатах опухолей и в клетках, выращенных в лаборатории. Они сосредоточились на наборе генов семейства NR4A, которые включаются при высоком уровне аденозина. В культурах добавление аденозина или его предшественников усиливало экспрессию NR4A в нескольких типах клеток, обнаруживаемых в опухолях поджелудочной железы, тогда как блокада CD73 или аденозиновых рецепторов подавляла этот сигнал. В образцах пациентов сама химиотерапия повышала активность NR4A во многих ассоциированных с опухолью клетках, что согласуется с выбросом аденозина после повреждения клеток. Примечательно, что пациенты, чьи опухоли изначально имели более высокий уровень NR4A, как правило, жили дольше на терапии кемликлустатом, но этот паттерн не наблюдался в двух внешних исследованиях, где пациенты получали подобную химиотерапию без кемликлустата. 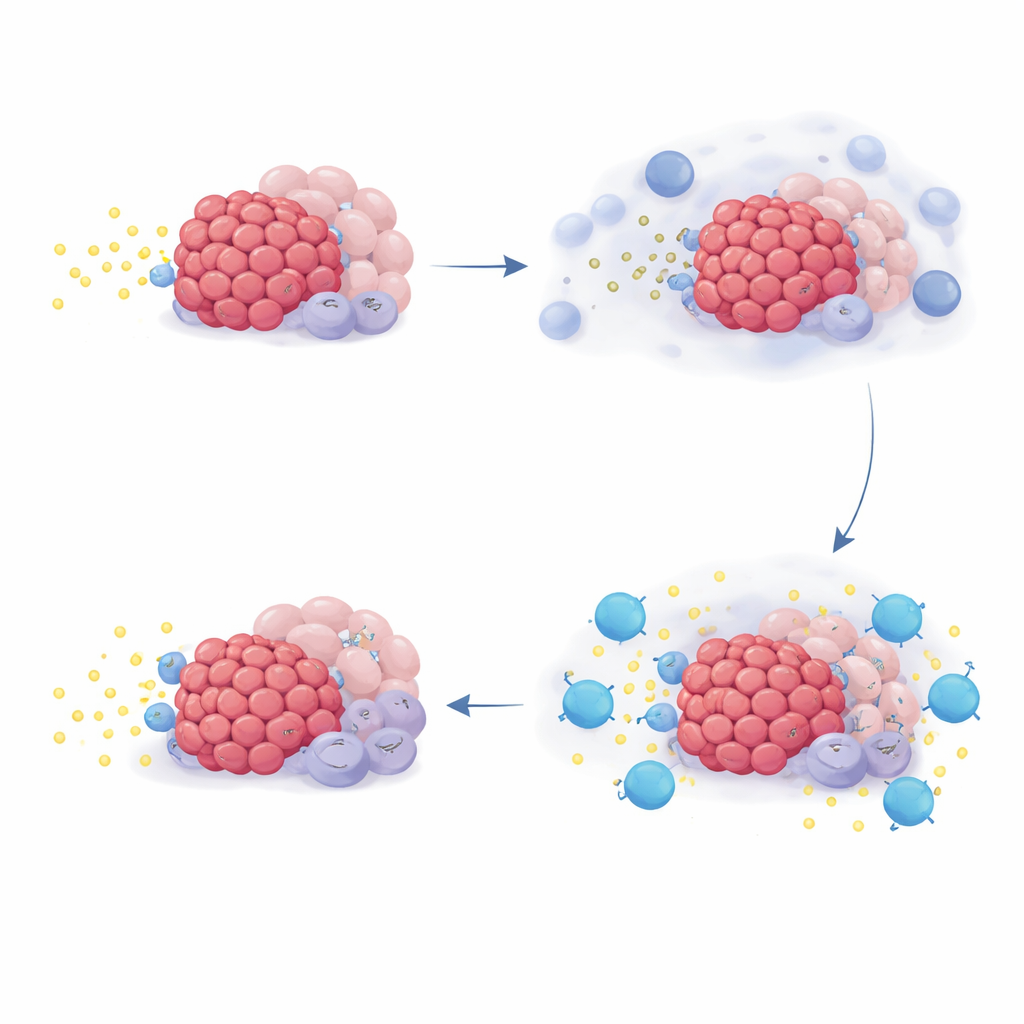
Возвращение иммунных клеток в бой
Современная визуализация срезов опухолей показала, что в областях с высоким уровнем NR4A рядом было меньше активированных цитотоксических Т‑клеток, что указывает на то, что аденозин создаёт градиент, удерживающий эти клетки на расстоянии. У пациентов, у которых брали биопсии до и после лечения, кемликлустат в целом снижал сигналы NR4A в опухолях. У тех, у кого падение было наибольшим, наблюдалось самое сильное повышение генетических маркеров присутствия и активности Т‑клеток, и именно они показали лучшую общую выживаемость — более половины оставались живы дольше двух лет. В совокупности эти данные поддерживают идею, что блокада CD73 рассеивает «туман» аденозина, позволяя иммунным клеткам приблизиться к раковым клеткам и эффективнее атаковать их.
Что это может значить для пациентов
Это раннее фазовое исследование было в первую очередь нацелено на проверку безопасности и не имеет традиционной рандомизированной контрольной группы только с химиотерапией, поэтому его результаты пока не доказывают, что кемликлустат продлевает жизнь. Тем не менее комбинация оказалась переносимой и продемонстрировала показатели выживаемости, сопоставимые с или более благоприятные по сравнению с прошлыми исследованиями. Биологические анализы связывают воздействие препарата, изменения в химии опухоли и активацию иммунитета с исходами у пациентов, что укрепляет доводы в пользу того, что таргетирование аденозина — многообещающая стратегия. В настоящее время проводится более крупное исследование фазы 3, которое проверит, действительно ли добавление кемликлустата к стандартной химиотерапии улучшает выживаемость людей с метастатическим раком поджелудочной железы.
Цитирование: Wainberg, Z.A., Manji, G.A., Bahary, N. et al. Quemliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1 trial. Nat Med 32, 1267–1277 (2026). https://doi.org/10.1038/s41591-026-04283-z
Ключевые слова: рак поджелудочной железы, опухолевая микросреда, иммунотерапия, аденозиновый путь, клиническое исследование