Clear Sky Science · nl
Quemliclustat en chemotherapie met of zonder zimberelimab bij gemetastaseerd pancreatisch adenocarcinoom: een gerandomiseerde fase 1-studie
Waarom deze studie ertoe doet
Pancreaskanker is een van de dodelijkste vormen van kanker, deels omdat het meestal pas wordt ontdekt nadat het zich heeft uitgezaaid en omdat standaardchemotherapie patiënten maar een beperkte extra tijd geeft. Deze studie onderzoekt een nieuwe geneesmiddelstrategie die niet alleen gericht is op het direct aanvallen van kankercellen, maar ook op het opheffen van een soort chemische “nevel” die het immuunsysteem belemmert. Door een gerichte therapie genaamd quemliclustat te combineren met routinematige chemotherapie, en soms met een immuunversterkend antilichaam, vragen de onderzoekers of zij veilig de overleving kunnen verlengen en de eigen afweer van het lichaam beter kunnen benutten.
Een chemisch schild rond de tumor
Pancreastumoren creëren een vijandige omgeving die het immuuncellen moeilijk maakt hun werk te doen. Wanneer chemotherapie kankercellen doodt, laten deze cellen een molecuul genaamd ATP vrijkomen in het omliggende weefsel. Een enzym op celoppervlakken, bekend als CD73, zet ATP snel om in adenosine, een stof die normaal helpt ontsteking te dempen en gezond weefsel te beschermen. In tumoren functioneren echter hoge adenosine‑niveaus als een chemisch schild: ze verminderen immuunaanvallen en laten kankercellen voortbestaan. Het nieuwe pilvormige middel quemliclustat blokkeert CD73, met als doel adenosine te verlagen en de tumoromgeving minder gastvrij voor kanker en aantrekkelijker voor immuuncellen te maken. 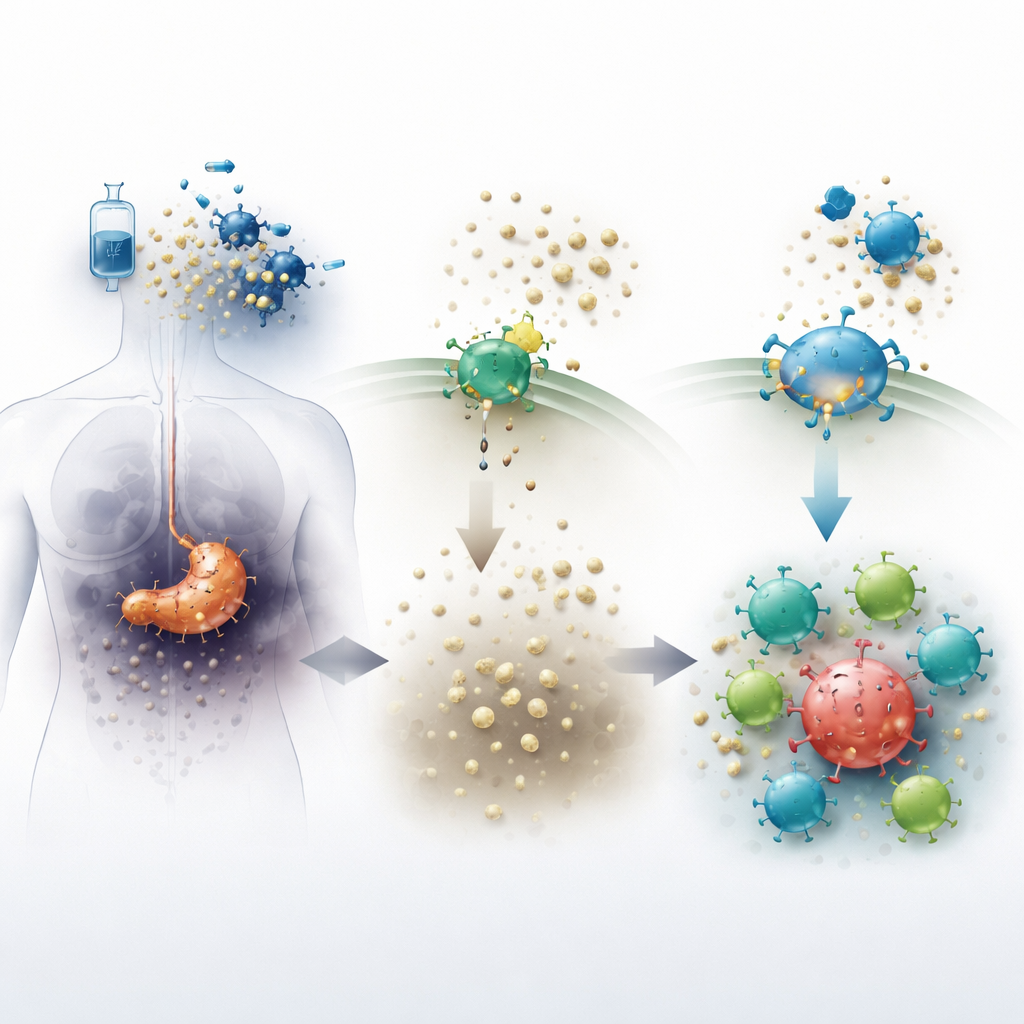
Een nieuwe combinatie testen bij patiënten
De ARC‑8‑trial schreef mensen in wiens pancreaskanker al was uitgezaaid en die nog geen behandeling voor gemetastaseerde ziekte hadden gekregen. Alle deelnemers kregen een standaard chemotherapieregie van gemcitabine en nab‑paclitaxel. In vroege dosisvondstgroepen kregen patiënten ook quemliclustat samen met een immuuncheckpoint‑antilichaam genaamd zimberelimab, dat moleculaire remmen op immuuncellen kan loslaten. Na het vaststellen van een veilige dosis quemliclustat breidde de studie uit naar grotere groepen waarin patiënten willekeurig werden toegewezen aan chemotherapie plus quemliclustat met of zonder zimberelimab. De belangrijkste doelen waren het beoordelen van veiligheid en het zoeken naar vroege aanwijzingen voor voordeel, zoals tumorkrimp en overleving.
Veiligheids- en overlevingssignalen
Over alle behandelingsarmen heen leken de bijwerkingen sterk op wat artsen verwachten van deze chemotherapieregie alleen, zoals vermoeidheid, misselijkheid en lage bloedwaarden. Ernstige immuungerelateerde complicaties kwamen weinig voor, en de meeste ernstige problemen waren gekoppeld aan chemotherapie in plaats van aan de nieuwe middelen. Toen de onderzoekers patiënten samenvoegden die de aanbevolen dosis quemliclustat ontvingen, vonden ze dat tumoren bij ongeveer een derde van de patiënten krimpten en bij ongeveer driekwart onder controle bleven. De mediane totale overleving bereikte in deze groep ongeveer 16 maanden, wat opvallend langer is dan de ongeveer 9 tot 12 maanden die in meerdere recente studies met alleen chemotherapie werden gezien. Een zorgvuldige vergelijking met een “synthetische” controlegroep opgebouwd uit eerdere onderzoeken suggereerde een overlevingsvoordeel van bijna zes maanden voor patiënten die de quemliclustat‑combinatie kregen.
Hoe het middel de tumorumgeving verandert
Om te begrijpen waarom sommige patiënten meer profiteerden dan anderen, bekeek het team genexpressiepatronen in tumorbiopten en in in het laboratorium gekweekte cellen. Ze concentreerden zich op een set genen die de NR4A‑familie heet, die oplichten wanneer adenosine‑niveaus hoog zijn. In kweekvaten verhoogde het toevoegen van adenosine of zijn voorlopers NR4A‑genen in meerdere celtypen die in pancreastumoren voorkomen, terwijl het blokkeren van CD73 of adenosinereceptoren dit signaal onderdrukte. In patiëntmonsters verhoogde chemotherapie zelf de NR4A‑activiteit in veel tumorgeassocieerde cellen, wat overeenkomt met een piek van adenosine na celschade. Opvallend was dat patiënten van wie de tumoren bij aanvang hogere NR4A‑waarden hadden, de neiging hadden langer te leven op quemliclustat‑therapie, maar dit patroon hield geen stand in twee externe studies waarin patiënten vergelijkbare chemotherapie ontvingen zonder quemliclustat. 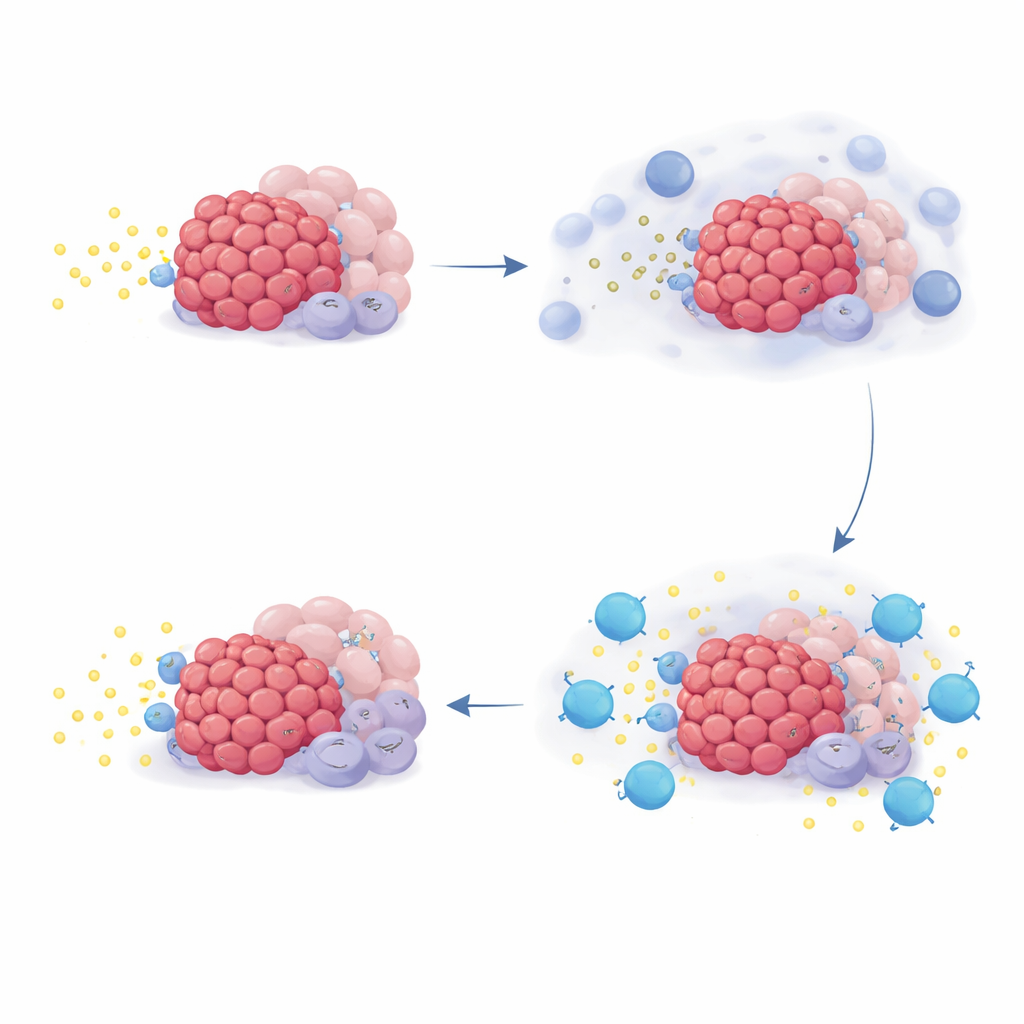
Immuuncellen terug in de strijd brengen
Geavanceerde beeldvorming van tumorplakjes liet zien dat gebieden met hoge NR4A‑waarden minder geactiveerde cytotoxische T‑cellen in de nabijheid hadden, wat suggereert dat adenosine een gradiënt creëert die deze cellen op afstand houdt. Bij patiënten van wie voor- en na‑behandelingsbiopten waren genomen, verlaagde quemliclustat doorgaans de NR4A‑signalen in tumoren. Degenen met de grootste daling vertoonden de sterkste toename in genmerken voor de aanwezigheid en activiteit van T‑cellen, en zij genoten ook de beste totale overleving, waarbij meer dan de helft nog steeds in leven was na meer dan twee jaar. Gezamenlijk ondersteunen deze bevindingen het idee dat blokkade van CD73 de adenosine‑“nevel” dunner maakt, waardoor immuuncellen dichter bij kankercellen kunnen komen en ze effectiever kunnen aanvallen.
Wat dit voor patiënten kan betekenen
Deze vroegefase‑trial was voornamelijk ontworpen om veiligheid te testen en mist een traditionele gerandomiseerde controlegroep met alleen chemotherapie, dus de resultaten kunnen nog niet bewijzen dat quemliclustat de levensduur verlengt. Desondanks leek de combinatie goed verdraagbaar en gaf ze overlevingstijden die gunstig vergelijken met eerdere studies. De biologische analyses koppelen medicijnblootstelling, veranderingen in tumorchemie en immuunactivatie aan patiëntuitkomsten, en versterken daarmee het argument dat het richten op adenosine een veelbelovende strategie is. Een grotere fase 3‑studie die nu loopt zal testen of het toevoegen van quemliclustat aan standaardchemotherapie daadwerkelijk de overleving verbetert voor mensen met gemetastaseerde pancreaskanker.
Bronvermelding: Wainberg, Z.A., Manji, G.A., Bahary, N. et al. Quemliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1 trial. Nat Med 32, 1267–1277 (2026). https://doi.org/10.1038/s41591-026-04283-z
Trefwoorden: pancreaskanker, tumormicro‑omgeving, immunotherapie, adenosine‑pad, klinische studie