Clear Sky Science · ar
كومليكلاستات والعلاج الكيميائي مع زمبرليماب أو بدونه في سرطانة البنكرياس الغدي النقيلي: تجربة عشوائية من المرحلة الأولى
لماذا تهمنا هذه الدراسة
يعد سرطان البنكرياس من أكثر السرطانات فتكًا، ويرجع ذلك جزئيًا إلى أنه غالبًا ما يُكتشف بعد انتشاره وأن العلاج الكيميائي القياسي يمنح المرضى وقتًا إضافيًا قصيرًا فقط. تختبر هذه الدراسة استراتيجية دوائية جديدة تهدف ليس فقط إلى مهاجمة خلايا الورم مباشرة، بل إلى رفع نوع من «الضباب» الكيميائي الذي يمنع الجهاز المناعي من المساعدة. من خلال اقتران دواء مستهدف يُدعى كومليكلاستات بالعلاج الكيميائي الروتيني، وأحيانًا مع جسم مضاد معزز للمناعة، يسأل الباحثون ما إذا كان بإمكانهم تمديد البقاء بأمان واستغلال دفاعات الجسم بشكل أفضل.
درع كيميائي حول الورم
تُنشئ أورام البنكرياس محيطًا قاسيًا يجعل من الصعب على الخلايا المناعية أداء وظيفتها. عندما يقتل العلاج الكيميائي الخلايا السرطانية، تُطلق جزيءً يُدعى ATP في النسيج المحيط. إن إنزيمًا على أسطح الخلايا، يُعرف باسم CD73، يحول ATP بسرعة إلى الأدينوزين، وهي مادة تساعد عادةً على تهدئة الالتهاب وحماية الأنسجة السليمة. داخل الأورام، مع ذلك، تعمل المستويات العالية من الأدينوزين كدرع كيميائي، مقلِّلةً من الهجوم المناعي ومسمحةً لخلايا السرطان بالاستمرار. يمنع الدواء الجديد الشبيه بالحبوب كومليكلاستات CD73، بهدف خفض الأدينوزين وجعل بيئة الورم أقل ترحيبًا بالسرطان وأكثر جذبًا للخلايا المناعية. 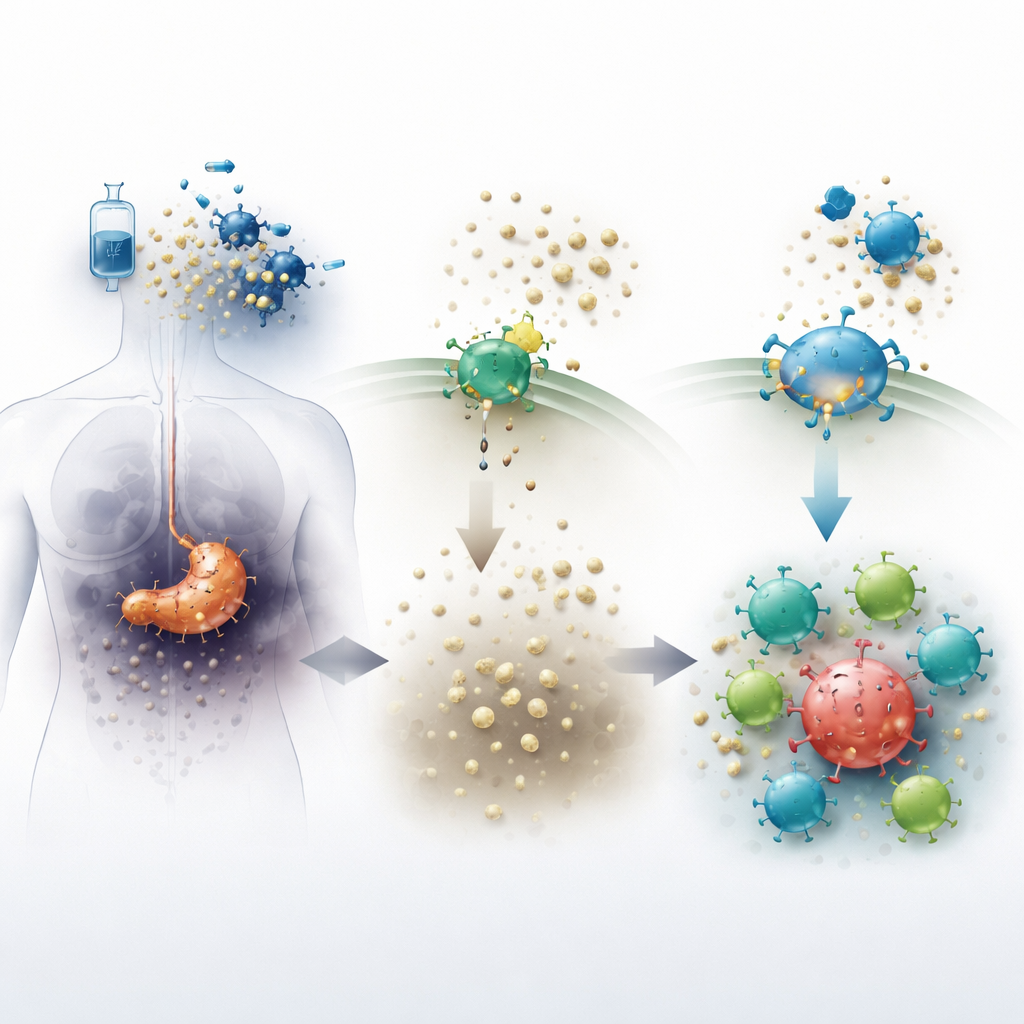
اختبار تركيبة جديدة على المرضى
سجلت تجربة ARC‑8 أشخاصًا كان قد انتشر لديهم سرطان البنكرياس ولم يتلقوا علاجًا بعد لمرضهم النقيلي. تلقى جميع المشاركين مزيجًا كيميائيًا قياسيًا من جيمسيتابين وناب‑باكليتاكسيل. في مجموعات تحديد الجرعات المبكرة، تلقى المرضى أيضًا كومليكلاستات مع جسم مضاد لمُعينات المناعة يُدعى زمبرليماب، والذي يمكنه تحرير المكابح الجزيئية على الخلايا المناعية. بعد تحديد جرعة آمنة من كومليكلاستات، توسعت الدراسة إلى مجموعات أكبر حيث تم توزيع المرضى عشوائيًا لتلقّي العلاج الكيميائي زائد كومليكلاستات إما مع زمبرليماب أو بدونه. كانت الأهداف الأساسية تقييم السلامة والبحث عن دلائل مبكرة على الفائدة، مثل تقلص الأورام والبقاء على قيد الحياة.
إشارات السلامة والبقاء
عبر جميع فروع العلاج، بدت الآثار الجانبية مشابهة جدًا لما يتوقعه الأطباء من هذا النظام الكيميائي وحده، مثل التعب والغثيان وقلة خلايا الدم. كانت المضاعفات المناعية الخطيرة غير شائعة، وكان معظم المشاكل الشديدة مرتبطة بالعلاج الكيميائي أكثر من ارتباطها بالأدوية الجديدة. عندما جمع الباحثون بيانات المرضى الذين تلقوا الجرعة الموصى بها من كومليكلاستات، وجدوا أن الأورام تقلصت لدى نحو ثلث المرضى وبقيت تحت السيطرة لدى حوالي ثلاثة أرباعهم. بلغ متوسط البقاء الكلي نحو 16 شهرًا في هذه المجموعة، وهو أطول بشكل ملحوظ من نحو 9 إلى 12 شهرًا التي لوحظت في عدة تجارب حديثة للعلاج الكيميائي وحده. وقد اقترح مقارنة دقيقة مع مجموعة ضابطة «اصطناعية» بُنيت من دراسات سابقة أفضلية في البقاء تقارب ستة أشهر للمرضى الذين تلقوا تركيبة كومليكلاستات.
فهم كيف يعيد الدواء تشكيل محيط الورم
لفهم سبب استفادة بعض المرضى أكثر من غيرهم، نظر الفريق في أنماط نشاط الجينات في خزعات الورم وفي خلايا مزروعة مخبريًا. ركزوا على مجموعة جينات تُدعى عائلة NR4A، التي تُنشط عندما تكون مستويات الأدينوزين مرتفعة. في الأطباق المختبرية، أدى إضافة الأدينوزين أو سلفاته إلى تعزيز جينات NR4A في أنواع خلوية متعددة توجد في أورام البنكرياس، بينما أبقى حجب CD73 أو مستقبلات الأدينوزين هذا الإشارة منخفضة. في عينات المرضى، زاد العلاج الكيميائي نفسه من نشاط NR4A في العديد من الخلايا المرتبطة بالورم، تماشيًا مع اندفاع الأدينوزين بعد تلف الخلايا. لافتًا أن المرضى الذين كانت أورامهم تحتوي في البداية على مستويات أعلى من NR4A مالوا إلى العيش لفترات أطول على علاج كومليكلاستات، لكن هذا النمط لم يُرَ في تجربتين خارجيتين حصل فيها المرضى على علاج كيميائي مشابه بدون كومليكلاستات. 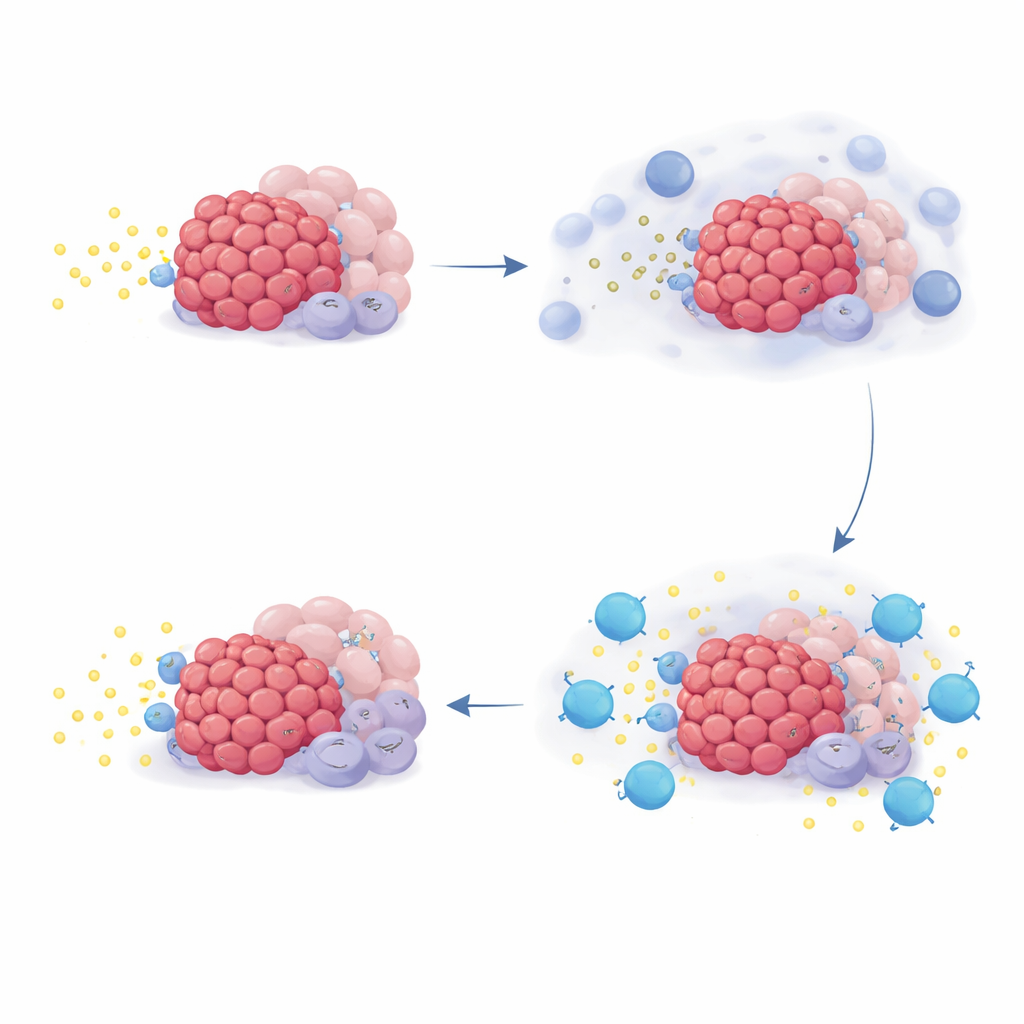
إعادة الخلايا المناعية إلى المعركة
أظهر تصوير متقدم لشرائح الأورام أن المناطق ذات مستويات NR4A العالية كانت تحتوي على عدد أقل من الخلايا التائية القاتلة المنشّطة في الجوار، مما يشير إلى أن الأدينوزين يخلق تدرجًا يبقي هذه الخلايا على مسافة. في المرضى الذين أُخذت منهم خزعات قبل وبعد العلاج، خفّض كومليكلاستات عمومًا إشارات NR4A في الأورام. وأولئك الذين شهدوا أكبر هبوط أظهروا أقوى ارتفاع في علامات الجينات ذات الصلة بوجود ونشاط الخلايا التائية، وتمتعوا أيضًا بأفضل بقاء كلي، حيث كان أكثر من النصف منهم على قيد الحياة بعد أكثر من عامين. تدعم هذه النتائج مجتمعة الفكرة القائلة بأن حجب CD73 يخفف «ضباب» الأدينوزين، مما يسمح للخلايا المناعية بالاقتراب من الخلايا السرطانية ومهاجمتها بشكل أكثر فعالية.
ماذا قد يعني هذا للمرضى
تم تصميم هذه التجربة المبكرة بالأساس لاختبار السلامة، وتفتقر إلى مجموعة ضابطة تقليدية عشوائية للعلاج الكيميائي فقط، لذا لا يمكن للنتائج حتى الآن أن تثبت أن كومليكلاستات يطيل الحياة. ومع ذلك، بدا أن التركيبة محتملة التحمل وأنتجت أوقات بقاء تقارن إيجابيًا بالدراسات السابقة. تربط التحليلات البيولوجية التعرض للعقار وتغيرات كيمياء الورم وتنشيط المناعة بنتائج المرضى، مما يعزز الحجة أن استهداف الأدينوزين استراتيجية واعدة. ستختبر تجربة أكبر من المرحلة الثالثة جارية الآن ما إذا كان إضافة كومليكلاستات إلى العلاج الكيميائي القياسي يحسّن بالفعل البقاء للأشخاص المصابين بسرطان البنكرياس النقيلي.
الاستشهاد: Wainberg, Z.A., Manji, G.A., Bahary, N. et al. Quemliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1 trial. Nat Med 32, 1267–1277 (2026). https://doi.org/10.1038/s41591-026-04283-z
الكلمات المفتاحية: سرطان البنكرياس, البيئة الدقيقة للورم, العلاج المناعي, مسار الأدينوزين, تجربة سريرية