Clear Sky Science · pt
Quemliclustato e quimioterapia com ou sem zimberelimabe em adenocarcinoma pancreático metastático: um ensaio de fase 1 randomizado
Por que este estudo importa
O câncer de pâncreas é um dos tumores mais letais, em parte porque costuma ser detectado depois de já ter se espalhado e porque a quimioterapia padrão oferece aos pacientes apenas um curto acréscimo de tempo. Este estudo testa uma nova estratégia medicamentosa que visa não apenas atacar as células tumorais diretamente, mas também dissipar uma espécie de “névoa” química que impede o sistema imune de atuar. Ao combinar um fármaco direcionado chamado quemliclustato com a quimioterapia habitual, e às vezes com um anticorpo que estimula a imunidade, os pesquisadores investigam se é possível prolongar a sobrevida de forma segura e aproveitar melhor as defesas do próprio corpo.
Um escudo químico ao redor do tumor
Os tumores pancreáticos criam um ambiente hostil que dificulta o trabalho das células imunes. Quando a quimioterapia mata células cancerosas, elas liberam uma molécula chamada ATP no tecido circundante. Uma enzima na superfície celular, conhecida como CD73, converte rapidamente o ATP em adenosina, uma substância que normalmente ajuda a acalmar a inflamação e proteger o tecido saudável. Dentro dos tumores, porém, níveis altos de adenosina funcionam como um escudo químico, atenuando o ataque imune e permitindo que as células cancerosas persistam. O novo comprimido quemliclustato bloqueia a CD73, com o objetivo de reduzir a adenosina e tornar o microambiente tumoral menos acolhedor ao câncer e mais receptivo às células imunes. 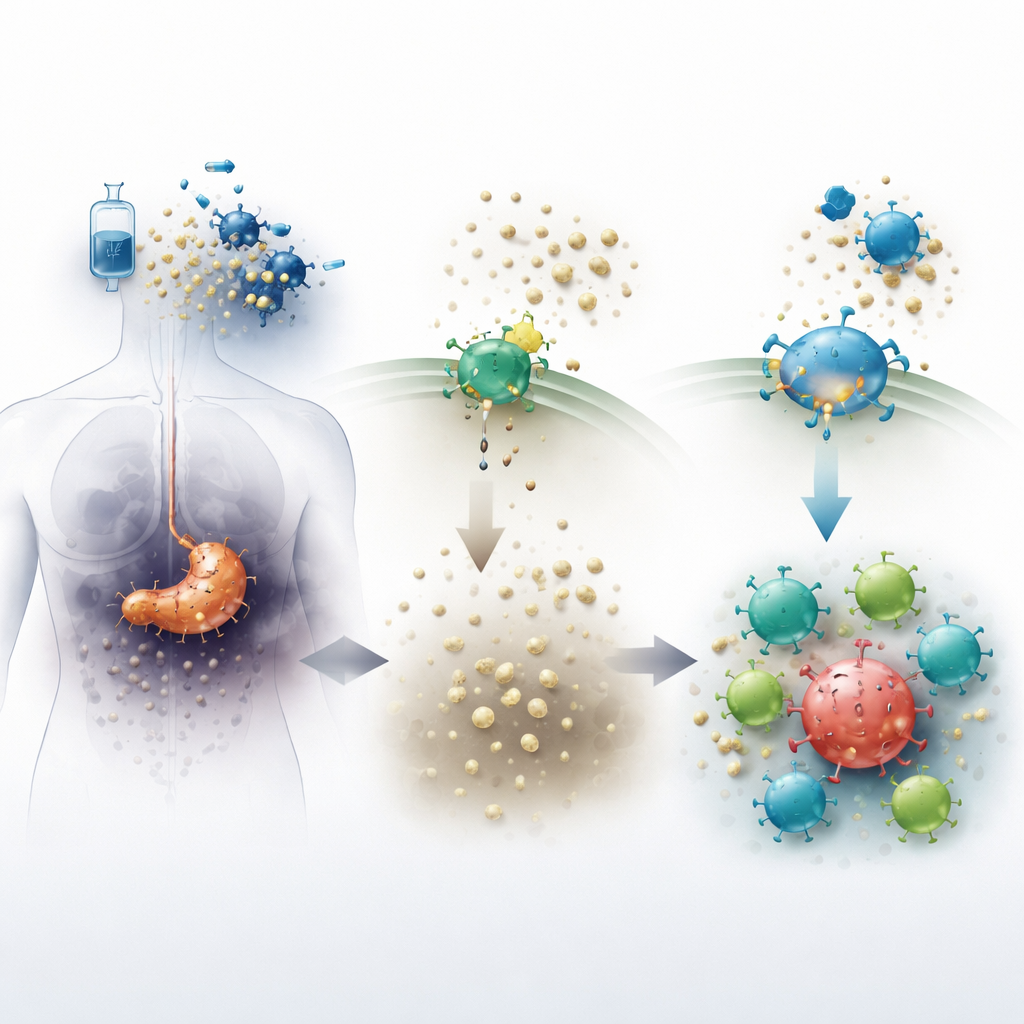
Testando uma nova combinação em pacientes
O ensaio ARC‑8 incluiu pessoas cujo câncer de pâncreas já havia se espalhado e que ainda não haviam recebido tratamento para doença metastática. Todos os participantes receberam a combinação quimioterápica padrão de gemcitabina e nab‑paclitaxel. Nos primeiros grupos de determinação de dose, os pacientes também receberam quemliclustato juntamente com um anticorpo de checkpoint imune chamado zimberelimabe, que pode liberar freios moleculares nas células imunes. Após estabelecer uma dose segura de quemliclustato, o estudo expandiu‑se para grupos maiores nos quais os pacientes foram randomizados a receber quimioterapia mais quemliclustato com ou sem zimberelimabe. Os objetivos principais foram avaliar a segurança e buscar sinais iniciais de benefício, como redução tumoral e sobrevida.
Sinais de segurança e sobrevida
Em todos os braços de tratamento, os efeitos colaterais foram muito semelhantes ao esperado com esse esquema quimioterápico isolado, como fadiga, náusea e contagens sanguíneas baixas. Complicações imunológicas graves foram incomuns, e os problemas mais severos estiveram na maior parte ligados à quimioterapia, não aos fármacos novos. Quando os pesquisadores agruparam pacientes que receberam a dose recomendada de quemliclustato, observaram que os tumores diminuíram em cerca de um terço dos pacientes e permaneceram controlados em aproximadamente três quartos. A mediana de sobrevida global alcançou cerca de 16 meses nesse grupo, notavelmente mais do que os aproximadamente 9 a 12 meses observados em vários ensaios recentes apenas com quimioterapia. Uma comparação cuidadosa com um grupo controle “sintético” construído a partir de estudos anteriores sugeriu uma vantagem de sobrevida de quase seis meses para pacientes que receberam a combinação com quemliclustato.
Entendendo como o fármaco remodela o microambiente tumoral
Para entender por que alguns pacientes se beneficiaram mais do que outros, a equipe analisou padrões de atividade gênica em biópsias tumorais e em células cultivadas em laboratório. Focaram em um conjunto de genes chamado família NR4A, que se ativam quando os níveis de adenosina são altos. Em culturas, a adição de adenosina ou de seus precursores aumentou a expressão dos genes NR4A em múltiplos tipos celulares presentes em tumores pancreáticos, enquanto o bloqueio da CD73 ou dos receptores de adenosina diminuiu esse sinal. Nas amostras de pacientes, a própria quimioterapia aumentou a atividade de NR4A em várias células associadas ao tumor, consistente com uma onda de adenosina após o dano celular. De forma notável, pacientes cujos tumores exibiam níveis iniciais mais altos de NR4A tenderam a viver mais com a terapia com quemliclustato, mas esse padrão não se observou em dois ensaios externos nos quais os pacientes receberam quimioterapia semelhante sem quemliclustato. 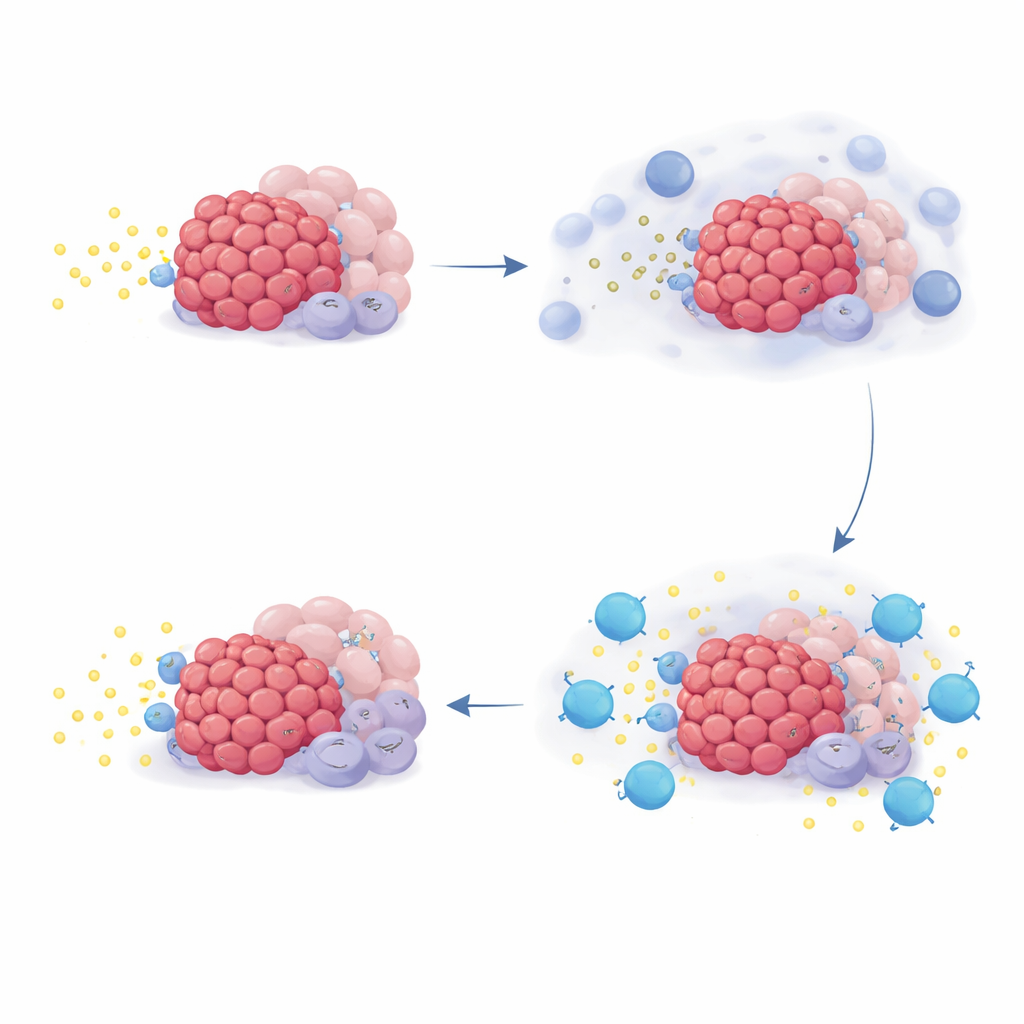
Trazer as células imunes de volta à luta
Imagens avançadas de cortes tumorais revelaram que áreas com altos níveis de NR4A tinham menos células T citotóxicas ativadas nas proximidades, sugerindo que a adenosina cria um gradiente que mantém essas células à distância. Em pacientes que tiveram biópsias antes e depois do tratamento, o quemliclustato geralmente reduziu os sinais de NR4A nos tumores. Aqueles com a maior queda apresentaram o maior aumento em marcadores genéticos de presença e atividade de células T, e também desfrutaram da melhor sobrevida global, com mais da metade ainda viva além de dois anos. Em conjunto, essas descobertas apoiam a ideia de que bloquear a CD73 afina a “névoa” de adenosina, permitindo que as células imunes se aproximem das células cancerosas e as ataquem com maior eficácia.
O que isso pode significar para os pacientes
Este ensaio de fase inicial foi concebido principalmente para testar segurança, e carece de um grupo controle tradicional randomizado com apenas quimioterapia, de modo que os resultados ainda não podem provar que o quemliclustato prolonga a vida. Ainda assim, a combinação mostrou‑se tolerável e produziu tempos de sobrevida que se comparam favoravelmente com estudos anteriores. As análises biológicas conectam a exposição ao fármaco, alterações na química tumoral e ativação imune aos desfechos dos pacientes, fortalecendo o argumento de que mirar na adenosina é uma estratégia promissora. Um ensaio de fase 3 maior, agora em andamento, testará se adicionar quemliclustato à quimioterapia padrão realmente melhora a sobrevida de pessoas com câncer pancreático metastático.
Citação: Wainberg, Z.A., Manji, G.A., Bahary, N. et al. Quemliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1 trial. Nat Med 32, 1267–1277 (2026). https://doi.org/10.1038/s41591-026-04283-z
Palavras-chave: câncer de pâncreas, microambiente tumoral, imunoterapia, via da adenosina, ensaio clínico