Clear Sky Science · pl
Quemliclustat i chemioterapia z lub bez zimberelimabu w przerzutowym gruczolakoraku trzustki: randomizowane badanie fazy 1
Dlaczego to badanie ma znaczenie
Rak trzustki jest jednym z najbardziej śmiertelnych nowotworów, częściowo dlatego, że zwykle wykrywany jest po rozprzestrzenieniu się, a standardowa chemioterapia daje pacjentom tylko niewielkie wydłużenie czasu życia. To badanie sprawdza nowe podejście lekowe, które ma na celu nie tylko bezpośrednie atakowanie komórek nowotworowych, lecz także rozwianie swego rodzaju chemicznej „mgły”, która uniemożliwia układowi odpornościowemu pomoc. Łącząc celowaną terapię o nazwie quemliclustat ze standardową chemioterapią, a w niektórych przypadkach także z przeciwciałem pobudzającym odporność, badacze pytają, czy można bezpiecznie wydłużyć przeżycie i lepiej wykorzystać naturalne mechanizmy obronne organizmu.
Chemiczna tarcza wokół guza
Guzy trzustki tworzą surowe otoczenie, które utrudnia pracę komórek odpornościowych. Gdy chemioterapia zabija komórki nowotworowe, uwalniają one do otaczających tkanek cząsteczkę zwaną ATP. Enzym obecny na powierzchni komórek, znany jako CD73, szybko przekształca ATP w adenozynę — substancję, która zwykle pomaga tłumić stan zapalny i chronić zdrowe tkanki. W obrębie guzów jednak wysokie poziomy adenozyny działają jak chemiczna tarcza, osłabiając atak odpornościowy i pozwalając komórkom nowotworowym przetrwać. Nowy doustny lek quemliclustat blokuje CD73, dążąc do obniżenia poziomu adenozyny i uczynienia mikrośrodowiska guza mniej przyjaznym dla raka, a bardziej sprzyjającym komórkom odpornościowym. 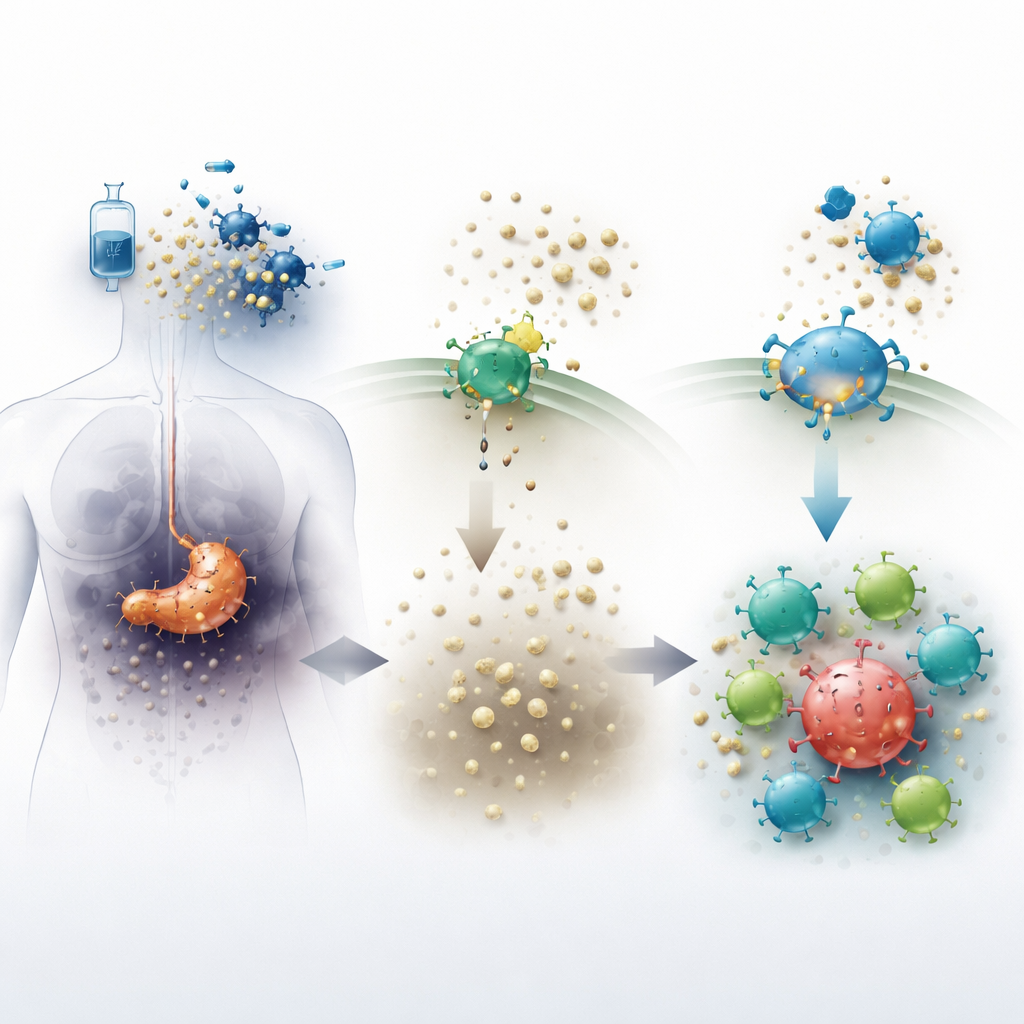
Testowanie nowego połączenia u pacjentów
W badaniu ARC‑8 zrekrutowano osoby z przerzutowym rakiem trzustki, które nie otrzymywały jeszcze leczenia choroby przerzutowej. Wszyscy uczestnicy otrzymywali standardowy schemat chemioterapii z gemcytabiną i nab‑paklitakselem. W początkowych kohortach ustalających dawkę pacjenci otrzymywali także quemliclustat razem z przeciwciałem hamującym punkt kontrolny immunologiczny o nazwie zimberelimab, które może zwalniać molekularne hamulce na komórkach odpornościowych. Po ustaleniu bezpiecznej dawki quemliclustatu badanie rozszerzono do większych grup, w których pacjenci byli losowo przydzielani do chemioterapii z quemliclustatem z lub bez zimberelimabu. Główne cele obejmowały ocenę bezpieczeństwa oraz poszukiwanie wczesnych sygnałów korzyści, takich jak zmniejszenie guza i przeżycie.
Sygnały bezpieczeństwa i przeżycia
We wszystkich ramionach leczenia działania niepożądane były zbliżone do tych, których lekarze spodziewają się po samym schemacie chemioterapii, takich jak zmęczenie, nudności i obniżenie liczby krwinek. Ciężkie powikłania związane z układem odpornościowym były rzadkie, a większość poważnych problemów wiązała się z chemioterapią, a nie z nowymi lekami. Po zgrupowaniu pacjentów, którzy otrzymali zalecaną dawkę quemliclustatu, stwierdzono, że guzy zmniejszyły się u około jednej trzeciej chorych, a pozostawały pod kontrolą u około trzech czwartych. Mediana całkowitego przeżycia w tej grupie wyniosła około 16 miesięcy, co jest istotnie dłużej niż około 9–12 miesięcy obserwowanych w kilku niedawnych badaniach chemioterapii stosowanej samodzielnie. Staranna analiza porównawcza z „syntetyczną” grupą kontrolną zbudowaną na podstawie wcześniejszych badań zasugerowała korzyść w przeżyciu sięgającą prawie sześciu miesięcy dla pacjentów otrzymujących kombinację z quemliclustatem.
Jak lek zmienia mikrośrodowisko guza
Aby zrozumieć, dlaczego niektórzy pacjenci odnosili większe korzyści niż inni, zespół przeanalizował wzorce aktywności genów w wycinkach guza i w komórkach hodowanych w laboratorium. Skoncentrowano się na zestawie genów z rodziny NR4A, które uaktywniają się przy wysokim poziomie adenozyny. W hodowlach dodanie adenozyny lub jej prekursorów zwiększało ekspresję genów NR4A w wielu typach komórek występujących w guzach trzustki, podczas gdy blokada CD73 lub receptorów adenozyny hamowała ten sygnał. W próbkach pacjentów sama chemioterapia zwiększała aktywność NR4A w wielu komórkach związanych z guzem, co jest zgodne z wyrzutem adenozyny po uszkodzeniu komórek. Uderzająco, pacjenci, których guzy początkowo wykazywały wyższe poziomy NR4A, mieli skłonność do dłuższego przeżycia podczas terapii quemliclustatem, ale ten wzorzec nie utrzymywał się w dwóch zewnętrznych badaniach, w których pacjenci otrzymywali podobną chemioterapię bez quemliclustatu. 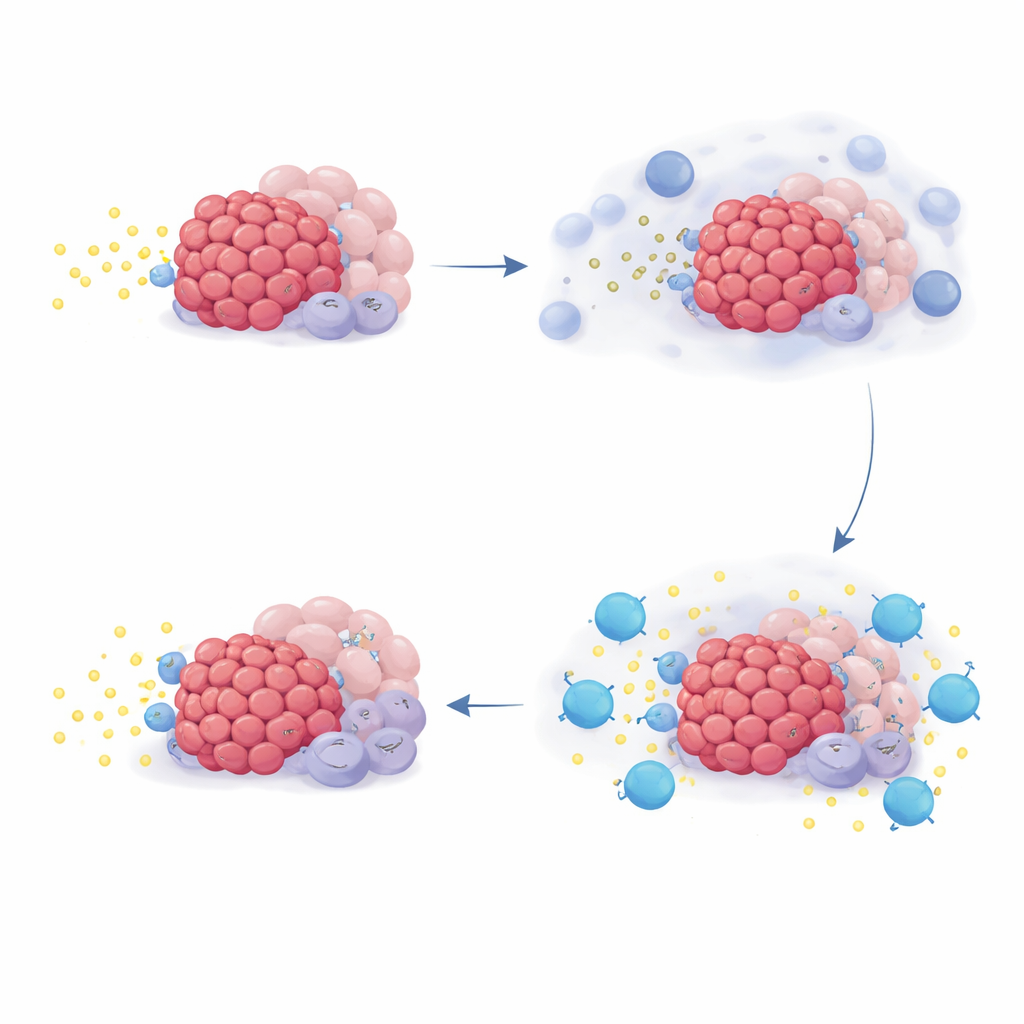
Przywracanie komórek odpornościowych do walki
Zaawansowane obrazowanie wycinków guza wykazało, że obszary o wysokim poziomie NR4A miały mniej aktywowanych cytotoksycznych limfocytów T w pobliżu, co sugeruje, że adenozyna tworzy gradient, który trzyma te komórki w dystansie. U pacjentów, u których pobrano wycinki przed i po leczeniu, quemliclustat generalnie obniżał sygnały NR4A w guzach. Ci, którzy doświadczyli największego spadku, wykazywali najsilniejszy wzrost markerów genowych obecności i aktywności limfocytów T, a także osiągali najlepsze przeżycie ogólne, z ponad połową pacjentów żyjących dłużej niż dwa lata. Wszystkie te obserwacje wspierają ideę, że blokada CD73 rozrzedza adenozynową „mgłę”, umożliwiając komórkom odpornościowym zbliżenie się do komórek nowotworowych i skuteczniejszy ich atak.
Co to może oznaczać dla pacjentów
To wczesnofazowe badanie miało przede wszystkim na celu ocenę bezpieczeństwa i nie zawiera tradycyjnej, randomizowanej grupy kontrolnej leczonej jedynie chemioterapią, dlatego wyniki nie mogą jeszcze dowieść, że quemliclustat wydłuża życie. Mimo to skojarzenie okazało się tolerowane i dało czasy przeżycia, które wypadają korzystnie w porównaniu z wcześniejszymi badaniami. Analizy biologiczne powiązały ekspozycję na lek, zmiany w chemii guza i aktywację układu odpornościowego z wynikami pacjentów, co wzmacnia argument, że celowanie w adenozynę jest obiecującą strategią. Trwające obecnie większe badanie fazy 3 sprawdzi, czy dodanie quemliclustatu do standardowej chemioterapii rzeczywiście poprawia przeżycie osób z przerzutowym rakiem trzustki.
Cytowanie: Wainberg, Z.A., Manji, G.A., Bahary, N. et al. Quemliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1 trial. Nat Med 32, 1267–1277 (2026). https://doi.org/10.1038/s41591-026-04283-z
Słowa kluczowe: rak trzustki, mikrośrodowisko guza, immunoterapia, szlak adenozynowy, badanie kliniczne