Clear Sky Science · de
Quemliclustat und Chemotherapie mit oder ohne Zimberelimab beim metastasierten Pankreasadenokarzinom: eine randomisierte Phase‑1‑Studie
Warum diese Studie wichtig ist
Pankreaskrebs gehört zu den tödlichsten Krebsarten, teilweise weil er meist erst entdeckt wird, nachdem er bereits gestreut hat, und weil die Standardchemotherapie den Patienten nur eine begrenzte zusätzliche Zeit verschafft. Diese Studie prüft eine neue Wirkstrategie, die nicht nur tumoröses Gewebe direkt angreift, sondern auch eine Art chemischen „Nebel“ beseitigen soll, der das Immunsystem am Helfen hindert. Indem das gezielte Mittel Quemliclustat mit üblicher Chemotherapie kombiniert und gelegentlich eine immunstimulierende Antikörpertherapie hinzugefügt wird, fragen die Forschenden, ob sich dadurch das Überleben sicher verlängern und die körpereigene Abwehr besser nutzen lässt.
Ein chemischer Schutzschild um den Tumor
Pankreastumoren schaffen ein feindliches Umfeld, das es Immunzellen schwer macht, ihre Aufgabe zu erfüllen. Wenn Chemotherapie Krebszellen zerstört, setzen diese ein Molekül namens ATP in das umliegende Gewebe frei. Ein Enzym auf Zelloberflächen, bekannt als CD73, wandelt ATP rasch in Adenosin um, einen Stoff, der normalerweise Entzündungen dämpft und gesundes Gewebe schützt. Innerhalb von Tumoren wirken hohe Adenosinspiegel jedoch wie ein chemischer Schutzschild: Sie dämpfen die Immunantwort und erlauben Krebszellen, zu überdauern. Das neue Tablettenpräparat Quemliclustat blockiert CD73, mit dem Ziel, Adenosin zu senken und die Tumorumgebung weniger einladend für Krebs, aber einladender für Immunzellen zu machen. 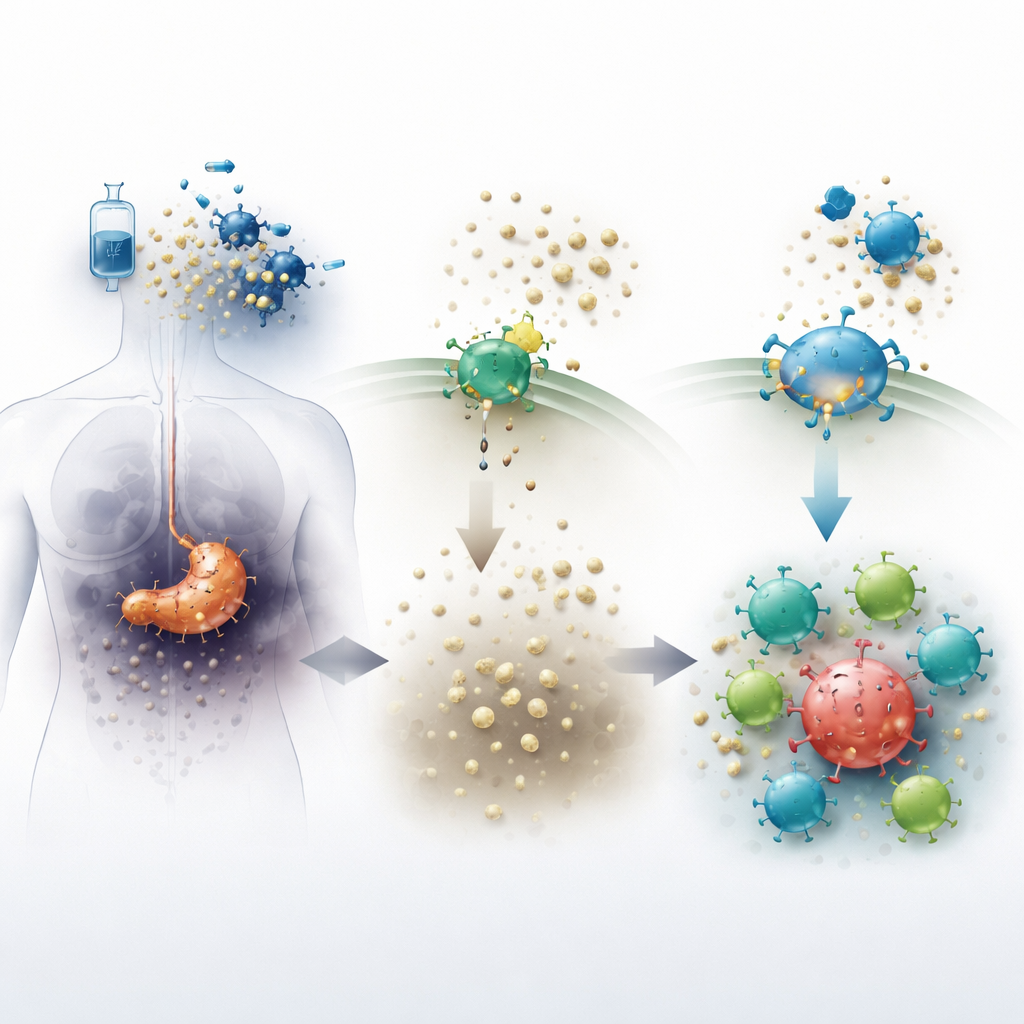
Prüfung einer neuen Kombination bei Patienten
Die ARC‑8‑Studie rekrutierte Personen, deren Pankreaskrebs bereits metastasiert war und die noch keine Behandlung der metastatischen Erkrankung erhalten hatten. Alle Teilnehmenden erhielten eine Standardchemotherapie aus Gemcitabin und nab‑Paclitaxel. In frühen Dosisfindungsgruppen bekamen Patienten zusätzlich Quemliclustat zusammen mit einem Immuncheck‑Point‑Antikörper namens Zimberelimab, der molekulare Bremssysteme auf Immunzellen lösen kann. Nach Festlegung einer sicheren Quemliclustat‑Dosis weitete die Studie die Gruppen aus, in denen Patienten randomisiert zugeteilt wurden, Chemotherapie plus Quemliclustat entweder mit oder ohne Zimberelimab zu erhalten. Die Hauptziele waren die Bewertung der Sicherheit und das Auffinden erster Hinweise auf einen Nutzen, etwa Tumorschrumpfung und Überleben.
Sicherheits‑ und Überlebenssignale
Über alle Behandlungsarme hinweg ähnelten die Nebenwirkungen weitgehend denen, die Ärzte von dieser Chemotherapieregime allein erwarten, wie Müdigkeit, Übelkeit und niedrige Blutwerte. Ernsthafte immunvermittelte Komplikationen waren selten, und die meisten schweren Probleme standen eher mit der Chemotherapie als mit den neuen Substanzen in Zusammenhang. Wenn die Forschenden die Patienten zusammenfassten, die die empfohlene Quemliclustat‑Dosis erhielten, zeigte sich, dass die Tumoren bei etwa einem Drittel der Patienten schrumpften und bei rund drei Vierteln unter Kontrolle blieben. Das mediane Gesamtüberleben lag in dieser Gruppe bei etwa 16 Monaten, deutlich länger als die etwa 9 bis 12 Monate, die in mehreren jüngeren Studien mit alleiniger Chemotherapie berichtet wurden. Ein vorsichtiger Vergleich mit einer aus früheren Studien gebildeten „synthetischen“ Kontrollgruppe deutete auf einen Überlebensvorteil von fast sechs Monaten für Patienten in der Quemliclustat‑Kombination hin.
Aufklärung, wie das Medikament die Tumorumgebung umgestaltet
Um zu verstehen, warum einige Patienten mehr profitierten als andere, untersuchte das Team Genaktivitätsmuster in Tumorbiopsien und in im Labor gezüchteten Zellen. Sie konzentrierten sich auf eine Genfamilie namens NR4A, die bei hohen Adenosinspiegeln besonders aktiv wird. Im Reagenzglas steigerten Zugaben von Adenosin oder dessen Vorstufen die NR4A‑Expression in mehreren Zelltypen, die in Pankreastumoren vorkommen, während die Blockade von CD73 oder Adenosinrezeptoren dieses Signal dämpfte. In Patientproben erhöhte die Chemotherapie selbst die NR4A‑Aktivität in vielen tumorassoziierten Zellen, was zu einer Adenosinwelle nach Zellschädigung passt. Auffallend war, dass Patienten, deren Tumoren zu Beginn höhere NR4A‑Spiegel aufwiesen, tendenziell länger unter Quemliclustat lebten, ein Muster, das in zwei externen Studien mit ähnlicher Chemotherapie ohne Quemliclustat nicht zu sehen war. 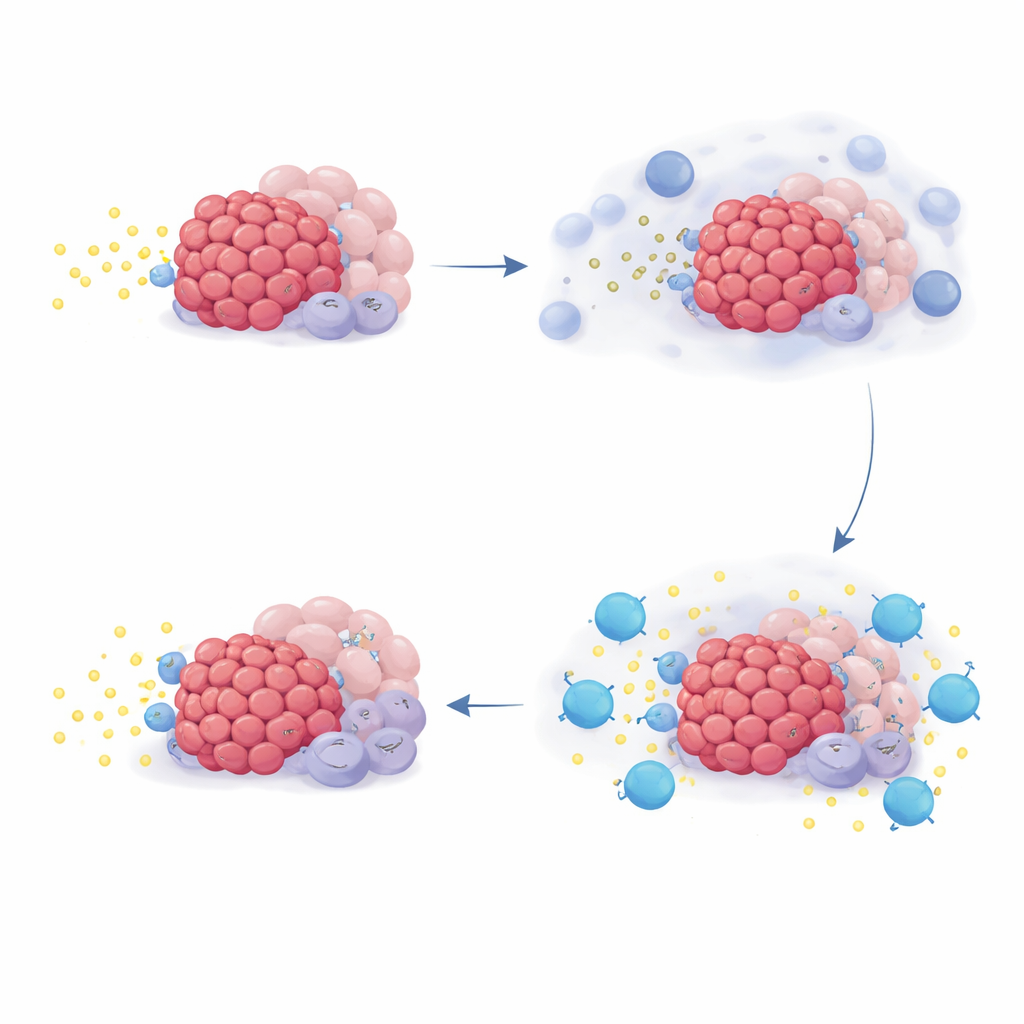
Rückführung von Immunzellen in den Kampf
Fortgeschrittene Bildgebung von Tumorschnitten zeigte, dass Bereiche mit hohen NR4A‑Werten weniger aktivierte Killer‑T‑Zellen in der Nähe hatten, was darauf hindeutet, dass Adenosin einen Gradient erzeugt, der diese Zellen fernhält. Bei Patienten, von denen vor und nach der Behandlung Biopsien entnommen wurden, senkte Quemliclustat allgemein die NR4A‑Signale in den Tumoren. Diejenigen mit dem stärksten Rückgang zeigten die stärkste Zunahme von Genmarkern für Anwesenheit und Aktivität von T‑Zellen, und sie hatten auch das beste Gesamtüberleben, wobei mehr als die Hälfte noch nach zwei Jahren lebte. Zusammen stützen diese Befunde die Idee, dass die Blockade von CD73 den Adenosin‑„Nebel“ lichtet, sodass Immunzellen näher an Krebszellen heranrücken und diese effektiver angreifen können.
Was das für Patienten bedeuten könnte
Diese Frühphasenstudie war vorwiegend auf Sicherheitsfragen ausgelegt und enthält keine traditionelle randomisierte Kontrollgruppe mit ausschließlich Chemotherapie, daher kann sie noch nicht beweisen, dass Quemliclustat das Leben verlängert. Dennoch wirkte die Kombination tolerierbar und ergab Überlebenszeiten, die im Vergleich zu früheren Studien vorteilhaft erscheinen. Die biologischen Analysen verknüpfen Medikamentenexposition, Veränderungen der Tumorchemie und Immunaktivierung mit den Patientenergebnissen und untermauern damit die These, dass die Zielsetzung des Adenosins ein vielversprechender Ansatz ist. Eine größere Phase‑3‑Studie, die derzeit läuft, wird prüfen, ob die Hinzufügung von Quemliclustat zur Standardchemotherapie das Überleben von Menschen mit metastasiertem Pankreaskrebs tatsächlich verbessert.
Zitation: Wainberg, Z.A., Manji, G.A., Bahary, N. et al. Quemliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1 trial. Nat Med 32, 1267–1277 (2026). https://doi.org/10.1038/s41591-026-04283-z
Schlüsselwörter: Pankreaskrebs, Tumormikroumgebung, Immuntherapie, Adenosin‑Signalweg, klinische Studie