Clear Sky Science · fr
Quemliclustat et chimiothérapie avec ou sans zimberelimab dans l’adénocarcinome pancréatique métastatique : un essai de phase 1 randomisé
Pourquoi cette étude est importante
Le cancer du pancréas est l’un des plus mortels, en partie parce qu’il est généralement détecté après diffusion et parce que la chimiothérapie standard n’offre aux patients qu’un gain de temps limité. Cette étude évalue une nouvelle stratégie médicamenteuse qui vise non seulement à attaquer directement les cellules tumorales, mais aussi à dissiper une sorte de « brume » chimique qui empêche le système immunitaire d’intervenir. En associant un médicament ciblé appelé quemliclustat à la chimiothérapie habituelle, et parfois à un anticorps stimulant l’immunité, les chercheurs se demandent s’ils peuvent prolonger la survie en toute sécurité et mieux mobiliser les défenses naturelles de l’organisme.
Un bouclier chimique autour de la tumeur
Les tumeurs pancréatiques créent un environnement hostile qui rend difficile le travail des cellules immunitaires. Quand la chimiothérapie tue les cellules cancéreuses, celles‑ci libèrent une molécule nommée ATP dans les tissus environnants. Une enzyme à la surface des cellules, appelée CD73, convertit rapidement l’ATP en adénosine, une substance qui aide normalement à calmer l’inflammation et à protéger les tissus sains. Dans les tumeurs, toutefois, des niveaux élevés d’adénosine agissent comme un bouclier chimique, atténuant l’attaque immunitaire et permettant aux cellules cancéreuses de persister. Le nouveau médicament oral quemliclustat bloque CD73, visant à réduire l’adénosine et à rendre l’environnement tumoral moins accueillant pour le cancer et plus propice aux cellules immunitaires. 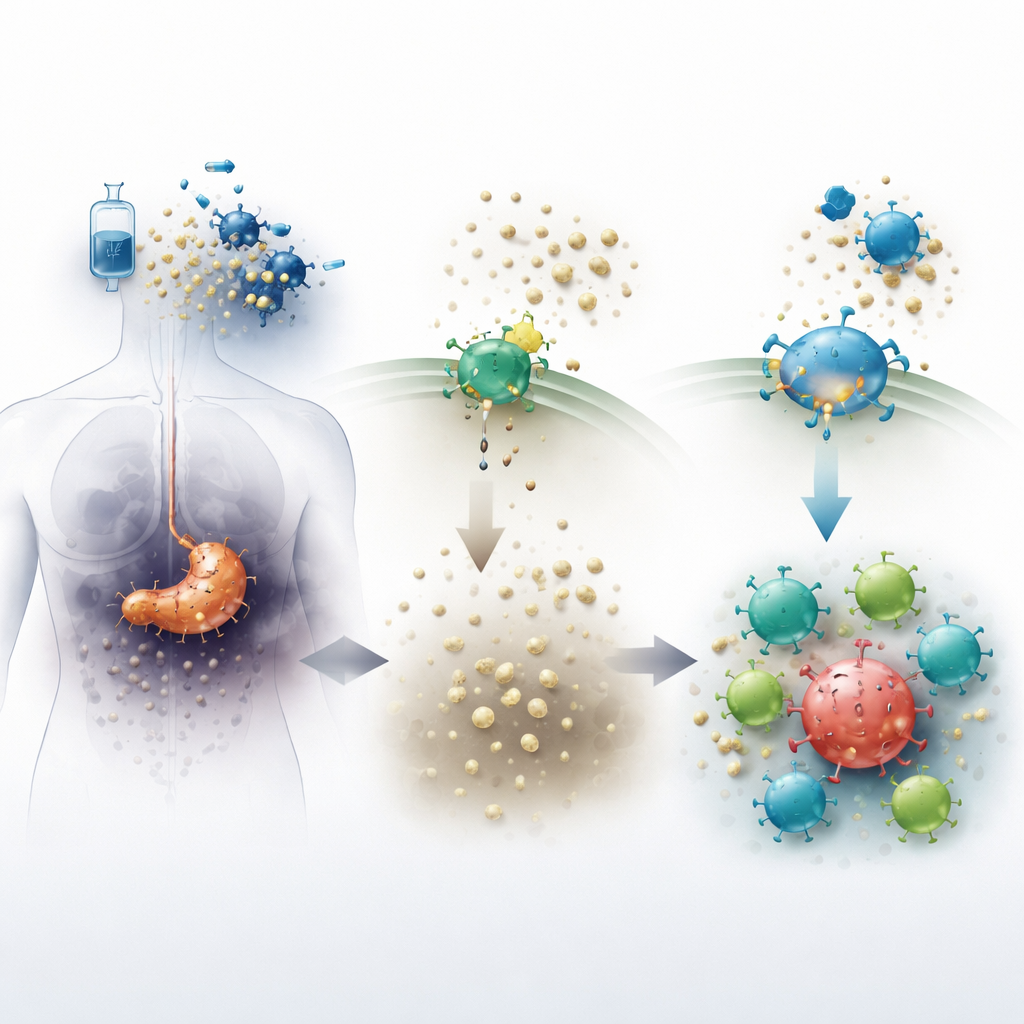
Tester une nouvelle combinaison chez des patients
L’essai ARC‑8 a recruté des personnes dont le cancer du pancréas s’était déjà étendu et qui n’avaient pas encore reçu de traitement pour la maladie métastatique. Tous les participants ont reçu une chimiothérapie standard à base de gemcitabine et nab‑paclitaxel. Dans les premiers groupes d’ajustement de dose, les patients ont également reçu quemliclustat avec un anticorps inhibiteur de point de contrôle immunitaire nommé zimberelimab, capable de relâcher certaines freins moléculaires des cellules immunitaires. Après avoir établi une dose sûre de quemliclustat, l’étude s’est élargie en groupes plus importants où les patients étaient assignés aléatoirement à recevoir la chimiothérapie plus quemliclustat soit avec, soit sans zimberelimab. Les objectifs principaux étaient d’évaluer la sécurité et de rechercher des signes précoces d’efficacité, comme la réduction tumorale et la survie.
Signaux de sécurité et de survie
Sur l’ensemble des bras de traitement, les effets secondaires étaient très similaires à ce que les médecins attendent de ce schéma de chimiothérapie seul, tels que fatigue, nausées et diminution des cellules sanguines. Les complications sévères liées à l’immunité étaient peu fréquentes, et la plupart des problèmes graves étaient associés à la chimiothérapie plutôt qu’aux nouveaux médicaments. Lorsque les chercheurs ont regroupé les patients ayant reçu la dose recommandée de quemliclustat, ils ont observé une réduction tumorale chez environ un tiers des patients et un contrôle de la maladie chez près des trois quarts. La survie globale médiane a atteint environ 16 mois dans ce groupe, nettement plus longue que les ~9 à 12 mois observés dans plusieurs essais récents de chimiothérapie seule. Une comparaison prudente avec un groupe témoin « synthétique » constitué à partir d’études antérieures a suggéré un avantage de survie d’environ six mois pour les patients recevant la combinaison incluant quemliclustat.
Comprendre comment le médicament remodèle le voisinage tumoral
Pour expliquer pourquoi certains patients ont mieux répondu que d’autres, l’équipe a étudié les profils d’expression génique dans des biopsies tumorales et des cellules cultivées en laboratoire. Ils se sont concentrés sur un ensemble de gènes appelé famille NR4A, qui s’exprime lorsque les niveaux d’adénosine sont élevés. En culture, l’ajout d’adénosine ou de ses précurseurs augmentait l’expression des gènes NR4A dans plusieurs types cellulaires présents dans les tumeurs pancréatiques, tandis que le blocage de CD73 ou des récepteurs de l’adénosine limitait ce signal. Dans les échantillons de patients, la chimiothérapie elle‑même augmentait l’activité des NR4A dans de nombreuses cellules associées à la tumeur, cohérent avec un pic d’adénosine après la destruction cellulaire. De façon notable, les patients dont les tumeurs présentaient des niveaux initiaux plus élevés de NR4A avaient tendance à vivre plus longtemps sous Quemliclustat, mais ce schéma n’a pas été observé dans deux essais externes où les patients recevaient une chimiothérapie similaire sans quemliclustat. 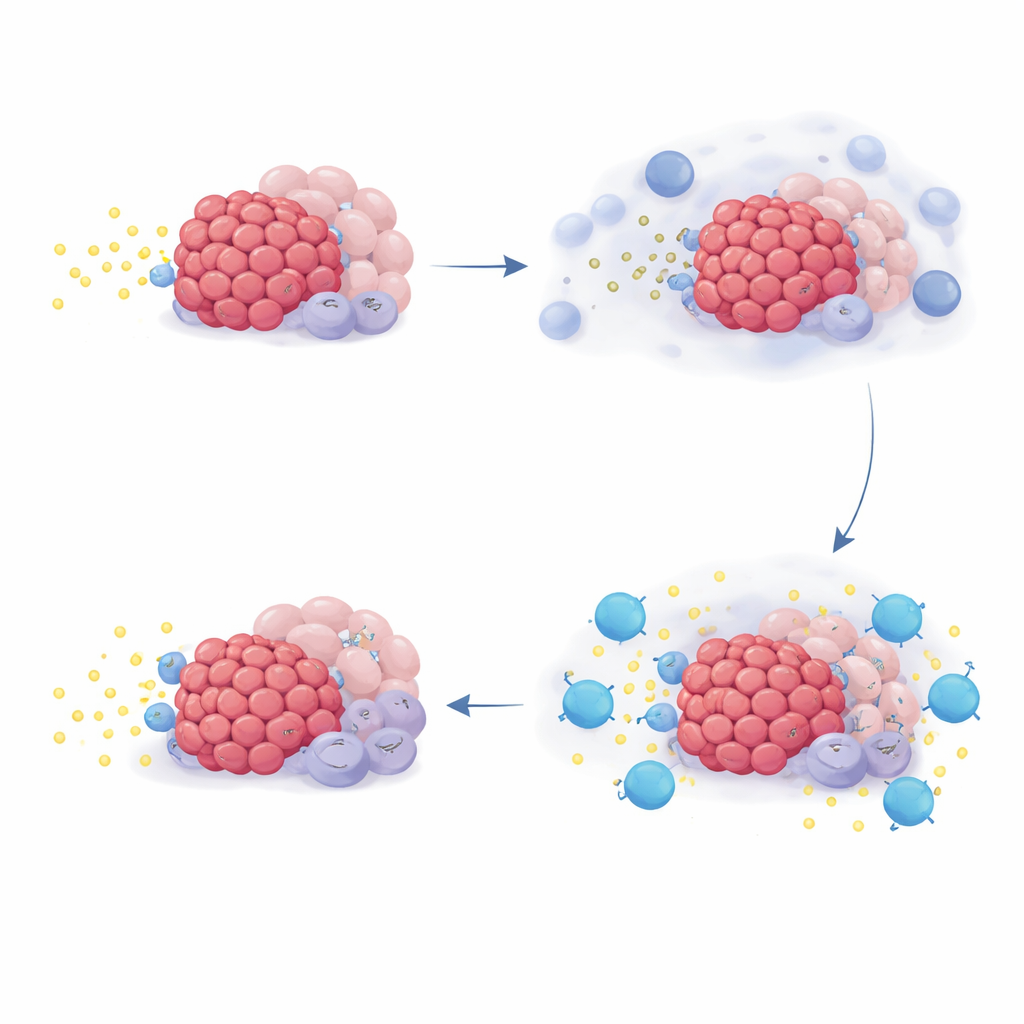
Ramener les cellules immunitaires dans la lutte
Des imageries avancées de coupes tumorales ont montré que les zones à forte expression de NR4A comportaient moins de lymphocytes T cytotoxiques activés à proximité, suggérant que l’adénosine crée un gradient qui maintient ces cellules à distance. Chez les patients ayant bénéficié de biopsies avant et après traitement, quemliclustat réduisait généralement les signaux NR4A dans les tumeurs. Ceux présentant la plus forte diminution montraient la plus grande augmentation des marqueurs géniques de présence et d’activité des cellules T, et bénéficiaient également de la meilleure survie globale, plus de la moitié restant vivants au‑delà de deux ans. Ensemble, ces résultats soutiennent l’idée que bloquer CD73 dissipe la « brume » d’adénosine, permettant aux cellules immunitaires de se rapprocher des cellules cancéreuses et de les attaquer plus efficacement.
Ce que cela pourrait signifier pour les patients
Cet essai de phase précoce visait principalement à tester la sécurité, et il ne comporte pas de groupe témoin traditionnel randomisé traité par chimiothérapie seule, aussi les résultats ne peuvent‑ils pas encore prouver que quemliclustat prolonge la vie. Néanmoins, la combinaison semblait tolérable et a produit des durées de survie comparables favorablement aux études antérieures. Les analyses biologiques relient l’exposition au médicament, les changements de la chimie tumorale et l’activation immunitaire aux résultats des patients, renforçant l’hypothèse que cibler l’adénosine est une stratégie prometteuse. Un essai de phase 3 plus vaste en cours testera désormais si l’ajout de quemliclustat à la chimiothérapie standard améliore réellement la survie des personnes atteintes d’un cancer du pancréas métastatique.
Citation: Wainberg, Z.A., Manji, G.A., Bahary, N. et al. Quemliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1 trial. Nat Med 32, 1267–1277 (2026). https://doi.org/10.1038/s41591-026-04283-z
Mots-clés: cancer du pancréas, microenvironnement tumoral, immunothérapie, voie de l’adénosine, essai clinique