Clear Sky Science · es
Quemliclustat y quimioterapia con o sin zimberelimab en adenocarcinoma pancreático metastásico: un ensayo aleatorizado de fase 1
Por qué importa este estudio
El cáncer de páncreas es uno de los más letales, en parte porque suele encontrarse cuando ya se ha diseminado y porque la quimioterapia estándar solo concede a los pacientes una pequeña cantidad de tiempo adicional. Este estudio prueba una estrategia farmacológica nueva que busca no solo atacar directamente las células tumorales, sino también disipar una especie de “niebla” química que impide que el sistema inmunitario ayude. Al combinar un fármaco dirigido llamado quemliclustat con la quimioterapia habitual, y en ocasiones con un anticuerpo que potencia la inmunidad, los investigadores preguntan si pueden prolongar la supervivencia de forma segura y aprovechar mejor las defensas propias del cuerpo.
Un escudo químico alrededor del tumor
Los tumores pancreáticos crean un entorno hostil que dificulta la función de las células inmunitarias. Cuando la quimioterapia mata células cancerosas, estas liberan una molécula llamada ATP en el tejido circundante. Una enzima en la superficie celular, conocida como CD73, convierte rápidamente el ATP en adenosina, una sustancia que normalmente ayuda a calmar la inflamación y a proteger el tejido sano. Sin embargo, dentro de los tumores, niveles elevados de adenosina actúan como un escudo químico, atenuando el ataque inmunitario y permitiendo que las células cancerosas persistan. El nuevo fármaco oral quemliclustat bloquea CD73, con el objetivo de reducir la adenosina y hacer que el microambiente tumoral sea menos acogedor para el cáncer y más favorable para las células inmunitarias. 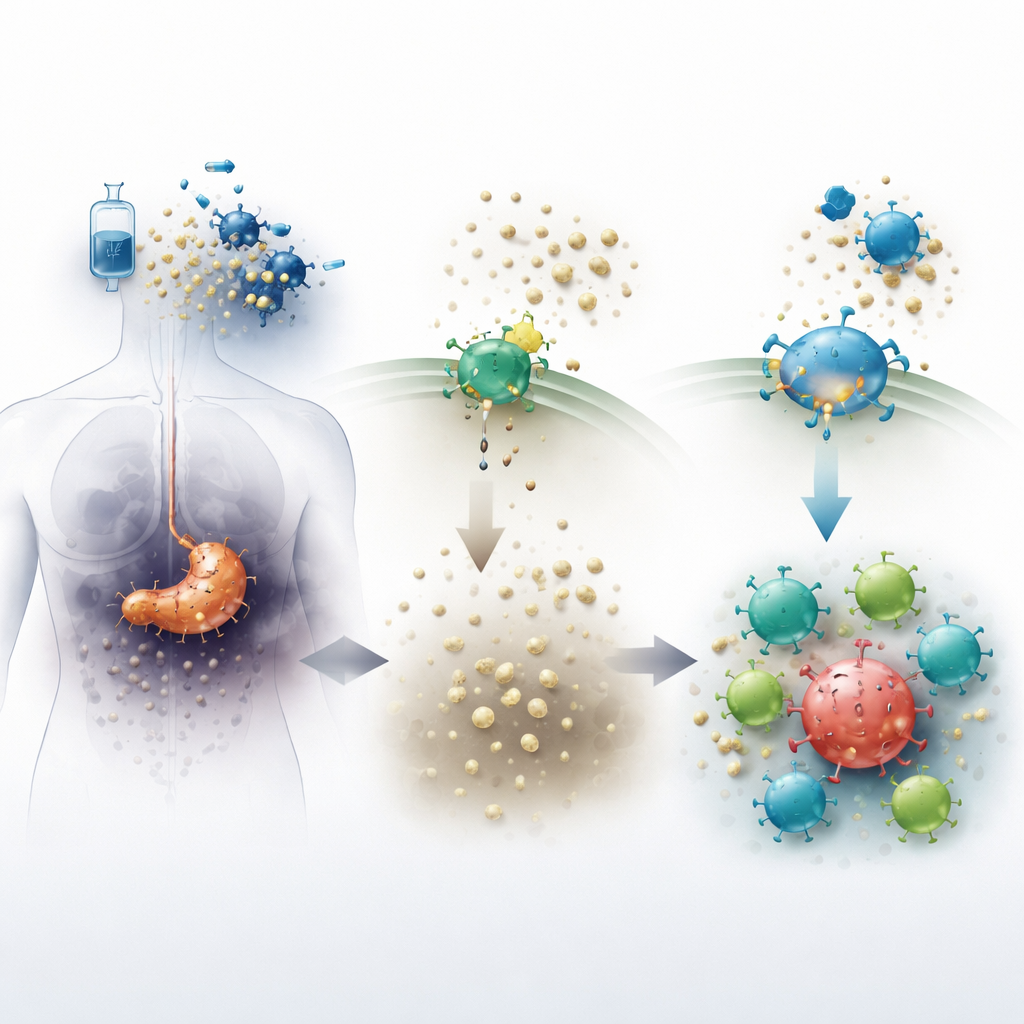
Probando una nueva combinación en pacientes
El ensayo ARC‑8 reclutó a personas cuyo cáncer de páncreas ya se había diseminado y que no habían recibido tratamiento para la enfermedad metastásica. Todos los participantes recibieron la combinación de quimioterapia estándar con gemcitabina y nab‑paclitaxel. En los grupos iniciales de búsqueda de dosis, los pacientes también recibieron quemliclustat junto con un anticuerpo inhibidor de puntos de control inmunitario llamado zimberelimab, que puede liberar los frenos moleculares sobre las células inmunitarias. Tras establecer una dosis segura de quemliclustat, el estudio se amplió a grupos mayores en los que los pacientes fueron asignados aleatoriamente para recibir quimioterapia más quemliclustat con o sin zimberelimab. Los objetivos principales fueron evaluar la seguridad y buscar señales tempranas de beneficio, como la reducción tumoral y la supervivencia.
Señales de seguridad y supervivencia
En todos los brazos del tratamiento, los efectos secundarios fueron muy semejantes a lo que los médicos esperan de este régimen de quimioterapia por sí solo, como fatiga, náuseas y disminución de las células sanguíneas. Las complicaciones inmunológicas graves fueron poco frecuentes, y la mayoría de los problemas severos se relacionaron con la quimioterapia más que con los fármacos nuevos. Al agrupar a los pacientes que recibieron la dosis recomendada de quemliclustat, se observó que los tumores se redujeron en aproximadamente un tercio de los pacientes y que se mantuvieron controlados en cerca de tres cuartas partes. La mediana de supervivencia global alcanzó alrededor de 16 meses en este grupo, notablemente superior a los aproximadamente 9 a 12 meses observados en varios ensayos recientes de quimioterapia sola. Una comparación cuidadosa con un grupo de control “sintético” construido a partir de estudios previos sugirió una ventaja de supervivencia de casi seis meses para los pacientes que recibieron la combinación con quemliclustat.
Descifrando cómo el fármaco remodela el microambiente tumoral
Para entender por qué algunos pacientes se beneficiaron más que otros, el equipo examinó patrones de actividad génica en biopsias tumorales y en células cultivadas en el laboratorio. Se centraron en un conjunto de genes llamado familia NR4A, que se activan cuando los niveles de adenosina son altos. En cultivos, añadir adenosina o sus precursores aumentó la expresión de genes NR4A en múltiples tipos celulares presentes en tumores pancreáticos, mientras que bloquear CD73 o los receptores de adenosina mantuvo esta señal baja. En muestras de pacientes, la propia quimioterapia aumentó la actividad de NR4A en muchas células asociadas al tumor, coherente con una oleada de adenosina tras el daño celular. De forma llamativa, los pacientes cuyos tumores mostraban niveles iniciales más altos de NR4A tendieron a vivir más con la terapia con quemliclustat, pero este patrón no se observó en dos ensayos externos en los que los pacientes recibieron quimioterapia similar sin quemliclustat. 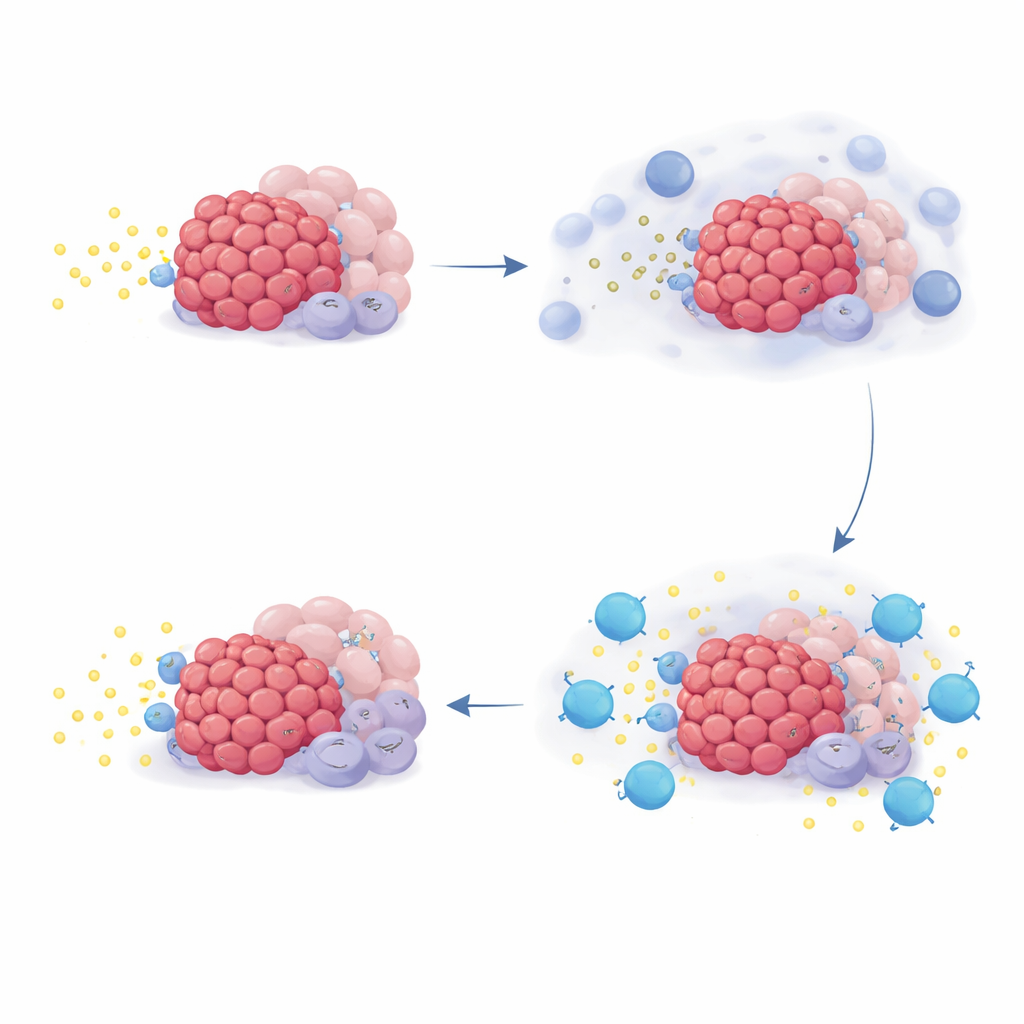
Devolver las células inmunitarias a la lucha
Imágenes avanzadas de cortes tumorales revelaron que las zonas con altos niveles de NR4A presentaban menos células T citotóxicas activadas en las cercanías, lo que sugiere que la adenosina crea un gradiente que mantiene a estas células a distancia. En pacientes a quienes se les tomaron biopsias antes y después del tratamiento, quemliclustat redujo en general las señales de NR4A en los tumores. Aquellos con la mayor disminución mostraron el mayor aumento en marcadores génicos de presencia y actividad de células T, y también disfrutaron de la mejor supervivencia global, con más de la mitad aún vivos pasados dos años. En conjunto, estos hallazgos apoyan la idea de que bloquear CD73 adelgaza la “niebla” de adenosina, permitiendo que las células inmunitarias se acerquen más a las células cancerosas y las ataquen con mayor eficacia.
Qué podría significar esto para los pacientes
Este ensayo de fase temprana se diseñó principalmente para evaluar la seguridad y carece de un grupo de control tradicional aleatorizado con solo quimioterapia, por lo que los resultados aún no pueden probar que quemliclustat prolongue la vida. Aun así, la combinación pareció tolerable y produjo tiempos de supervivencia que comparan favorablemente con estudios previos. Los análisis biológicos vinculan la exposición al fármaco, los cambios en la química tumoral y la activación inmunitaria con los resultados de los pacientes, lo que refuerza el argumento de que dirigir la adenosina es una estrategia prometedora. Un ensayo de fase 3 más amplio que ya está en marcha analizará si añadir quemliclustat a la quimioterapia estándar mejora de verdad la supervivencia de las personas con cáncer pancreático metastásico.
Cita: Wainberg, Z.A., Manji, G.A., Bahary, N. et al. Quemliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1 trial. Nat Med 32, 1267–1277 (2026). https://doi.org/10.1038/s41591-026-04283-z
Palabras clave: cáncer de páncreas, microambiente tumoral, inmunoterapia, vía de la adenosina, ensayo clínico