Clear Sky Science · it
Quemliclustat e chemioterapia con o senza zimberelimab nell’adenocarcinoma pancreatico metastatico: uno studio randomizzato di fase 1
Perché questo studio è importante
Il cancro del pancreas è uno dei tumori più letali, in parte perché viene spesso scoperto dopo che si è già diffuso e perché la chemioterapia standard regala ai pazienti solo un modesto tempo aggiuntivo. Questo studio testa una nuova strategia farmacologica che mira non solo ad attaccare direttamente le cellule tumorali, ma anche a dissipare una sorta di “nebbia” chimica che impedisce al sistema immunitario di intervenire efficacemente. Abbinando un farmaco mirato chiamato quemliclustat alla chemioterapia di routine, e talvolta a un anticorpo che potenzia la risposta immunitaria, i ricercatori hanno cercato di stabilire se sia possibile prolungare in sicurezza la sopravvivenza e sfruttare meglio le difese naturali dell’organismo.
Uno scudo chimico intorno al tumore
I tumori pancreatici creano un ambiente ostile che rende difficile il lavoro delle cellule immunitarie. Quando la chemioterapia uccide le cellule tumorali, queste rilasciano una molecola chiamata ATP nel tessuto circostante. Un enzima presente sulla superficie cellulare, noto come CD73, converte rapidamente l’ATP in adenosina, una sostanza che normalmente aiuta a calmare l’infiammazione e a proteggere i tessuti sani. All’interno dei tumori, però, alti livelli di adenosina agiscono come uno scudo chimico, attenuando l’attacco immunitario e permettendo alle cellule tumorali di persistere. Il nuovo farmaco orale quemliclustat blocca CD73, con l’obiettivo di ridurre l’adenosina e rendere il microambiente tumorale meno ospitale per il cancro e più accogliente per le cellule immunitarie. 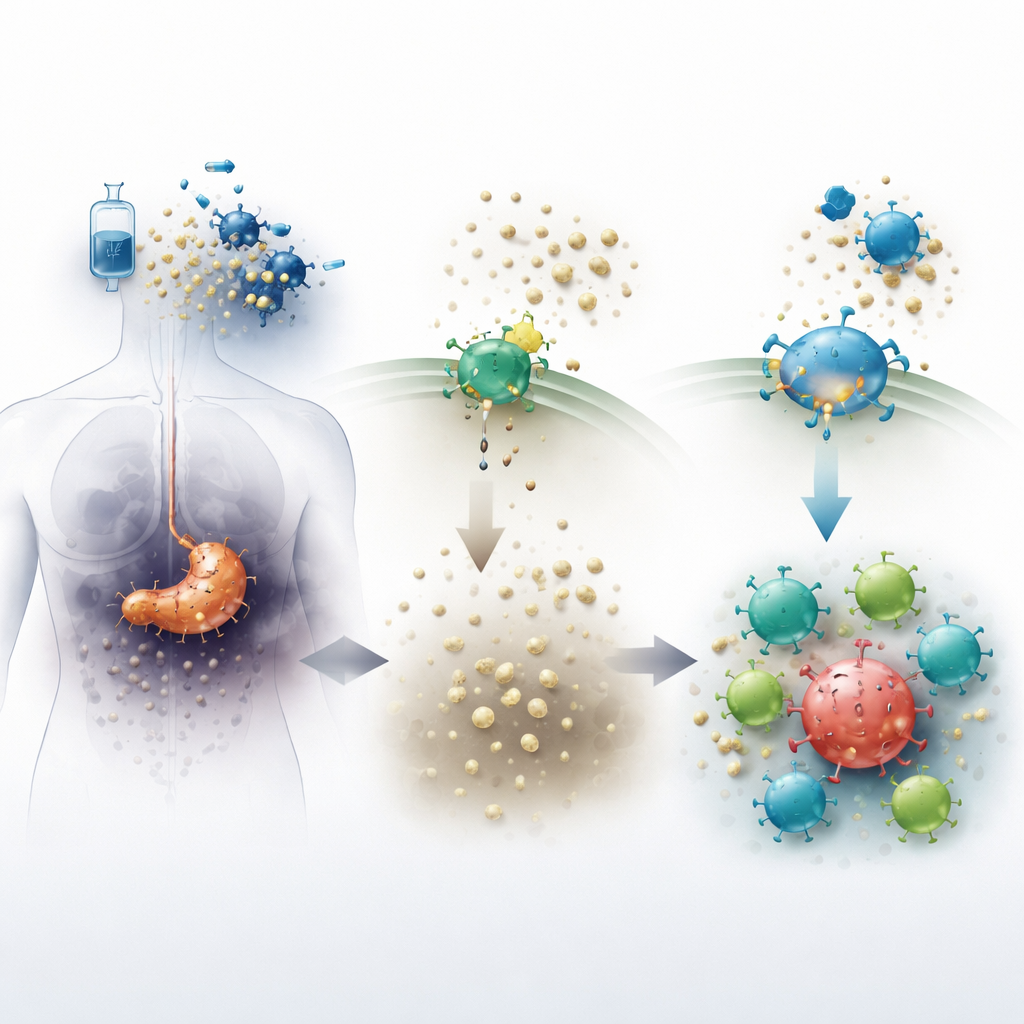
Testare una nuova combinazione nei pazienti
Lo studio ARC‑8 ha arruolato persone il cui cancro del pancreas si era già diffuso e che non avevano ancora ricevuto trattamenti per la malattia metastatica. Tutti i partecipanti hanno ricevuto una combinazione chemioterapica standard di gemcitabina e nab‑paclitaxel. Nei primi gruppi per la determinazione della dose, i pazienti hanno ricevuto anche quemliclustat insieme a un anticorpo contro i checkpoint immunitari chiamato zimberelimab, che può rimuovere i freni molecolari sulle cellule immunitarie. Dopo aver stabilito una dose sicura di quemliclustat, lo studio è stato ampliato in gruppi più grandi in cui i pazienti sono stati assegnati casualmente a ricevere la chemioterapia più quemliclustat con o senza zimberelimab. Gli obiettivi principali erano valutare la sicurezza e cercare segnali precoci di beneficio, come la riduzione del tumore e la sopravvivenza.
Segnali di sicurezza e sopravvivenza
In tutti i rami di trattamento, gli effetti collaterali sono risultati molto simili a quelli attesi da questo schema chemioterapico da solo, come affaticamento, nausea e diminuzione dei conteggi ematici. Complicanze immuno‑correlate gravi sono state rare e la maggior parte dei problemi più severi è stata attribuita alla chemioterapia piuttosto che ai nuovi farmaci. Quando i ricercatori hanno raggruppato i pazienti che avevano ricevuto la dose raccomandata di quemliclustat, hanno osservato che i tumori si sono ridotti in circa un terzo dei pazienti e sono rimasti sotto controllo in circa tre quarti dei casi. La sopravvivenza mediana globale ha raggiunto circa 16 mesi in questo gruppo, sensibilmente più lunga rispetto ai circa 9‑12 mesi riportati in diversi studi recenti sulla sola chemioterapia. Un confronto attento con un gruppo di controllo “sintetico” costruito da studi precedenti ha suggerito un vantaggio di sopravvivenza di quasi sei mesi per i pazienti trattati con la combinazione quemlilcustat.
Capire come il farmaco rimodella il microambiente tumorale
Per comprendere perché alcuni pazienti hanno beneficiato più di altri, il team ha analizzato i modelli di attività genica nelle biopsie tumorali e nelle cellule coltivate in laboratorio. Si sono concentrati su un insieme di geni chiamati famiglia NR4A, che si attivano quando i livelli di adenosina sono elevati. In colture cellulari, l’aggiunta di adenosina o dei suoi precursori aumentava l’espressione dei geni NR4A in diversi tipi cellulari presenti nei tumori pancreatici, mentre il blocco di CD73 o dei recettori dell’adenosina atteneva questo segnale. Nei campioni dei pazienti, la chemioterapia stessa aumentava l’attività di NR4A in molte cellule associate al tumore, coerentemente con un picco di adenosina dopo il danno cellulare. In modo interessante, i pazienti i cui tumori presentavano livelli iniziali più elevati di NR4A tendevano a vivere più a lungo con la terapia a base di quemliclustat, ma questo schema non si è osservato in due studi esterni in cui i pazienti avevano ricevuto una chemioterapia simile senza quemliclustat. 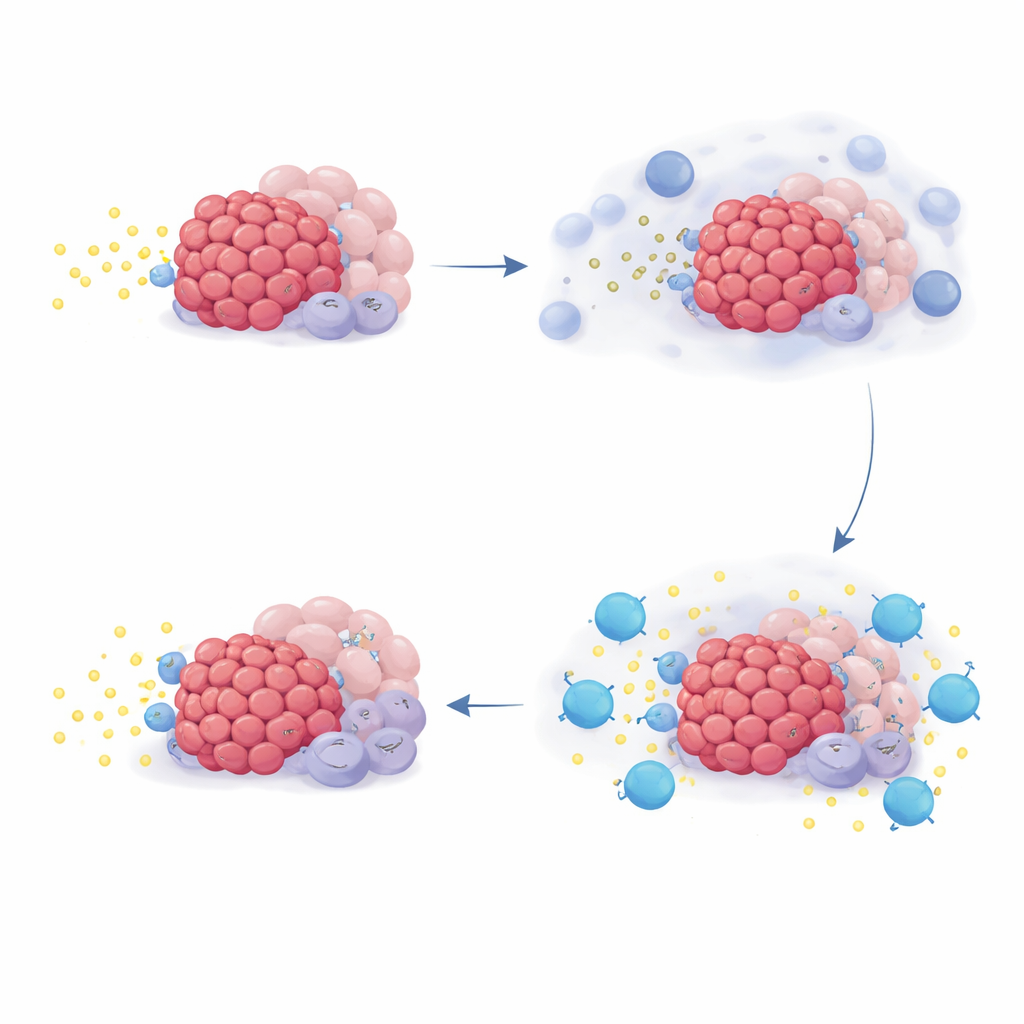
Riportare le cellule immunitarie nella battaglia
Immagini avanzate di fette tumorali hanno rivelato che le aree con alti livelli di NR4A avevano meno cellule T killer attivate nelle immediate vicinanze, suggerendo che l’adenosina crea un gradiente che tiene queste cellule a distanza. Nei pazienti che hanno avuto biopsie prima e dopo il trattamento, quemliclustat ha generalmente ridotto i segnali di NR4A nei tumori. Chi ha mostrato il calo maggiore ha manifestato il più forte aumento nei marcatori genici di presenza e attività delle cellule T, e ha goduto anche della migliore sopravvivenza complessiva, con più della metà ancora in vita oltre i due anni. Nel complesso, questi risultati supportano l’idea che bloccare CD73 diradi la “nebbia” di adenosina, permettendo alle cellule immunitarie di avvicinarsi alle cellule tumorali e attaccarle più efficacemente.
Cosa potrebbe significare per i pazienti
Questo trial di fase iniziale era progettato principalmente per valutare la sicurezza e non include un tradizionale gruppo di controllo randomizzato trattato solo con chemioterapia, quindi i risultati non possono ancora dimostrare definitivamente che quemliclustat allunga la vita. Tuttavia, la combinazione è risultata tollerabile e ha prodotto tempi di sopravvivenza che confrontano favorevolmente con studi passati. Le analisi biologiche collegano l’esposizione al farmaco, i cambiamenti nella chimica tumorale e l’attivazione immunitaria agli esiti dei pazienti, rafforzando l’ipotesi che mirare all’adenosina sia una strategia promettente. Un più ampio trial di fase 3 in corso valuterà ora se aggiungere quemliclustat alla chemioterapia standard migliori effettivamente la sopravvivenza delle persone affette da cancro pancreatico metastatico.
Citazione: Wainberg, Z.A., Manji, G.A., Bahary, N. et al. Quemliclustat and chemotherapy with or without zimberelimab in metastatic pancreatic adenocarcinoma: a randomized phase 1 trial. Nat Med 32, 1267–1277 (2026). https://doi.org/10.1038/s41591-026-04283-z
Parole chiave: cancro del pancreas, microambiente tumorale, immunoterapia, via dell’adenosina, studio clinico