Clear Sky Science · sv
Transport av ett intermediärt FeMo-ko faktor‑byggnadsteg i nitrogenas
Hur mikrober hjälper till att föda världen
Kväve är en grundläggande byggsten i DNA och proteiner, men de flesta levande organismer kan inte utnyttja den stora reserven av kvävgas i luften. Istället är de beroende av specialiserade mikrober som omvandlar denna gas till former som växter kan ta upp, och på så vis tyst stödjer både jordbruk och naturliga ekosystem. Den här artikeln ger en inblick i en av de mest intrikata molekylära maskinerierna bakom det här tricket och ställer en enkel fråga: hur bygger celler noggrant upp och överlämnar den lilla metallklustern i mitten av kvävefixeringsenzymet utan att tappa den på vägen?
Den lilla motorn inne i kvävefixerande bakterier
Många mark‑ och vattenmikrober använder ett enzym som kallas nitrogenas för att omvandla kvävgas till ammoniak, som växter sedan använder som gödningsämne. Den vanligaste versionen av detta enzym förlitar sig på en komplex metallkluster kallad FeMo‑ko faktorn, byggd av järn, svavel, kol, molybden och en organisk sidogrupp känd som homocitrat. Denna ko faktor monteras inte inne i det färdiga enzymet av sig själv. Istället bygger cellerna upp den steg för steg på hjälpproteiner och levererar den sedan in i nitrogenasens aktiva säte. Att förstå hur denna monteringslinje fungerar är avgörande inte bara för grundläggande biologi utan också för långsiktiga mål, såsom att designa grödor eller industriella system som fixerar kväve mer effektivt och med mindre energi än dagens gödselproduktion.
En molekylär stafett för ett skört gods
Studien fokuserar på ett viktigt sent steg i denna monteringslinje. Vid detta stadium har ett annat enzym, NifB, redan format en stor järn‑svavel‑kluster kallad NifB‑co. Denna sköra kluster måste förflyttas till ett stödproteinkomplex, NifEN, där den kommer att omvandlas till den slutliga FeMo‑ko faktorn. Ett litet bärarprotein, NifX, fungerar som en kurir som plockar upp NifB‑co från dess födelseplats och för det till NifEN. Med högupplösande kryo‑elektronmikroskopi fångade författarna NifEN tillsammans med NifX och NifB‑co, i praktiken frös överlämningen mitt i rörelsen. De fann att NifX är förankrat i NifEN via sin svans men lämnar sin huvudkropp flexibel, vilket gör att det kan svänga sin last i position.
Att se överlämningen i atomdetalj
Bilderna visar att NifB‑co först dockar på NifEN:s yttre yta, där två svavelinnehållande aminosyror i början av NifE‑subenheten greppar klustern i motsatta ändar. I ett särskilt "transfer"‑tillstånd hålls ena änden av klustern fortfarande av en histidin på NifX medan den andra fångas av NifE. Detta skapar ett kort ögonblick då godset bokstavligen delas mellan kuriren och stommen, vilket säkerställer en säker, direkt överlämning som minimerar exponering för omgivningen. Biokemiska tester med mutanta stammar av den kvävefixerande bakterien Azotobacter vinelandii visade att när denna N‑terminala griploop på NifE tas bort, har cellerna svårt att växa enbart på kvävgas, särskilt när NifB‑co är sällsynt, vilket understryker hur avgörande denna dockningsplats är för effektiv ko faktor‑produktion.
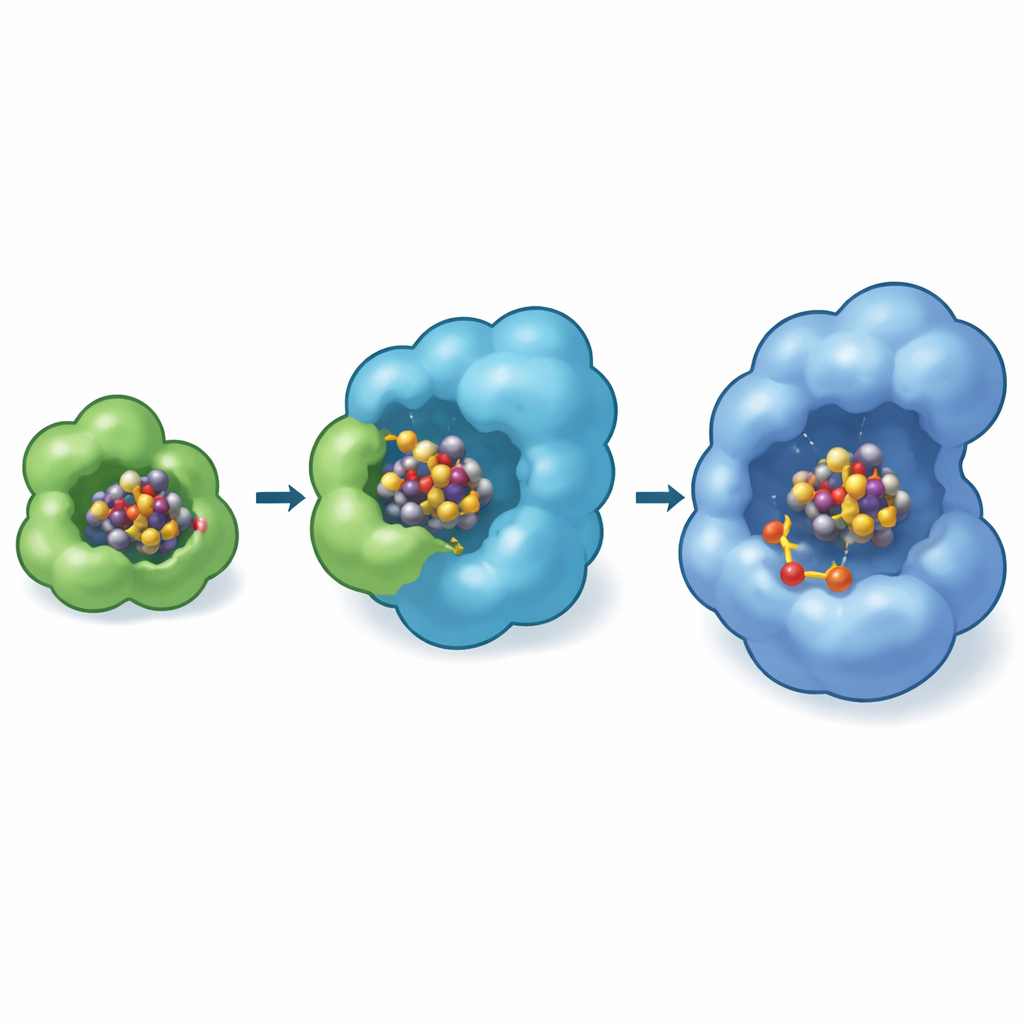
En dold verkstad inne i stommen
Det är anmärkningsvärt att den experimentellt observerade dockningsplatsen på NifEN ligger nära proteinets yta, medan den mogna FeMo‑ko faktorn i det färdiga nitrogenasenzymet sitter djupt inne i en kavity. För att överbrygga detta gap använde författarna avancerade datoriska modeller (Boltz‑2) för att förutsäga var klustern kan röra sig härnäst. Dessa simuleringar placerade konsekvent NifB‑co i ett inre fack i NifEN nära en specifik cysteinrest som är känd för att vara väsentlig för ko faktor‑bildningen. Modellerna föreslog vidare att detta inre fack är där molybden och homocitrat läggs till klustern, vilket omvandlar NifB‑co till den kompletta FeMo‑ko faktorn. Inom samma modelleringsram binder NifX sin last i ett positivt laddat fack som överensstämmer med den experimentella strukturen, vilket stärker idén om en definierad rutt: NifX → yttre mottagarställe på NifE → intern omvandlingskammare.
Varför denna osynliga dans är viktig
Tillsammans skisserar de strukturella ögonblicksbilderna och simuleringarna en koreograferad sekvens för att bygga nitrogenasens hjärta: en kostbar metallkluster tillverkas, överlämnas från bärare till stomme, förflyttas in i en inre kammare och uppgraderas först där med molybden och homocitrat innan den vidarebefordras till det slutliga enzymet. För en allmän läsare är huvudbudskapet att livet investerar stor omsorg i hanteringen av värdefulla kemiska delar, med en kedja av specialiserade proteiner som skyddar och förädlar dem. Genom att klargöra hur denna molekylära stafett fungerar lägger studien till en viktig pusselbit i vår förståelse av biologisk kvävefixering, en process som ligger till grund för markens bördighet och livsmedelsproduktionen världen över och som en dag kan inspirera renare, mer hållbara sätt att framställa gödsel.
Citering: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
Nyckelord: kvävefixering, nitrogenas, metall‑koenzymer, kryoelektronmikroskopi, enzymuppbyggnad