Clear Sky Science · fr
Trafic d’un intermédiaire d’assemblage du FeMo-cofacteur de la nitrogénase
Comment les microbes aident à nourrir le monde
L’azote est un ingrédient de base de l’ADN et des protéines, et pourtant la plupart des êtres vivants ne peuvent pas utiliser l’énorme réserve d’azote gazeux présente dans l’air. Ils dépendent plutôt de microbes spécialisés qui transforment ce gaz en formes assimilables par les plantes, soutenant discrètement l’agriculture mondiale et les écosystèmes naturels. Cet article explore l’une des machines moléculaires les plus complexes à l’œuvre dans ce processus et pose une question simple : comment les cellules construisent-elles et transmettent-elles avec soin le minuscule agglomérat métallique au cœur de l’enzyme fixatrice d’azote sans le laisser tomber en chemin ?
Le petit moteur à l’intérieur des bactéries fixatrices d’azote
De nombreux microbes du sol et des milieux aquatiques utilisent une enzyme appelée nitrogénase pour convertir l’azote gazeux en ammoniac, que les plantes utilisent ensuite comme fertilisant. La version la plus courante de cette enzyme repose sur un complexe métallique appelé FeMo-cofacteur, composé de fer, de soufre, de carbone, de molybdène et d’un fragment organique nommé homocitrate. Ce cofacteur ne s’assemble pas seul une fois l’enzyme formée. Les cellules le construisent étape par étape sur des protéines auxiliaires, puis le livrent dans le site actif de la nitrogénase. Comprendre le fonctionnement de cette chaîne de montage est crucial non seulement pour la biologie fondamentale, mais aussi pour des objectifs à long terme, comme concevoir des cultures ou des systèmes industriels qui fixent l’azote plus efficacement et avec moins d’énergie que la production d’engrais actuelle.
Un relais moléculaire pour un chargement fragile
L’étude se concentre sur une étape clé tardive de cette chaîne d’assemblage. À ce stade, une autre enzyme, NifB, a déjà forgé un grand cluster fer–soufre appelé NifB-co. Ce cluster fragile doit être transféré sur une paire de protéines échafaudage, NifEN, où il sera converti en FeMo-cofacteur final. Une petite protéine porteuse, NifX, joue le rôle de coursier qui récupère NifB-co à son site de naissance et l’apporte à NifEN. Grâce à la cryo–microscopie électronique à haute résolution, les auteurs ont capturé NifEN avec NifX et NifB-co, congelant ainsi la passation en plein mouvement. Ils ont observé que NifX est ancré à NifEN par sa queue tout en gardant son corps principal flexible, ce qui lui permet de balancer sa cargaison en position.
Voir la passation dans le détail atomique
Les images révèlent que NifB-co s’arrime d’abord à la surface externe de NifEN, où deux acides aminés contenant du soufre situés au début de la sous-unité NifE saisissent le cluster à ses extrémités opposées. Dans un état spécial de « transfert », une extrémité du cluster est encore tenue par une histidine de NifX tandis que l’autre est capturée par NifE. Cela crée un bref instant où la cargaison est littéralement partagée entre le coursier et l’échafaudage, assurant une passe directe et sécurisée qui minimise l’exposition à l’environnement. Des tests biochimiques utilisant des souches mutantes de la bactérie fixatrice d’azote Azotobacter vinelandii ont montré que lorsque cette boucle de préhension N‑terminal sur NifE est supprimée, les cellules peinent à croître uniquement à partir d’azote gazeux, surtout lorsque NifB-co est rare, soulignant l’importance vitale de ce site d’arrimage pour une production efficace du cofacteur.
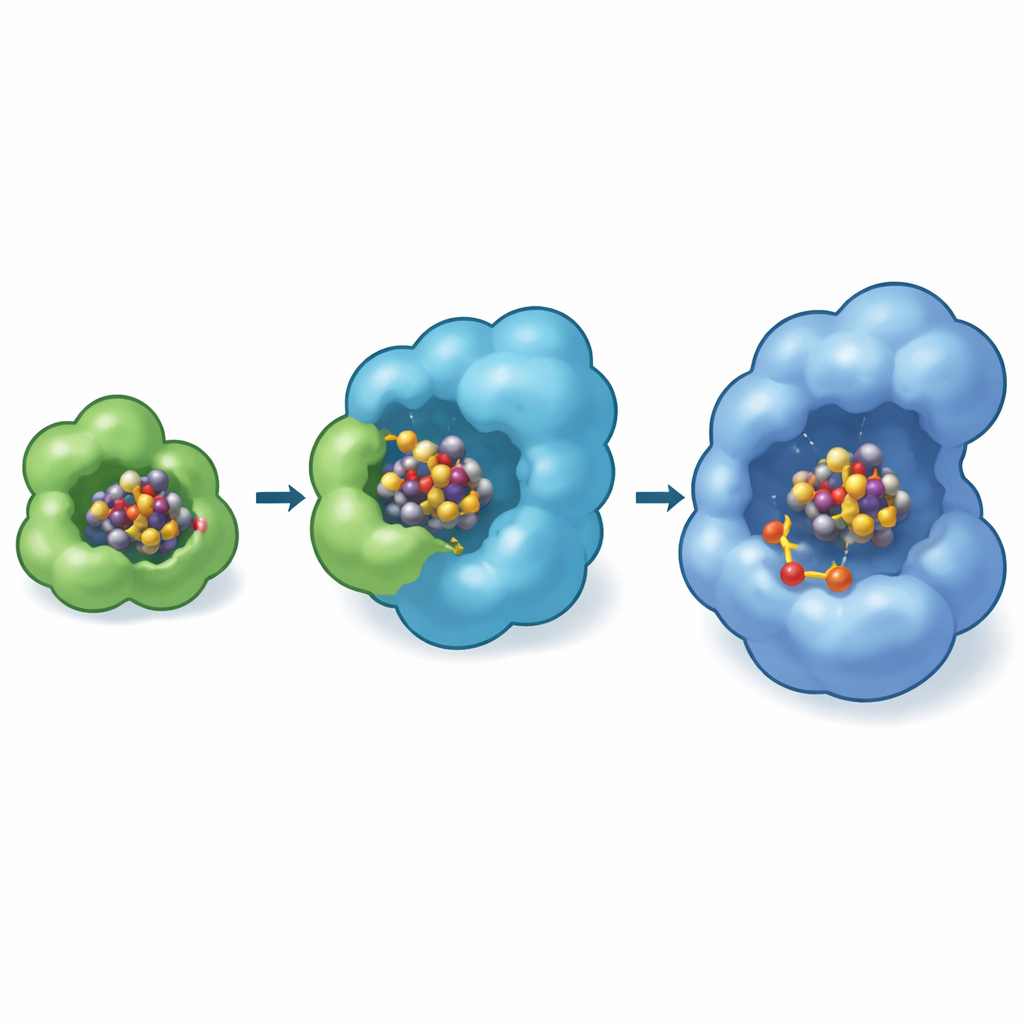
Un atelier caché à l’intérieur de l’échafaudage
Fait curieux, le site d’arrimage observé expérimentalement sur NifEN se trouve près de la surface protéique, tandis que dans l’enzyme nitrogénase aboutie, le FeMo-cofacteur mature est logé profondément à l’intérieur d’une cavité. Pour combler cet écart, les auteurs ont utilisé des modèles informatiques avancés (Boltz-2) pour prédire où le cluster pourrait se déplacer ensuite. Ces simulations ont à plusieurs reprises placé NifB-co dans une poche interne de NifEN près d’une cystéine spécifique connue pour être essentielle à la formation du cofacteur. Les modèles ont en outre suggéré que cette poche interne est l’endroit où le molybdène et l’homocitrate sont ajoutés au cluster, transformant NifB-co en FeMo-cofacteur complet. Dans le même cadre de modélisation, NifX lie sa cargaison dans une poche chargée positivement qui correspond à la structure expérimentale, renforçant l’idée d’un itinéraire défini : NifX → site de réception en surface sur NifE → chambre interne de conversion.
Pourquoi cette danse invisible compte
Pris ensemble, les instantanés structuraux et les simulations décrivent une séquence chorégraphiée pour fabriquer le cœur de la nitrogénase : un cluster métallique coûteux est fabriqué, remis du porteur à l’échafaudage, déplacé dans une chambre interne, puis seulement là enrichi en molybdène et homocitrate avant d’être transmis à l’enzyme finale. Pour le lecteur général, le message clé est que la vie investit un soin considérable pour gérer des pièces chimiques précieuses, en utilisant une chaîne de protéines spécialisées pour les protéger et les affiner. En éclairant le fonctionnement de ce relais moléculaire, l’étude apporte une pièce importante à notre compréhension de la fixation biologique de l’azote, un processus qui soutient la fertilité des sols et la production alimentaire dans le monde et pourrait un jour inspirer des moyens plus propres et plus durables de fabriquer des engrais.
Citation: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
Mots-clés: fixation de l’azote, nitrogénase, cofacteurs métalliques, cryo-microscopie électronique, assemblage enzymatique