Clear Sky Science · de
Transport eines Nitrogenase-FeMo-Kofaktor-Bauzwischenstücks
Wie Mikroben helfen, die Welt zu ernähren
Stickstoff ist ein Grundbaustein von DNA und Proteinen, doch die meisten Lebewesen können das riesige Reservoir an Stickstoffgas in der Luft nicht direkt nutzen. Stattdessen sind sie auf spezialisierte Mikroben angewiesen, die dieses Gas in für Pflanzen verfügbare Formen umwandeln und so stillschweigend die globale Landwirtschaft und natürliche Ökosysteme stützen. Dieser Artikel blickt in eine der komplexesten molekularen Maschinen hinter diesem Kunststück und stellt eine einfache Frage: Wie bauen Zellen das winzige Metallcluster im Zentrum des stickstofffixierenden Enzyms sorgfältig zusammen und geben es weiter, ohne es unterwegs fallen zu lassen?
Der winzige Motor in stickstofffixierenden Bakterien
Viele Boden- und Wasser-Mikroben nutzen ein Enzym namens Nitrogenase, um Stickstoffgas in Ammoniak umzuwandeln, das Pflanzen als Dünger verwenden. Die verbreitetste Version dieses Enzyms beruht auf einem komplexen Metallcluster, dem FeMo-Kofaktor, der aus Eisen, Schwefel, Kohlenstoff, Molybdän und einem organischen Seitenstück, dem Homozitrat, aufgebaut ist. Dieser Kofaktor entsteht nicht von selbst innerhalb des fertigen Enzyms. Stattdessen bauen Zellen ihn schrittweise auf Helferproteinen auf und liefern ihn dann an die Wirkortstelle der Nitrogenase aus. Zu verstehen, wie diese Produktionslinie arbeitet, ist nicht nur für die Grundlagenforschung wichtig, sondern auch für längerfristige Ziele wie die Entwicklung von Nutzpflanzen oder industriellen Systemen, die Stickstoff effizienter und mit weniger Energieaufwand binden als die heutige Düngemittelherstellung.
Ein molekularer Staffellauf für eine fragile Fracht
Die Studie konzentriert sich auf einen wichtigen späten Schritt dieser Aufbaukette. In diesem Stadium hat ein anderes Enzym, NifB, bereits ein großes Eisen-Schwefel-Cluster namens NifB-co geschmiedet. Dieses fragile Cluster muss zu einem Gerüstprotein-Paar, NifEN, transportiert werden, wo es in den finalen FeMo-Kofaktor umgewandelt wird. Ein kleines Trägerprotein, NifX, fungiert wie ein Kurier, der NifB-co von seinem Entstehungsort aufnimmt und zu NifEN bringt. Mithilfe hochauflösender Kryo-Elektronenmikroskopie hielten die Autoren NifEN zusammen mit NifX und NifB-co fest und frierten so die Übergabe in einer Zwischenstufe ein. Sie fanden heraus, dass NifX mit seinem Schwanz an NifEN verankert ist, während sein Hauptkörper flexibel bleibt, sodass es seine Fracht in Position schwenken kann.
Die Übergabe in atomarer Detailansicht
Die Aufnahmen zeigen, dass NifB-co zunächst an der Außenseite von NifEN andockt, wo zwei schwefelhaltige Aminosäuren am Beginn der NifE-Untereinheit das Cluster an gegenüberliegenden Enden greifen. In einem speziellen „Transfer“-Zustand wird ein Ende des Clusters noch von einem Histidin auf NifX gehalten, während das andere von NifE erfasst wird. Das schafft einen kurzen Moment, in dem die Fracht buchstäblich zwischen Kurier und Gerüst geteilt wird, was eine sichere, direkte Übergabe gewährleistet und die Exposition gegenüber der Umgebung minimiert. Biochemische Tests mit Mutantenstämmen des stickstofffixierenden Bakteriums Azotobacter vinelandii zeigten, dass, wenn diese N-terminale Greifschleife auf NifE entfernt wird, die Zellen Schwierigkeiten haben, allein mit Stickstoffgas zu wachsen — besonders wenn NifB-co knapp ist — und unterstreichen damit, wie essentiell diese Andockstelle für eine effiziente Kofaktorproduktion ist.
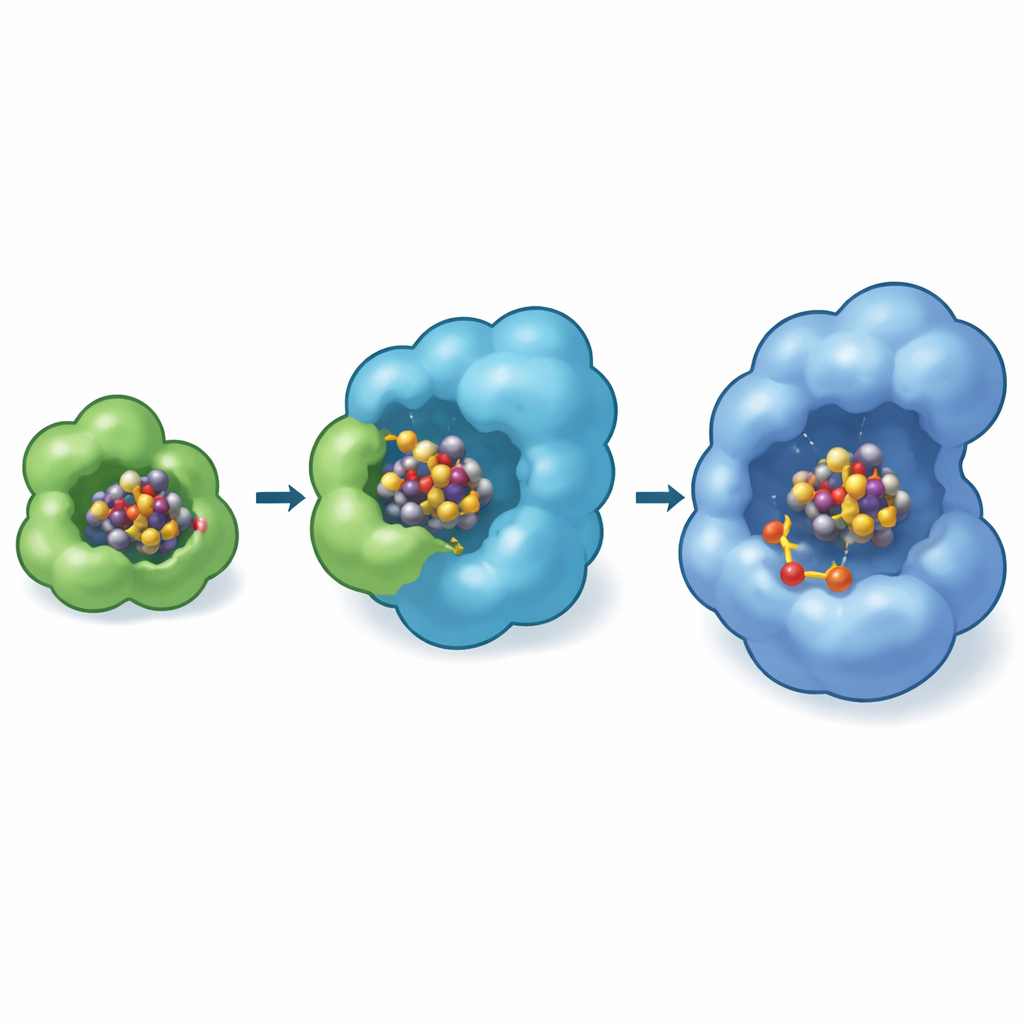
Eine verborgene Werkstatt im Inneren des Gerüsts
Interessanterweise liegt die experimentell beobachtete Andockstelle auf NifEN nahe der Proteinoberfläche, während der reife FeMo-Kofaktor im fertigen Nitrogenase-Enzym tief in einer Kavität sitzt. Um diese Lücke zu schließen, nutzten die Autoren fortgeschrittene Computermodelle (Boltz-2), um vorherzusagen, wohin das Cluster als Nächstes wandern könnte. Diese Simulationen platzierten NifB-co wiederholt in einer inneren Tasche von NifEN in der Nähe einer spezifischen Cystein-Restgruppe, von der bekannt ist, dass sie für die Kofaktorenbildung essentiell ist. Die Modelle legten nahe, dass diese innere Tasche der Ort ist, an dem Molybdän und Homozitrat dem Cluster hinzugefügt werden und NifB-co in den kompletten FeMo-Kofaktor verwandeln. Im selben Modellrahmen bindet NifX seine Fracht in einer positiv geladenen Tasche, die zur experimentellen Struktur passt, was die Idee einer definierten Route verstärkt: NifX → Oberflächen-Empfangsstelle auf NifE → interne Umwandlungskammer.
Warum dieser unsichtbare Tanz wichtig ist
Zusammengefasst zeichnen die strukturellen Momentaufnahmen und Simulationen eine choreografierte Abfolge für den Aufbau des Nitrogenase-Kerns: Ein aufwändig hergestelltes Metallcluster wird produziert, vom Träger zum Gerüst übergeben, in eine Innenkammer verlagert und erst dort mit Molybdän und Homozitrat ergänzt, bevor es an das finale Enzym weitergegeben wird. Für den allgemeinen Leser ist die zentrale Botschaft, dass das Leben großen Aufwand betreibt, um wertvolle chemische Bauteile zu verwalten, indem es eine Kette spezialisierter Proteine nutzt, um sie zu schützen und zu veredeln. Indem die Studie klärt, wie diese molekulare Übergabe funktioniert, liefert sie ein wichtiges Puzzleteil zum Verständnis der biologischen Stickstofffixierung — eines Prozesses, der die Bodenfruchtbarkeit und Nahrungsmittelproduktion weltweit stützt und eines Tages sauberere, nachhaltigere Wege zur Düngerherstellung inspirieren könnte.
Zitation: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
Schlüsselwörter: Stickstofffixierung, Nitrogenase, Metallkofaktoren, Kryo-Elektronenmikroskopie, Enzymaufbau