Clear Sky Science · pl
Transport pośredniowy międzyfazowego fragmentu składowego FeMo-kofaktora nitrogenazy
Jak mikroby pomagają karmić świat
Azot jest podstawowym składnikiem DNA i białek, a mimo to większość organizmów nie potrafi wykorzystać olbrzymiego zasobu gazowego azotu w powietrzu. Polegają więc na wyspecjalizowanych mikroorganizmach, które przekształcają ten gaz w formy przyswajalne dla roślin, cicho wspierając rolnictwo i ekosystemy naturalne. Ten artykuł zagląda w jeden z najbardziej złożonych mechanizmów molekularnych stojących za tym procesem i stawia proste pytanie: jak komórki ostrożnie składają i przekazują maleńki skup metalowy będący sercem enzymu wiążącego azot, nie upuszczając go po drodze?
Malutki silnik w bakteriach wiążących azot
Wiele mikroorganizmów glebowych i wodnych korzysta z enzymu zwanego nitrogenazą, który przekształca gazowy azot w amoniak, wykorzystywany przez rośliny jako nawóz. Najczęstsza wersja tego enzymu opiera się na złożonym skupie metali zwanym FeMo-kofaktorem, zbudowanym z żelaza, siarki, węgla, molibdenu i organicznego fragmentu nazywanego homocystynianem. Ten kofaktor nie składa się sam wewnątrz gotowego enzymu. Zamiast tego komórki konstruują go etapami na białkach pomocniczych, a następnie dostarczają do aktywnego miejsca nitrogenazy. Zrozumienie, jak działa ta linia montażowa, jest kluczowe nie tylko dla biologii podstawowej, lecz także dla długoterminowych celów, takich jak projektowanie upraw czy systemów przemysłowych, które wiążą azot efektywniej i z mniejszym nakładem energii niż obecna produkcja nawozów.
Molekularny przekaz dla kruchego ładunku
Badanie skupia się na kluczowym późnym etapie tej linii montażowej. Na tym etapie inny enzym, NifB, już uformował duży skup żelazo–siarka zwany NifB-co. Ten kruchy skup musi zostać przeniesiony na parę białek rusztowaniowych, NifEN, gdzie zostanie przekształcony w końcowy FeMo-kofaktor. Małe białko nośnikowe, NifX, działa jak kuriere — odbiera NifB-co z miejsca jego powstania i dostarcza je do NifEN. Korzystając z wysokorozdzielczej kriomikroskopii elektronowej, autorzy uchwycili NifEN wraz z NifX i NifB-co, skutecznie zamrażając przekazanie w półruchu. Stwierdzili, że NifX jest zakotwiczony do NifEN za pomocą ogona, lecz utrzymuje elastyczność głównej części, co pozwala mu zamachnąć ładunkiem i umieścić go na właściwym miejscu.
Zobaczyć przekaz na poziomie atomowym
Obrazy pokazują, że NifB-co najpierw dokuje na zewnętrznej powierzchni NifEN, gdzie dwa aminokwasy zawierające siarkę na początku podjednostki NifE chwycają skup na przeciwnych końcach. W specjalnym stanie „transferowym” jeden koniec skupy nadal trzyma histydyna na NifX, podczas gdy drugi jest przejmowany przez NifE. Powstaje krótkotrwały moment, gdy ładunek jest dosłownie dzielony między kuriera a rusztowanie, zapewniając bezpieczne, bezpośrednie przekazanie, które minimalizuje kontakt z otoczeniem. Testy biochemiczne z użyciem mutantów bakterii wiążącej azot Azotobacter vinelandii wykazały, że gdy pętla chwytająca na N-końcu NifE zostaje usunięta, komórkom trudno rosnąć tylko na gazowym azocie, szczególnie gdy NifB-co jest rzadki, co podkreśla, jak istotne jest to miejsce dokujące dla wydajnej produkcji kofaktora.
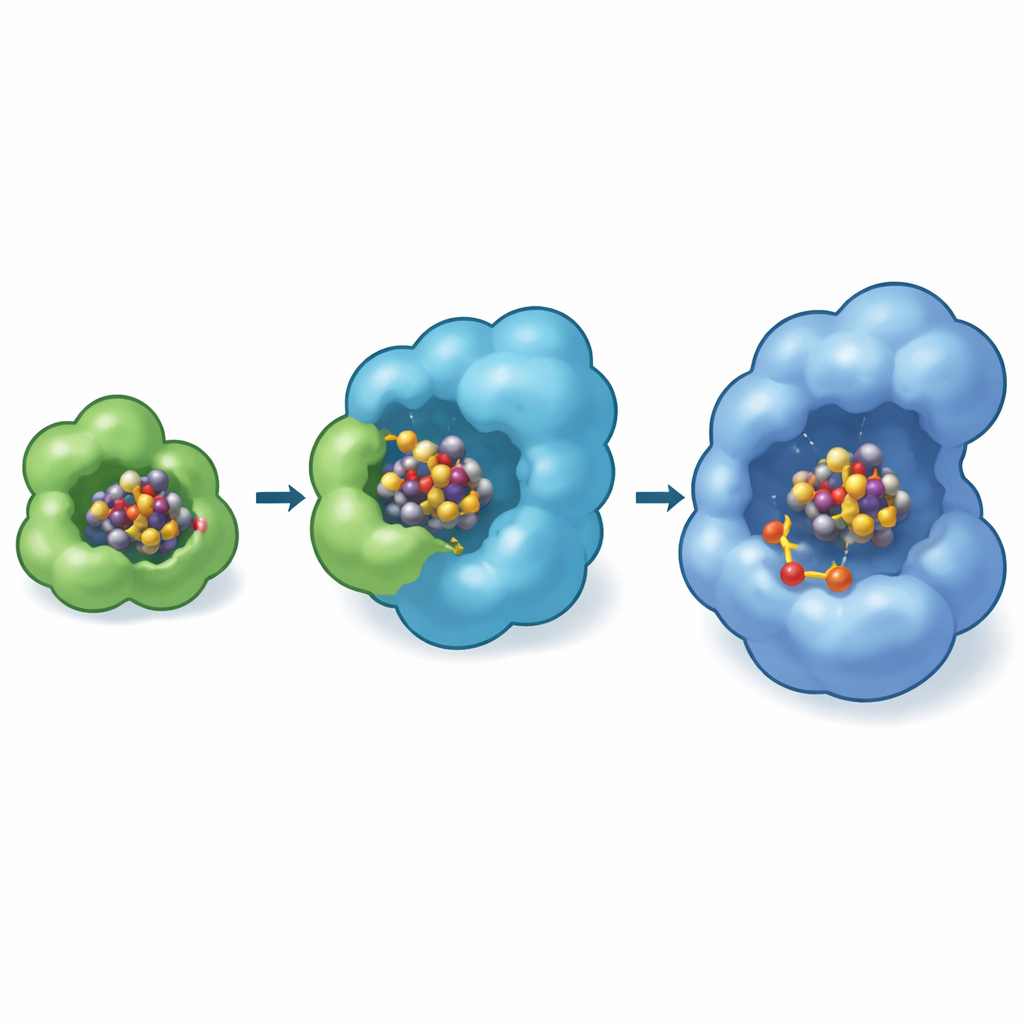
Ukryty warsztat wewnątrz rusztowania
Co ciekawe, doświadczalnie zaobserwowane miejsce dokowania na NifEN leży blisko powierzchni białka, podczas gdy w gotowej nitrogenazie dojrzały FeMo-kofaktor znajduje się głęboko w zatoczce. Aby pokonać tę różnicę, autorzy użyli zaawansowanych modeli komputerowych (Boltz-2), by przewidzieć, dokąd skup mógłby się przesunąć dalej. Symulacje wielokrotnie lokowały NifB-co w wewnętrznej kieszeni NifEN blisko określonego resztu cysteiny, który jest znany jako niezbędny do formowania kofaktora. Modele sugerowały ponadto, że to wewnętrzne zagłębienie jest miejscem, gdzie dodawany jest molibden i homocystynian, przekształcając NifB-co w kompletny FeMo-kofaktor. W tym samym ramieniu modelowym NifX wiąże swój ładunek w dodatnio naładowanej kieszeni zgodnej ze strukturą eksperymentalną, wzmacniając obraz wyraźnej trasy: NifX → powierzchniowe miejsce przyjęcia na NifE → wewnętrzna komora konwersji.
Dlaczego ten niewidoczny taniec ma znaczenie
W sumie migawki strukturalne i symulacje szkicują wyreżyserowaną sekwencję budowy serca nitrogenazy: kosztowny skup metalowy jest zbudowany, przekazany z nośnika na rusztowanie, przeniesiony do wewnętrznej komory, a dopiero potem wzbogacony o molibden i homocystynian przed przekazaniem do końcowego enzymu. Dla czytelnika ogólnego kluczowe przesłanie brzmi: życie przykłada ogromną staranność do zarządzania cennymi częściami chemicznymi, używając łańcucha wyspecjalizowanych białek, by je chronić i udoskonalać. Wyjaśniając, jak działa ten molekularny przekaz, badanie wnosi istotny element do naszego rozumienia biologicznego wiązania azotu — procesu, który leży u podstaw żyzności gleby i produkcji żywności na całym świecie i który może pewnego dnia inspirować czystsze, bardziej zrównoważone metody wytwarzania nawozów.
Cytowanie: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
Słowa kluczowe: wiązanie azotu, nitrogenaza, metalowe kofaktory, kriomikroskopia elektronowa, składanie enzymów