Clear Sky Science · ja
窒素還元酵素FeMo補因子組立中間体の輸送
微生物はどう世界の食を支えるか
窒素はDNAやタンパク質の基本成分ですが、大気中に豊富にある窒素ガスをそのまま利用できる生物は多くありません。代わりに、植物が利用できる形にこのガスを変換する特殊な微生物に依存しており、これらは世界の農業と自然生態系を静かに支えています。本記事は、その仕組みの背後にある最も精巧な分子機械の一つをのぞき込み、単純な問いを投げかけます:細胞は窒素固定酵素の中心にある小さな金属クラスターを、落とすことなくいかに慎重に組み立て、受け渡すのか?
窒素固定細菌の中の小さなエンジン
多くの土壌や水中の微生物は、窒素ガスをアンモニアに変換する酵素、窒素還元酵素を用います。植物はそのアンモニアを肥料として利用します。最も一般的な型のこの酵素は、鉄、硫黄、炭素、モリブデン、およびホモシトレートと呼ばれる有機側鎖からなる複雑な金属クラスター、FeMo補因子に依存しています。この補因子は完成した酵素内で自律的に組み立てられるのではなく、補助タンパク質上で段階的に構築されてから窒素還元酵素の働く場へと渡されます。この組立ラインの仕組みを理解することは、基礎生物学だけでなく、将来的に窒素をより効率的かつ低エネルギーで固定できる作物や産業システムの設計といった長期的な目標にも重要です。
壊れやすい荷物のための分子リレー
この研究はその組立ラインの重要な後期段階に焦点を当てています。この段階では、別の酵素NifBがすでにNifB-coと呼ばれる大きな鉄–硫黄クラスターを作り上げています。この壊れやすいクラスターは、最終的なFeMo補因子に変換される足場タンパク質ペアであるNifENへ移されなければなりません。小さな運搬タンパク質NifXは、生まれた場所からNifB-coを受け取りNifENに運ぶ運送人のように働きます。高分解能のクライオ電子顕微鏡を用いて、著者らはNifENとNifXおよびNifB-coを同時に捉え、まさに受け渡しの瞬間を凍結しました。彼らは、NifXが尾部でNifENに固定されつつ主要部分は柔軟性を保ち、荷を揺り動かして所定の位置に運ぶことができることを発見しました。
受け渡しを原子レベルで見る
画像は、まずNifB-coがNifENの外面にドッキングし、NifEサブユニットの先端にある二つの硫黄含有アミノ酸がクラスターの両端をつかむことを明らかにしました。特別な「移送」状態では、クラスターの一端がNifXのヒスチジンによって保持され、もう一端がNifEに捕らえられています。これにより、荷が文字通り運搬人と足場の間で共有される短い瞬間が生じ、環境への露出を最小限に抑えつつ安全かつ直接的に渡されます。窒素固定細菌Azotobacter vinelandiiの変異株を用いた生化学的試験では、NifEのこのN末端把持ループを除去すると、特にNifB-coが不足している状況で細胞が窒素ガスのみで成長するのに苦労することが示され、このドッキング部位が効率的な補因子生成に不可欠であることが裏付けられました。
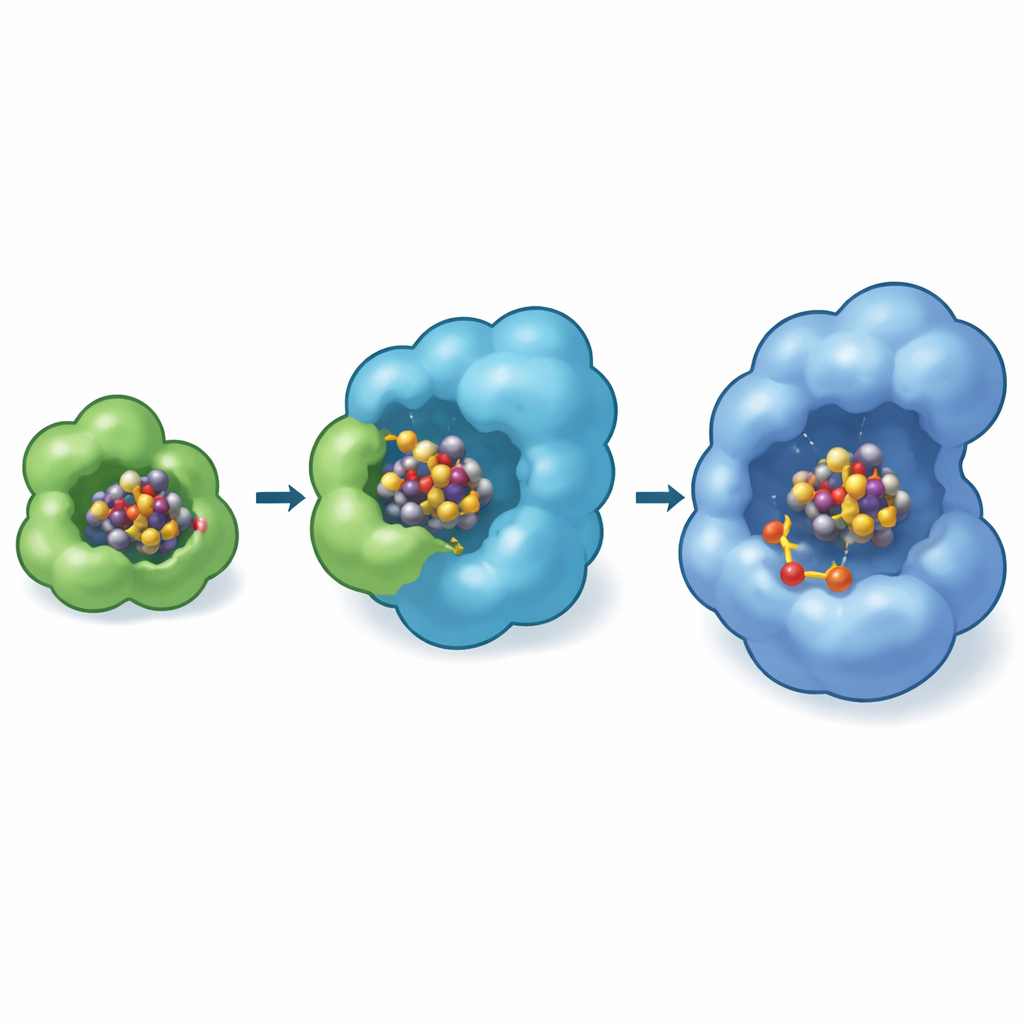
足場タンパク質の中に隠れた作業場
興味深いことに、実験で観察されたNifEN上のドッキング部位はタンパク質表面近くに位置する一方で、完成した窒素還元酵素内では成熟したFeMo補因子は深い空洞の内部に座しています。このギャップをつなぐために、著者らは高度なコンピューターモデル(Boltz-2)を用いてクラスターの次の移動先を予測しました。シミュレーションは繰り返し、NifB-coがNifENの内部ポケット、補因子形成に必須と知られる特定のシステイン残基の近くに配置されると示しました。モデルはさらに、この内側ポケットがモリブデンとホモシトレートがクラスターに付加されてNifB-coが完全なFeMo補因子に変わる場所であることを示唆しました。同じモデリングの枠組みでは、NifXは実験構造と一致する正に帯電したポケットに荷を結合し、所定の経路—NifX → NifEの表面受容部位 → 内部変換室—の考えを強めています。
この見えない舞踏が重要な理由
構造のスナップショットとシミュレーションを合わせると、窒素還元酵素の心臓部を作るための振付けられた一連の工程が描かれます:まず高コストの金属クラスターが作られ、運搬体から足場へと渡され、内部室へ移動され、そこでモリブデンとホモシトレートで改良されてから最終酵素へ渡されます。一般読者にとっての主要なメッセージは、生命は貴重な化学部品の管理に多大な注意を払っており、専門化したタンパク質の連鎖を用いてそれらを保護し精製しているということです。この分子リレーの働きを明らかにすることで、本研究は土壌の肥沃度と世界の食料生産を支える生物学的窒素固定の理解に重要な一片を加え、いつか肥料をよりクリーンで持続可能な方法で作ることを刺激するかもしれません。
引用: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
キーワード: 窒素固定, 窒素還元酵素, 金属補因子, クライオ電子顕微鏡法, 酵素の組立