Clear Sky Science · nl
Transport van een nitrogenase FeMo-cofactor assembleerintermediair
Hoe microben helpen de wereld te voeden
Stikstof is een basisingrediënt van DNA en eiwitten, maar de meeste levende wezens kunnen het enorme reservoir van stikstofgas in de lucht niet gebruiken. In plaats daarvan zijn ze afhankelijk van gespecialiseerde microben die dit gas omzetten in vormen die planten kunnen opnemen, en zo stilletjes de wereldwijde landbouw en natuurlijke ecosystemen ondersteunen. Dit artikel werpt een blik op een van de meest ingewikkelde moleculaire machines achter dat trucje en stelt een eenvoudige vraag: hoe bouwen cellen het kleine metaalcluster in het hart van het stikstoffixerende enzym zorgvuldig op en geven het door zonder het onderweg te laten vallen?
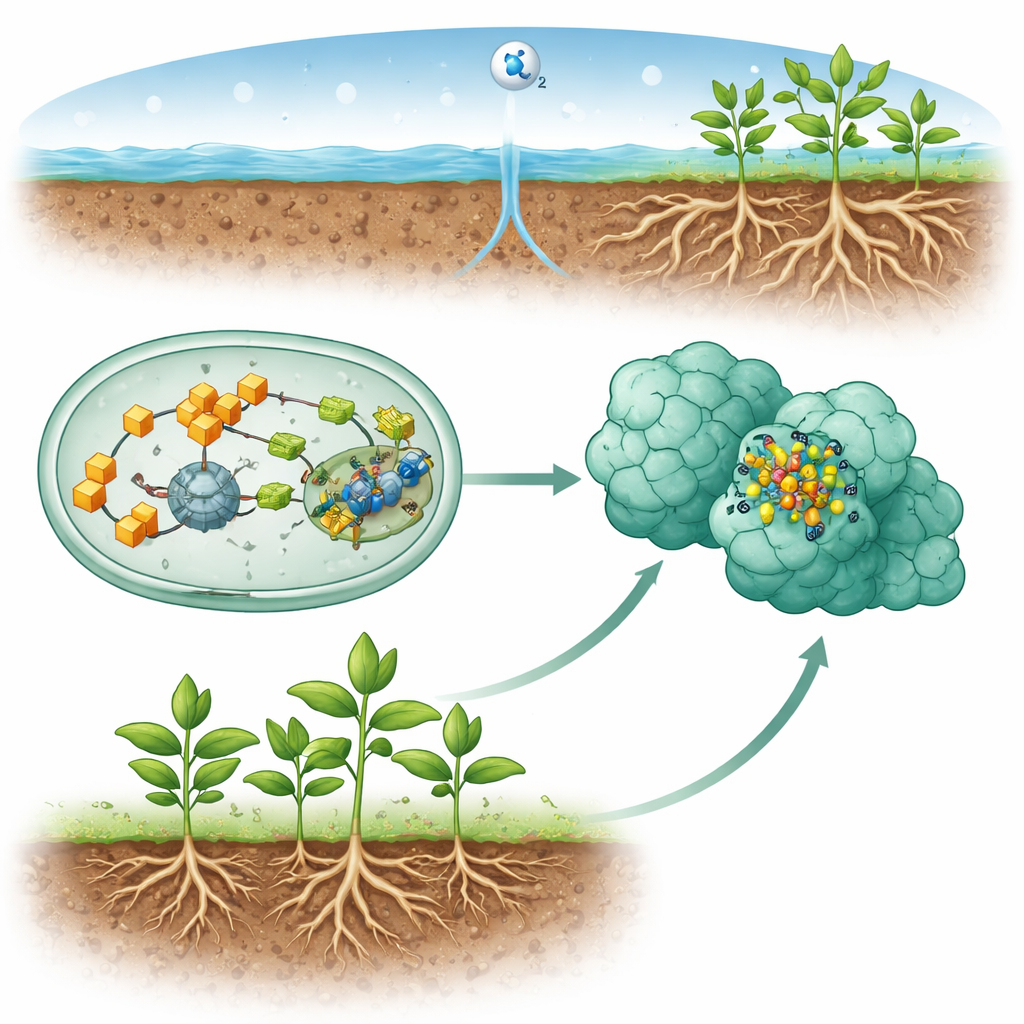
Het kleine motortje in stikstoffixerende bacteriën
Veel bodembacteriën en aquatische microben gebruiken een enzym dat nitrogenase heet om stikstofgas om te zetten in ammoniak, die planten vervolgens als meststof gebruiken. De meest voorkomende versie van dit enzym is afhankelijk van een complex metaalcluster dat het FeMo-cofactor wordt genoemd, opgebouwd uit ijzer, zwavel, koolstof, molybdeen en een organische zijketen bekend als homocitraat. Deze cofactor assembleert niet vanzelf binnen het voltooide enzym. In plaats daarvan bouwen cellen het stap voor stap op hulp-eiwitten en leveren het vervolgens af in de werkplaats van de nitrogenase. Begrijpen hoe deze assemblagelijn werkt is cruciaal, niet alleen voor fundamentele biologie maar ook voor langetermijndoelen zoals het ontwerpen van gewassen of industriële systemen die stikstof efficiënter en met minder energie kunnen fixeren dan de huidige productiemethodes voor kunstmest.
Een moleculaire estafette voor fragiele lading
De studie richt zich op een belangrijke late stap in deze assemblagelijn. In dit stadium heeft een ander enzym, NifB, al een groot ijzer–zwavelcluster gesmeed dat NifB-co wordt genoemd. Dit fragiele cluster moet verplaatst worden naar een stellage-eiwitpaar, NifEN, waar het wordt omgezet in de uiteindelijke FeMo-cofactor. Een klein drager-eiwit, NifX, fungeert als koerier die NifB-co oppikt op de plaats van ontstaan en naar NifEN brengt. Met behulp van hoge-resolutie cryo-elektronenmicroscopie legden de auteurs NifEN vast samen met NifX en NifB-co, waardoor de overdracht als het ware in beweging werd bevroren. Ze vonden dat NifX met zijn staart aan NifEN is verankerd maar zijn hoofdlichaam flexibel houdt, waardoor het zijn lading in positie kan zwaaien.
De overdracht in atomaire details zien
De beelden tonen dat NifB-co eerst aan de buitenkant van NifEN aankoppelt, waar twee zwavelhoudende aminozuren aan het begin van de NifE-subunit het cluster aan tegenovergestelde uiteinden vastgrijpen. In een speciale “transfer”-toestand wordt het ene uiteinde van het cluster nog steeds vastgehouden door een histidine op NifX terwijl het andere uiteinde door NifE wordt gevangen. Dit creëert een kort moment waarin de lading letterlijk gedeeld wordt tussen koerier en stellage, wat een veilige, directe overdracht garandeert en de blootstelling aan de omgeving minimaliseert. Biochemische tests met gemuteerde stammen van de stikstoffixerende bacterie Azotobacter vinelandii toonden aan dat wanneer deze N-terminale grijpende lus op NifE wordt verwijderd, de cellen moeite hebben op stikstofgas alleen te groeien, vooral wanneer NifB-co schaars is, wat onderstreept hoe essentieel deze aankoppelplaats is voor efficiënte cofactorproductie.
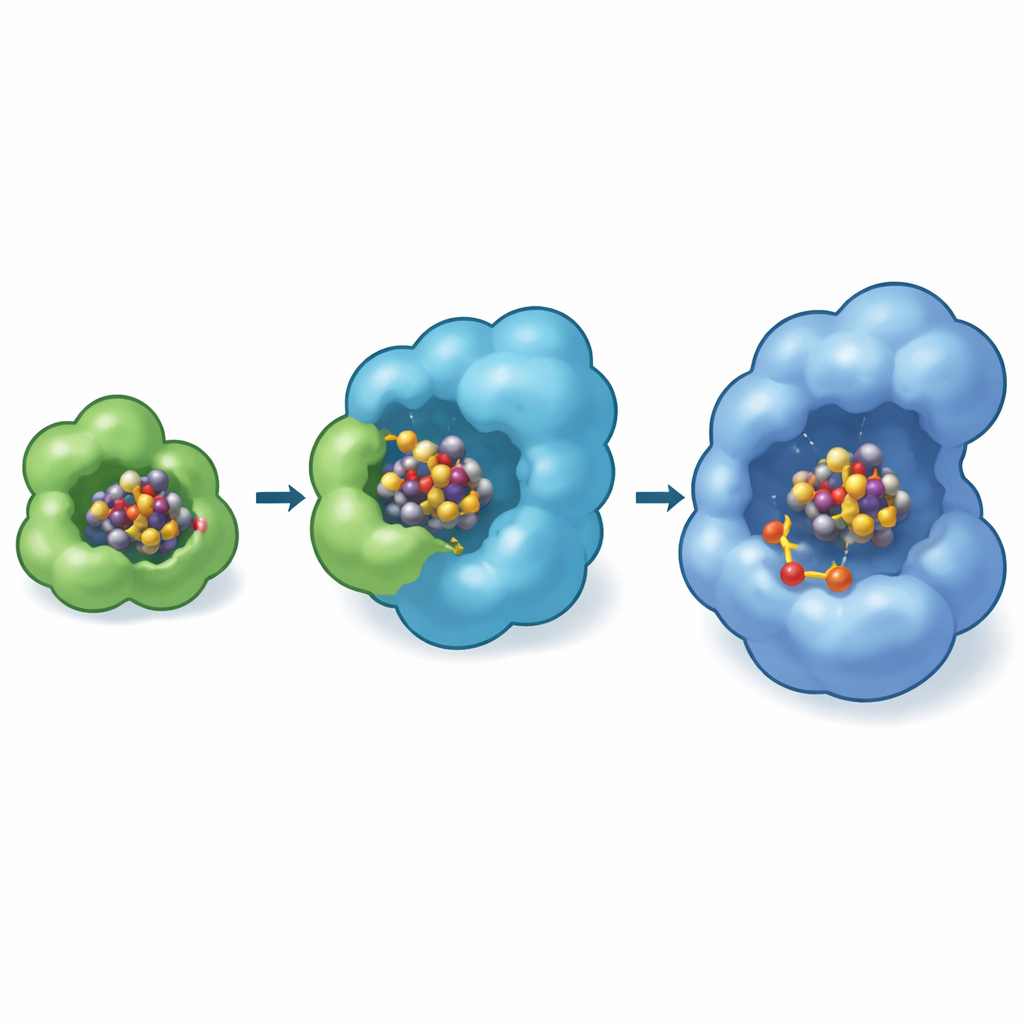
Een verborgen werkplaats binnen de stellage
Vreemd genoeg bevindt de experimenteel waargenomen aankoppelplaats op NifEN zich dicht bij het eiwitoppervlak, terwijl in het voltooide nitrogenase-enzym de rijpe FeMo-cofactor diep binnenin een holte zit. Om deze kloof te overbruggen gebruikten de auteurs geavanceerde computermodellen (Boltz-2) om te voorspellen waar het cluster daarna naartoe zou kunnen bewegen. Deze simulaties plaatsten NifB-co herhaaldelijk in een interne pocket van NifEN nabij een specifiek cysteïne-residu dat bekend staat als essentieel voor cofactorvorming. De modellen suggereerden verder dat deze binnenste pocket de plaats is waar molybdeen en homocitraat aan het cluster worden toegevoegd, waardoor NifB-co verandert in de complete FeMo-cofactor. Binnen hetzelfde modelleringskader bindt NifX zijn lading in een positief geladen pocket die overeenkomt met de experimentele structuur, wat het idee versterkt van een gedefinieerde route: NifX → oppervlakkige ontvangstplaats op NifE → interne conversiekamer.
Waarom deze onzichtbare dans ertoe doet
Gezamenlijk schetsen de structurele snapshots en simulaties een gechoreografeerde volgorde voor het bouwen van het hart van de nitrogenase: een kostbaar metaalcluster wordt gemaakt, van drager naar stellage doorgegeven, verplaatst naar een binnenkamer en pas daarna opgewaardeerd met molybdeen en homocitraat voordat het naar het uiteindelijke enzym wordt overgedragen. Voor een algemeen publiek is de kernboodschap dat het leven grote zorg besteedt aan het omgaan met waardevolle chemische onderdelen, door een keten van gespecialiseerde eiwitten te gebruiken om ze te beschermen en te verfijnen. Door te verduidelijken hoe deze moleculaire estafette werkt, voegt de studie een belangrijk stuk toe aan ons begrip van biologische stikstoffixatie, een proces dat de bodemvruchtbaarheid en voedselproductie wereldwijd ondersteunt en mogelijk op een dag schonere, duurzamere manieren kan inspireren om meststof te maken.
Bronvermelding: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
Trefwoorden: stikstoffixatie, nitrogenase, metaalkofactoren, cryo-electron microscopy</keyword=kryo-elektronenmicroscopie> <keyword>enzymassemblage