Clear Sky Science · es
Tráfico de un intermedio en el ensamblaje del FeMo-cofactor de la nitrogenasa
Cómo los microbios ayudan a alimentar al mundo
El nitrógeno es un ingrediente básico del ADN y las proteínas, sin embargo la mayor parte de los seres vivos no puede aprovechar el enorme depósito de gas nitrógeno en el aire. En su lugar, dependen de microbios especializados que convierten ese gas en formas que las plantas pueden asimilar, sosteniendo en silencio la agricultura global y los ecosistemas naturales. Este artículo se adentra en una de las máquinas moleculares más intrincadas detrás de ese truco y plantea una pregunta sencilla: ¿cómo construyen y transfieren las células con cuidado el pequeño clúster metálico en el corazón de la enzima que fija nitrógeno sin perderlo en el camino?
El pequeño motor dentro de las bacterias fijadoras de nitrógeno
Muchos microbios del suelo y acuáticos usan una enzima llamada nitrogenasa para convertir el gas nitrógeno en amoníaco, que las plantas emplean luego como fertilizante. La versión más común de esta enzima depende de un complejo clúster metálico llamado FeMo-cofactor, compuesto de hierro, azufre, carbono, molibdeno y un componente orgánico conocido como homocitrato. Este cofactor no se ensambla por sí solo dentro de la enzima terminada. En vez de eso, las células lo construyen paso a paso sobre proteínas auxiliares y luego lo transportan al sitio activo de la nitrogenasa. Entender cómo funciona esta cadena de montaje es crucial no solo para la biología básica, sino también para objetivos a largo plazo como diseñar cultivos o sistemas industriales que fijen nitrógeno de forma más eficiente y con menos energía que la producción actual de fertilizantes.
Un relevo molecular para una carga frágil
El estudio se centra en un paso tardío clave de esta cadena de montaje. En esta etapa, otra enzima, NifB, ya ha forjado un gran clúster hierro–azufre llamado NifB-co. Este clúster frágil debe trasladarse a un par de proteínas andamiaje, NifEN, donde será convertido en el FeMo-cofactor final. Una pequeña proteína portadora, NifX, actúa como mensajera que recoge NifB-co de su lugar de origen y lo lleva a NifEN. Empleando criomicroscopía electrónica de alta resolución, los autores capturaron a NifEN junto con NifX y NifB-co, congelando efectivamente la transferencia en plena ejecución. Descubrieron que NifX está anclada a NifEN por su cola pero mantiene su estructura principal flexible, lo que le permite balancear su carga hasta situarla en posición.
Ver la entrega con detalle atómico
Las imágenes revelan que NifB-co primero se acopla en la superficie externa de NifEN, donde dos aminoácidos que contienen azufre al comienzo de la subunidad NifE sujetan el clúster por extremos opuestos. En un estado especial de “transferencia”, un extremo del clúster todavía está retenido por una histidina en NifX mientras el otro es capturado por NifE. Esto crea un breve momento en el que la carga se comparte literalmente entre la mensajera y el andamiaje, asegurando un pase directo y seguro que minimiza la exposición al entorno. Pruebas bioquímicas con cepas mutantes de la bacteria fijadora de nitrógeno Azotobacter vinelandii mostraron que cuando se elimina este lazo de agarre N-terminal en NifE, las células tienen dificultades para crecer solo con gas nitrógeno, especialmente cuando NifB-co es escaso, subrayando lo vital que es este sitio de acoplamiento para la producción eficiente del cofactor.
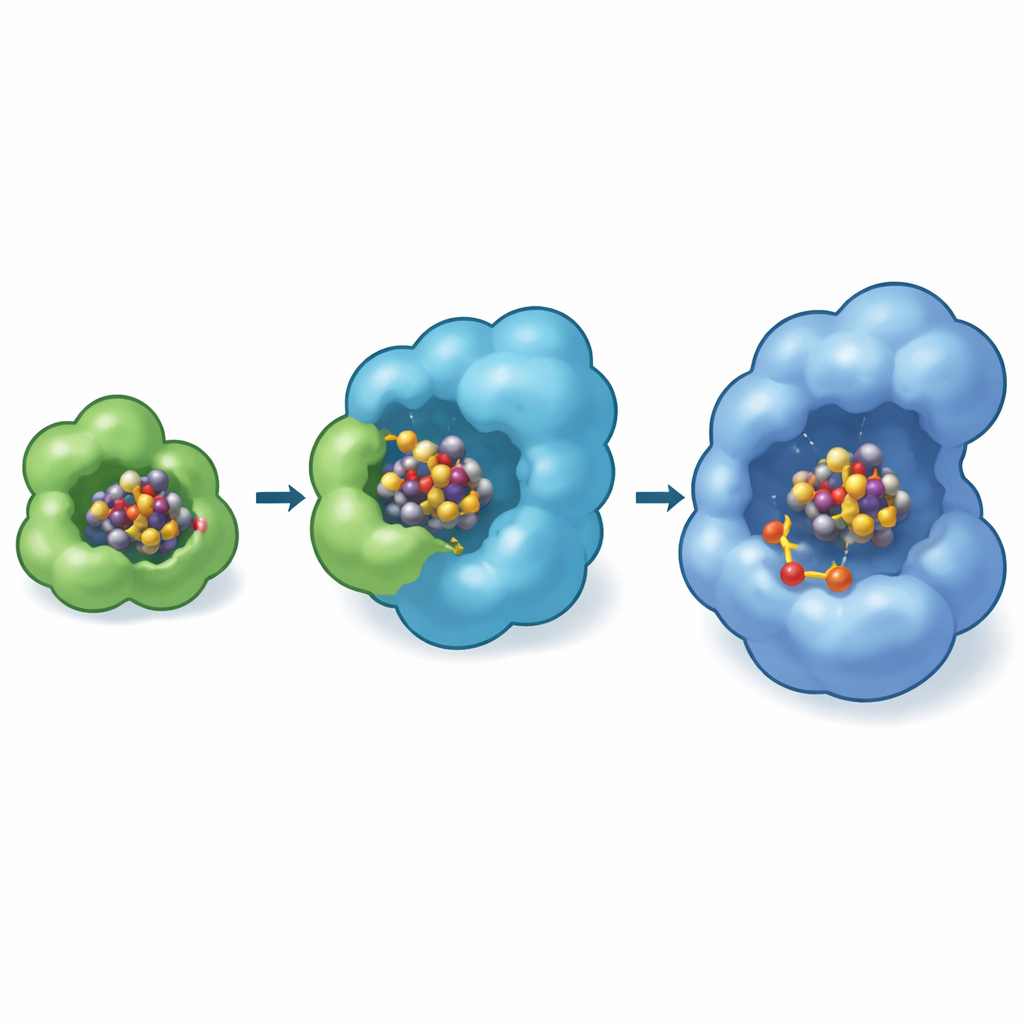
Un taller oculto dentro del andamiaje
Curiosamente, el sitio de acoplamiento observado experimentalmente en NifEN se sitúa cerca de la superficie de la proteína, mientras que en la nitrogenasa terminada el FeMo-cofactor maduro se encuentra profundamente dentro de una cavidad. Para salvar esa distancia, los autores usaron modelos computacionales avanzados (Boltz-2) para predecir hacia dónde podría moverse el clúster a continuación. Estas simulaciones colocaron repetidamente a NifB-co en un bolsillo interno de NifEN cerca de una cisteína específica que se sabe es esencial para la formación del cofactor. Los modelos sugirieron además que este bolsillo interior es donde se añaden el molibdeno y el homocitrato al clúster, transformando NifB-co en el FeMo-cofactor completo. En el mismo marco de modelado, NifX une su carga en un bolsillo cargado positivamente que coincide con la estructura experimental, reforzando la idea de una ruta definida: NifX → sitio receptor superficial en NifE → cámara interna de conversión.
Por qué importa esta danza invisible
En conjunto, las instantáneas estructurales y las simulaciones describen una secuencia coreografiada para construir el corazón de la nitrogenasa: un costoso clúster metálico se fabrica, se transfiere del portador al andamiaje, se traslada a una cámara interior y solo entonces se mejora con molibdeno y homocitrato antes de ser entregado a la enzima final. Para el lector general, el mensaje clave es que la vida invierte un gran cuidado en gestionar piezas químicas valiosas, usando una cadena de proteínas especializadas para protegerlas y refinarlas. Al aclarar cómo funciona este relevo molecular, el estudio añade una pieza importante a nuestra comprensión de la fijación biológica del nitrógeno, un proceso que sustenta la fertilidad del suelo y la producción de alimentos en todo el mundo y que puede algún día inspirar formas más limpias y sostenibles de fabricar fertilizantes.
Cita: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
Palabras clave: fijación de nitrógeno, nitrogenasa, cofactores metálicos, criomicroscopía electrónica, ensamblaje de enzimas