Clear Sky Science · ar
تهريب وسيط تجميع عامل مساعد FeMo لنيتروجينيز
كيف تساعد الميكروبات في إطعام العالم
النيتروجين مكوّن أساسي للحمض النووي والبروتينات، ومع ذلك فإن معظم الكائنات الحية لا تستطيع استخدام مخزون غاز النيتروجين الضخم في الهواء. بدلاً من ذلك، تعتمد الكائنات على ميكروبات متخصصة تحول هذا الغاز إلى أشكال يمكن للنباتات امتصاصها، فتدعم بذلك الزراعة والنظم البيئية الطبيعية بصمت. تقص هذه المقالة نظرة على إحدى أكثر الآلات الجزيئية تعقيدًا وراء تلك العملية وتطرح سؤالاً بسيطًا: كيف تبني الخلايا وتسلّم الكتلة المعدنية الصغيرة في قلب إنزيم تثبيت النيتروجين بعناية من دون إسقاطها خلال المسار؟
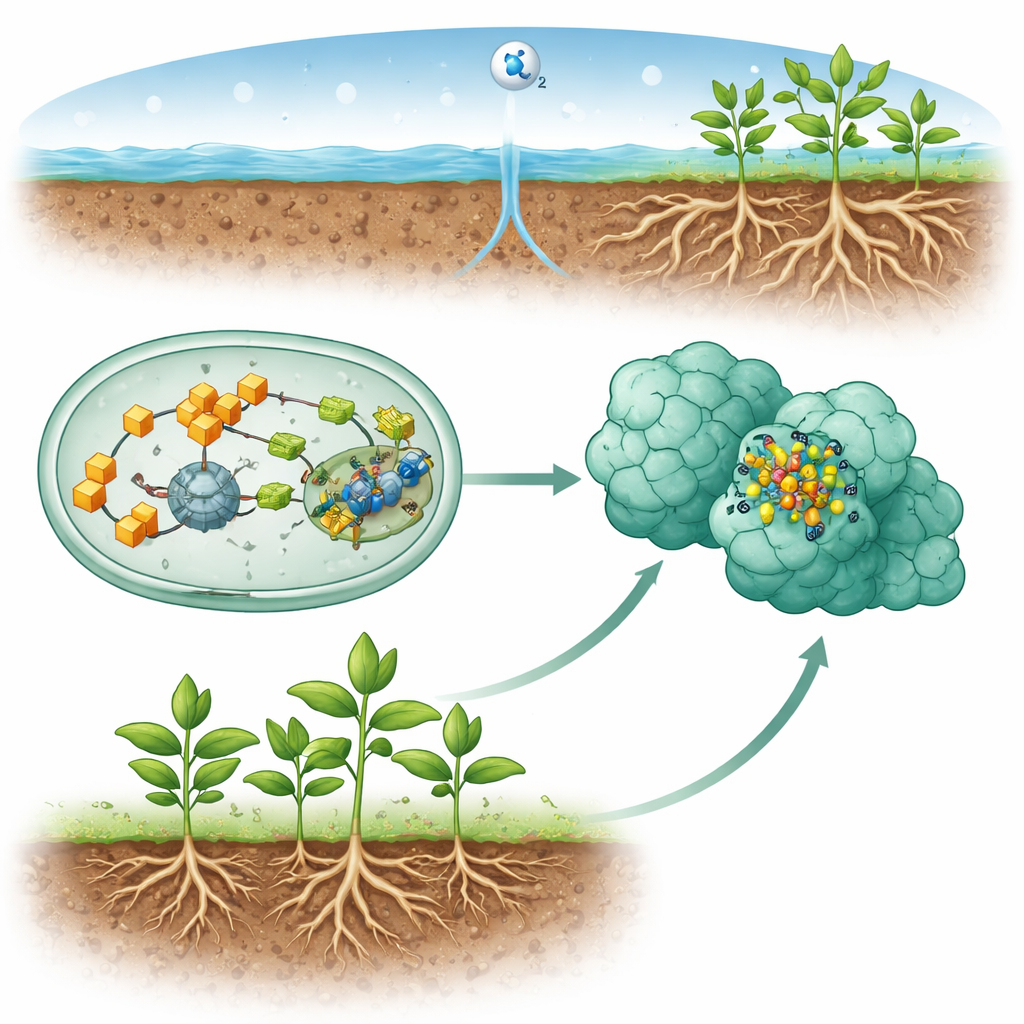
المحرك الصغير داخل بكتيريا مثبتة للنيتروجين
تستخدم العديد من الميكروبات الأرضية والمائية إنزيمًا يسمى النيتروجينيز لتحويل غاز النيتروجين إلى أمونيا، التي تستخدمها النباتات كأسمدة. الإصدار الأكثر شيوعًا من هذا الإنزيم يعتمد على مجموعة معدنية معقدة تسمى عامل FeMo المساعد، والمكوّن من حديد وكبريت وكربون والموليبدينوم وقطعة عضوية جانبية تعرف بالهوموسيتريت. هذا العامل المساعد لا يتجمع من تلقاء نفسه داخل الإنزيم النهائي؛ بل تقوم الخلايا ببنائه خطوة بخطوة على بروتينات مساعدة ثم تسلمه إلى موقع عمل النيتروجينيز. فهم كيفية عمل هذا الخطّ التجميعي أمر حاسم ليس فقط للبيولوجيا الأساسية بل أيضًا للأهداف بعيدة المدى مثل تصميم محاصيل أو أنظمة صناعية تثبت النيتروجين بكفاءة أعلى وبطاقة أقل من إنتاج الأسمدة الحالي.
تتابع جزيئي لحمولة هشة
يركز البحث على خطوة متأخرة رئيسية في هذا الخط التجميعي. في هذه المرحلة، يكون إنزيم آخر، NifB، قد شكّل بالفعل كتلة كبيرة من الحديد–الكبريت تُسمى NifB-co. يجب نقل هذه الكتلة الهشة إلى زوج من البروتينات الحاضنة، NifEN، حيث ستتحول إلى عامل FeMo المساعد النهائي. يعمل بروتين ناقل صغير، NifX، كرسول يلتقط NifB-co من موطنه ويحضره إلى NifEN. باستخدام المجهر الإلكتروني بالتبريد عالي الدقة، التقط المؤلفون NifEN مع NifX وNifB-co، مجمّدين بذلك عملية التسليم في منتصف الحركية. وجدوا أن NifX مرسخ إلى NifEN بواسطة ذيله لكنه يحتفظ بجسمه الرئيسي مرنًا، مما يتيح له أن يتأرجح ويحرك حمولته إلى الموضع المطلوب.
رؤية التسليم بتفاصيل ذرية
تكشف الصور أن NifB-co يرتبط أولًا بسطح NifEN الخارجي، حيث تمسك حمضتان أمينيتان تحتويان على الكبريت عند بداية وحدة NifE بالكتلة من الأطراف المتقابلة. في حالة خاصة تُسمى «حالة النقل»، يبقى أحد أطراف الكتلة ممسوكًا بواسطة هيستيدين على NifX بينما يمسك NifE بالطرف الآخر. هذا يخلق لحظة وجيزة تُشارك فيها الحمولة حرفيًا بين الرسول والحاضنة، مما يضمن مرورًا مباشرًا وآمنًا يقلل تعرضها للبيئة. اختبارات بيوكيميائية باستخدام سلالات طفيلية مطفرة من البكتيريا المثبتة للنيتروجين Azotobacter vinelandii أظهرت أنه عندما تُزال حلقة القبض عند النهاية N- على NifE، تكافح الخلايا للنمو على غاز النيتروجين بمفرده، لا سيما عندما تكون NifB-co نادرة، مما يؤكد مدى أهمية موقع الارتكاز هذا لإنتاج العامل المساعد بكفاءة.
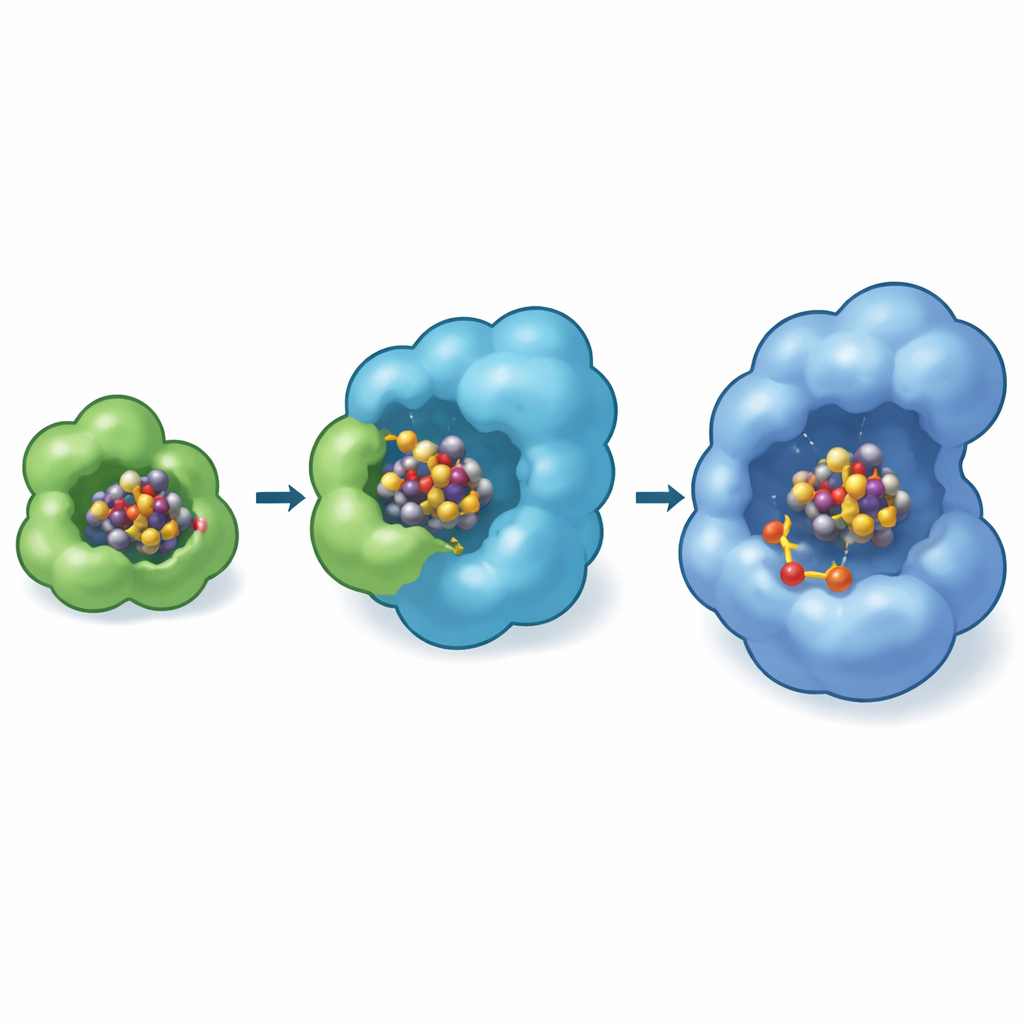
ورشة مخفية داخل الحاضنة
من الغريب أن موقع الارتكاز المرصود تجريبيًا على NifEN يقع بالقرب من سطح البروتين، بينما في إنزيم النيتروجينيز النهائي يجلس عامل FeMo الناضج عميقًا داخل تجويف. لسد هذه الفجوة، استخدم المؤلفون نماذج حاسوبية متقدمة (Boltz-2) للتنبؤ بالمكان الذي قد تتحرك إليه الكتلة بعد ذلك. وضعت هذه المحاكاة مرارًا NifB-co في جيب داخلي لـNifEN قرب حمض أميني سيستئين محدد يُعرف بأنه أساسي لتكوين العامل المساعد. كما أشارت النماذج إلى أن هذا الجيب الداخلي هو المكان الذي يُضاف فيه الموليبدينوم والهوموسيتريت إلى الكتلة، محوّلة NifB-co إلى عامل FeMo المساعد المكتمل. في إطار النمذجة نفسه، يرتبط NifX بحمولته في جيب موجب الشحنة يتطابق مع البنية التجريبية، معزّزًا فكرة وجود مسار محدد: NifX → موقع استقبال سطحي على NifE → حجرة تحويل داخلية.
لماذا تهم هذه الرقصة غير المرئية
معًا، تحدد اللقطات الهيكلية والمحاكاة تسلسلًا منسقًا لبناء قلب النيتروجينيز: تُصنَع كتلة معدنية مكلفة، تُمرّر من الناقل إلى الحاضنة، تُنقل إلى حجرة داخلية، وفقط بعد ذلك تُرقّى بإضافة الموليبدينوم والهوموسيتريت قبل أن تُسَلَّم إلى الإنزيم النهائي. للقراء العامين، الرسالة الأساسية أن الحياة تستثمر عناية كبيرة في إدارة أجزاء كيميائية ثمينة، مستخدمة سلسلة من البروتينات المتخصصة لحمايتها وصقلها. من خلال توضيح كيفية عمل هذا التتابع الجزيئي، تضيف الدراسة قطعة مهمة لفهمنا لتثبيت النيتروجين البيولوجي، العملية التي تقوم عليها خصوبة التربة وإنتاج الغذاء في العالم وقد تُلهم يومًا طرقًا أنظف وأكثر استدامة لصنع الأسمدة.
الاستشهاد: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
الكلمات المفتاحية: تثبيت النيتروجين, النيتروجينيز, العوامل المساعدة المعدنية, المجهر الإلكتروني بالتبريد, تركيب الإنزيمات