Clear Sky Science · ru
Транспортировка промежуточного комплекса сборки FeMo-кофактора нитрогеназы
Как микроорганизмы помогают питать мир
Азот — базовый компонент ДНК и белков, однако большинство живых существ не могут воспользоваться огромным резервуаром молекулярного азота в воздухе. Вместо этого они зависят от специализированных микробов, которые превращают этот газ в формы, усваиваемые растениями, тихо поддерживая мировое сельское хозяйство и природные экосистемы. В этой статье рассматривается один из самых сложных молекулярных аппаратов, ответственных за этот трюк, и задаётся простой вопрос: как клетки аккуратно собирают и передают крошечный металлический кластер в центре нитрогеназы, не уронив его по пути?
Крошечный двигатель внутри азотфиксирующих бактерий
Многие почвенные и водные микроорганизмы используют фермент нитрогеназу, чтобы превращать молекулярный азот в аммиак, который затем служит удобрением для растений. Наиболее распространённая версия этого фермента опирается на сложный металлический кластер FeMo-кофактор, собранный из железа, серы, углерода, молибдена и органической боковой группы, известной как гомоцитрат. Этот кофактор не собирается внутри уже зрелого фермента сам по себе. Клетки конструируют его поэтапно на вспомогательных белках, а затем доставляют в рабочее место нитрогеназы. Понимание того, как действует эта «сборочная линия», важно не только для фундаментальной биологии, но и для долгосрочных задач — например, разработки культур или промышленных систем, которые могли бы фиксировать азот эффективнее и с меньшими энергозатратами, чем современные методы производства удобрений.
Молекулярная эстафета для хрупкого груза
Исследование сосредоточено на ключевом позднем шаге этой сборки. На этой стадии другой фермент, NifB, уже сформировал крупный железо–серный кластер, называемый NifB-co. Этот хрупкий кластер необходимо переместить на парный каркасный белок NifEN, где он будет преобразован в окончательный FeMo-кофактор. Небольшой переносчик NifX действует как курьер: он забирает NifB-co с места его образования и приносит к NifEN. С помощью высокоразрешающей крио‑электронной микроскопии авторы поймали NifEN вместе с NifX и NifB-co, фактически зафиксировав момент передачи. Они обнаружили, что NifX прикрепляется к NifEN хвостом, но сохраняет гибкость основной части, что позволяет ему раскачивать груз в нужное положение.
Наблюдая передачу в атомных деталях
Снимки показывают, что NifB-co сначала швартуется на внешней поверхности NifEN, где две серосодержащие аминокислоты на начале субъединицы NifE захватывают кластер с противоположных концов. В специальном «переходном» состоянии один конец кластера всё ещё удерживается гистидином на NifX, в то время как другой захвачен NifE. Это создаёт краткий момент, когда груз буквально разделён между курьером и каркасом, обеспечивая безопасную прямую передачу и минимизируя экспозицию кластера окружающей среде. Биохимические тесты с мутантными штаммами азотфиксирующей бактерии Azotobacter vinelandii показали, что при удалении этого N‑концевого захватного петлевого участка на NifE клетки испытывают трудности с ростом на молекулярном азоте, особенно когда NifB-co в дефиците, что подчёркивает жизненную важность этой точки швартовки для эффективного производства кофактора.
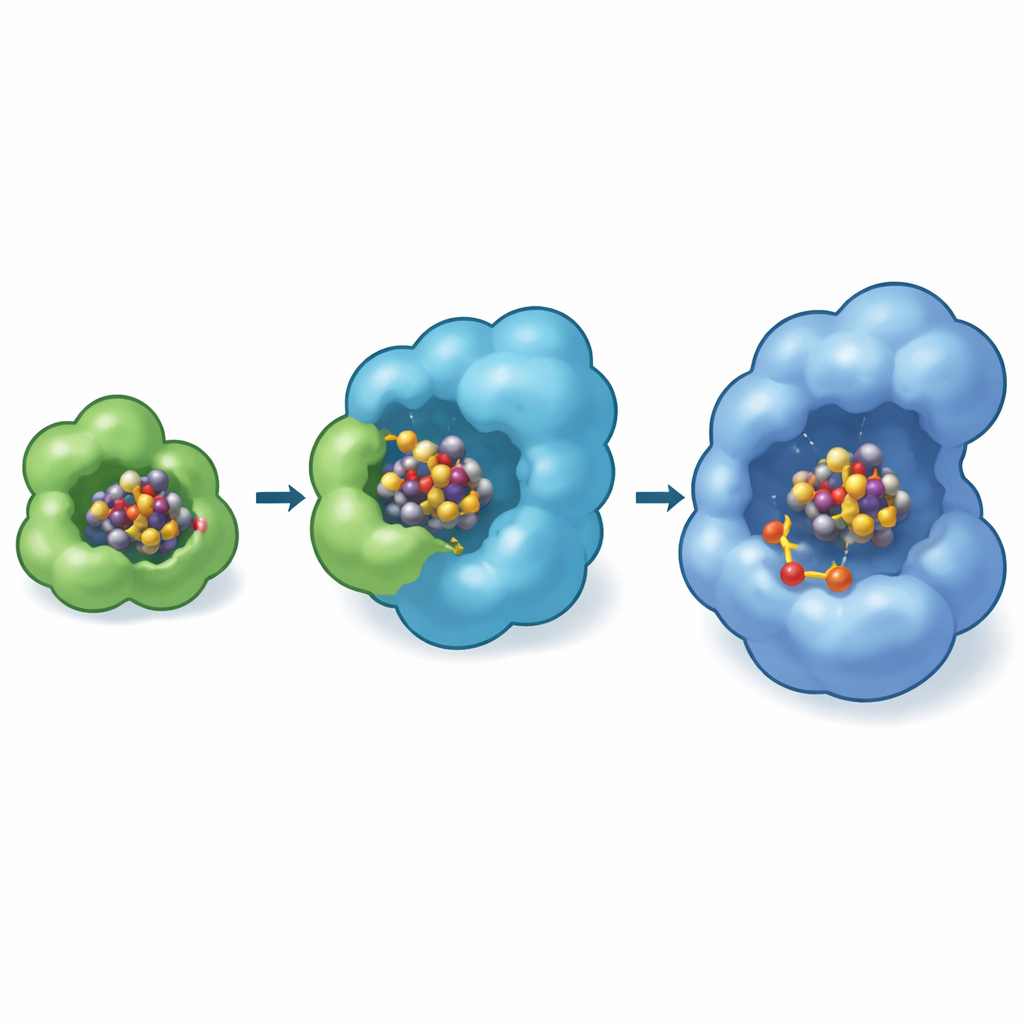
Скрытая мастерская внутри каркаса
Любопытно, что экспериментально наблюдаемое место швартовки на NifEN располагается близко к поверхности белка, тогда как в готовой нитрогеназе зрелый FeMo-кофактор сидит глубоко внутри полости. Чтобы преодолеть этот разрыв, авторы использовали продвинутые компьютерные модели (Boltz-2) для предсказания дальнейшей траектории перемещения кластера. Эти симуляции последовательно помещали NifB-co во внутренний карман NifEN рядом с определённым цистеиновым остатком, который известен как крайне важный для формирования кофактора. Модели также предположили, что именно в этой внутренней полости происходит добавление молибдена и гомоцитрата к кластеру, превращая NifB-co в полноценный FeMo-кофактор. В той же модели NifX удерживает свой груз в положительно заряженном кармане, соответствующем экспериментальной структуре, что укрепляет идею о чётко заданном маршруте: NifX → приёмная поверхность на NifE → внутренняя камера для преобразования.
Почему этот невидимый танец важен
В совокупности структурные «снимки» и моделирование очерчивают отрепетированную последовательность сборки сердца нитрогеназы: дорогостоящий металлический кластер создаётся, передаётся от переносчика к каркасу, перемещается в внутреннюю камеру и только затем дополняется молибденом и гомоцитратом перед передачей в конечный фермент. Для широкого читателя ключевая мысль в том, что жизнь тщательно управляет ценными химическими компонентами, используя цепочку специализированных белков для их защиты и «доработки». Уточняя, как работает эта молекулярная эстафета, исследование вносит важный вклад в наше понимание биологической фиксации азота — процесса, который поддерживает плодородие почв и производство продуктов питания во всём мире и однажды может вдохновить создание более чистых и устойчивых способов производства удобрений.
Цитирование: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
Ключевые слова: фиксация азота, нитрогеназа, металлические кофакторы, криоэлектронная микроскопия, сборка ферментов