Clear Sky Science · pt
Tráfego de um intermediário de montagem do co-fator FeMo da nitrogenase
Como os Micróbios Ajudam a Alimentar o Mundo
O nitrogênio é um ingrediente básico do DNA e das proteínas, porém a maioria dos seres vivos não consegue usar o enorme reservatório de gás nitrogênio na atmosfera. Em vez disso, dependem de micróbios especializados que convertem esse gás em formas que as plantas podem assimilar, sustentando em silêncio a agricultura global e os ecossistemas naturais. Este artigo examina uma das máquinas moleculares mais intrincadas por trás desse truque e faz uma pergunta simples: como as células constroem com cuidado e transferem o minúsculo aglomerado metálico no coração da enzima fixadora de nitrogênio sem deixá-lo cair pelo caminho?
O Pequeno Motor Dentro das Bactérias Fixadoras de Nitrogênio
Muitos micróbios do solo e aquáticos usam uma enzima chamada nitrogenase para converter gás nitrogênio em amônia, que as plantas então utilizam como fertilizante. A versão mais comum dessa enzima depende de um complexo de metais chamado co-fator FeMo, construído a partir de ferro, enxofre, carbono, molibdênio e um pedaço orgânico conhecido como homocitrato. Esse co-fator não se monta sozinho dentro da enzima pronta. Em vez disso, as células o constroem passo a passo sobre proteínas auxiliares e então o entregam ao sítio ativo da nitrogenase. Entender como essa linha de montagem funciona é crucial não apenas para a biologia básica, mas também para objetivos de longo prazo, como projetar culturas ou sistemas industriais que fixem nitrogênio de forma mais eficiente e com menos energia do que a produção de fertilizantes atual.
Um Revezamento Molecular para uma Carga Frágil
O estudo foca numa etapa tardia e chave dessa linha de montagem. Nesta fase, outra enzima, NifB, já formou um grande aglomerado ferro-enxofre chamado NifB-co. Esse aglomerado frágil deve ser movido para um par de proteínas andaimes, NifEN, onde será convertido no co-fator FeMo final. Uma pequena proteína carreadora, NifX, atua como um mensageiro que pega o NifB-co em sua origem e o leva até o NifEN. Usando crio–microscopia eletrônica de alta resolução, os autores capturaram NifEN junto com NifX e NifB-co, efetivamente congelando a passagem em pleno movimento. Eles descobriram que NifX está ancorada ao NifEN por sua cauda, mas mantém seu corpo principal flexível, permitindo que balance a carga para colocá-la na posição correta.
Vendo a Passagem em Detalhe Atômico
As imagens revelam que o NifB-co primeiro acopla-se à superfície externa do NifEN, onde dois aminoácidos contendo enxofre no começo da subunidade NifE seguram o aglomerado nas extremidades opostas. Em um estado especial de “transferência”, uma extremidade do aglomerado ainda é mantida por uma histidina no NifX enquanto a outra é capturada pelo NifE. Isso cria um breve momento em que a carga é literalmente compartilhada entre o mensageiro e o andaime, garantindo uma passagem segura e direta que minimiza a exposição ao ambiente. Testes bioquímicos com cepas mutantes da bactéria fixadora de nitrogênio Azotobacter vinelandii mostraram que, quando esse laço de fixação N-terminal no NifE é removido, as células têm dificuldade para crescer usando apenas gás nitrogênio, especialmente quando o NifB-co é escasso, ressaltando o quão vital esse sítio de acoplamento é para a produção eficiente do co-fator.
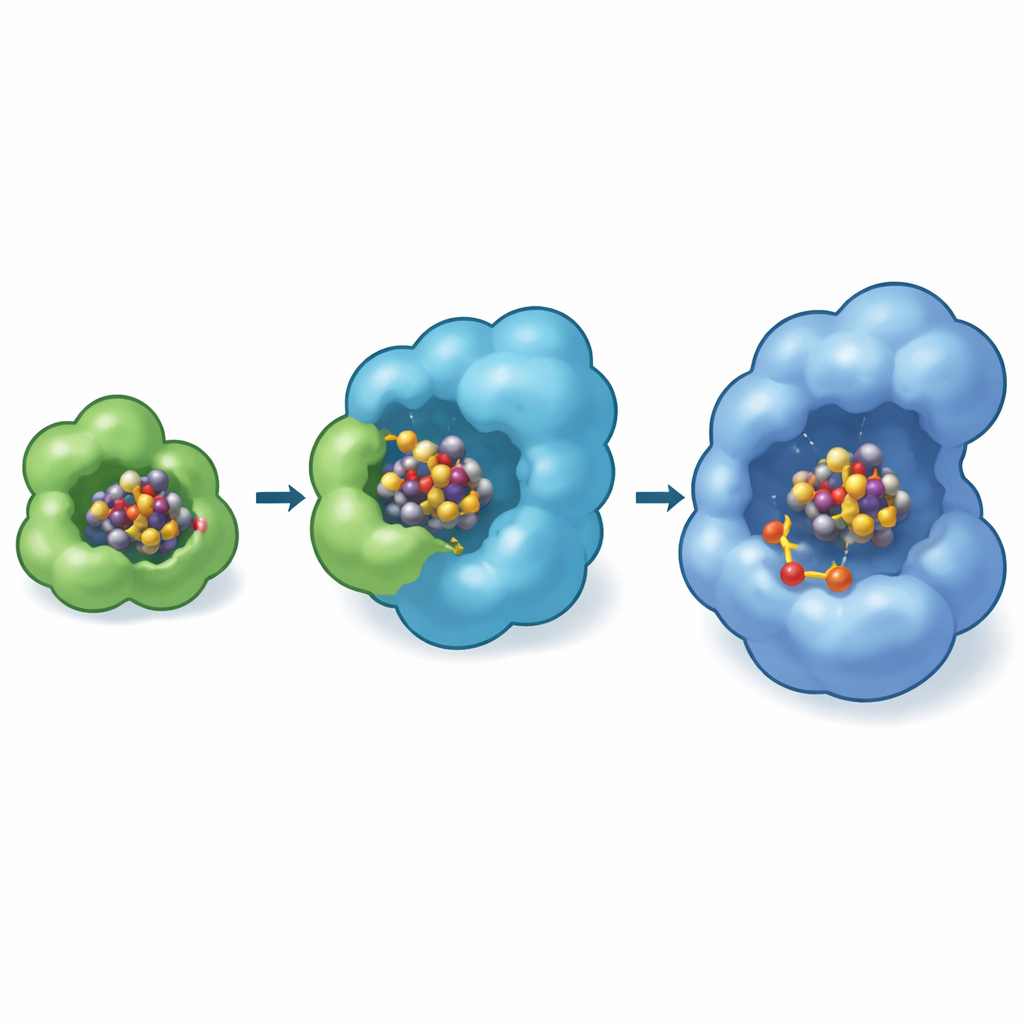
Uma Oficina Oculta Dentro do Andaime
Curiosamente, o sítio de acoplamento observado experimentalmente no NifEN fica próximo à superfície da proteína, enquanto na nitrogenase pronta o co-fator FeMo maduro situa-se profundamente dentro de uma cavidade. Para conectar esse trecho, os autores usaram modelos computacionais avançados (Boltz-2) para prever onde o aglomerado poderia se mover em seguida. Essas simulações repetidamente posicionaram o NifB-co em uma bolsa interna do NifEN próxima a um resíduo de cisteína específico que se sabe ser essencial para a formação do co-fator. Os modelos também sugeriram que essa câmara interna é onde o molibdênio e o homocitrato são adicionados ao aglomerado, transformando o NifB-co no co-fator FeMo completo. No mesmo arcabouço de modelagem, o NifX prende sua carga em um bolso carregado positivamente que corresponde à estrutura experimental, reforçando a ideia de uma rota definida: NifX → sítio receptor na superfície do NifE → câmara interna de conversão.
Por Que Essa Dança Invisível Importa
Juntas, as imagens estruturais e as simulações delineiam uma sequência coreografada para construir o coração da nitrogenase: um aglomerado metálico caro é produzido, passado do carregador para o andaime, movido para uma câmara interna e somente então atualizado com molibdênio e homocitrato antes de ser transferido para a enzima final. Para o leitor geral, a mensagem principal é que a vida investe grande zelo em gerenciar peças químicas preciosas, usando uma cadeia de proteínas especializadas para protegê-las e refiná-las. Ao clarificar como esse revezamento molecular funciona, o estudo adiciona uma peça importante ao nosso entendimento da fixação biológica do nitrogênio, um processo que fundamenta a fertilidade do solo e a produção de alimentos no mundo e que pode um dia inspirar maneiras mais limpas e sustentáveis de fabricar fertilizantes.
Citação: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
Palavras-chave: fixação de nitrogênio, nitrogenase, cofatores metálicos, crio-microscopia eletrônica, montagem de enzimas