Clear Sky Science · it
Traffico di un intermedio assemblativo del FeMo-cofattore della nitrogenasi
Come i microbi aiutano a nutrire il pianeta
L'azoto è un ingrediente fondamentale di DNA e proteine, eppure la maggior parte degli esseri viventi non può sfruttare il vasto serbatoio di azoto molecolare presente nell'aria. Dipendono invece da microbi specializzati che trasformano questo gas in forme assimilabili dalle piante, sostenendo silenziosamente l'agricoltura globale e gli ecosistemi naturali. Questo articolo osserva una delle macchine molecolari più complesse dietro questo processo e si pone una domanda semplice: come fanno le cellule a costruire con cura e a trasferire il minuscolo ammasso metallico al centro dell'enzima fissatore d'azoto senza farlo cadere lungo il percorso?
Il piccolo motore all'interno dei batteri fissatori d'azoto
Molti microbi del suolo e degli ambienti acquatici usano un enzima chiamato nitrogenasi per convertire l'azoto molecolare in ammoniaca, che le piante poi utilizzano come fertilizzante. La versione più comune di questo enzima si basa su un complesso ammasso metallico chiamato FeMo-cofattore, composto da ferro, zolfo, carbonio, molibdeno e una parte organica nota come omocitrato. Questo cofattore non si assemblA da solo all'interno dell'enzima finito. Le cellule lo costruiscono invece passo dopo passo su proteine ausiliarie e lo trasferiscono poi nel sito attivo della nitrogenasi. Capire come funziona questa catena di montaggio è cruciale non solo per la biologia di base ma anche per obiettivi a lungo termine, come progettare colture o sistemi industriali che fissino l'azoto in modo più efficiente e con meno energia rispetto alla produzione attuale di fertilizzanti.
Una staffetta molecolare per un carico fragile
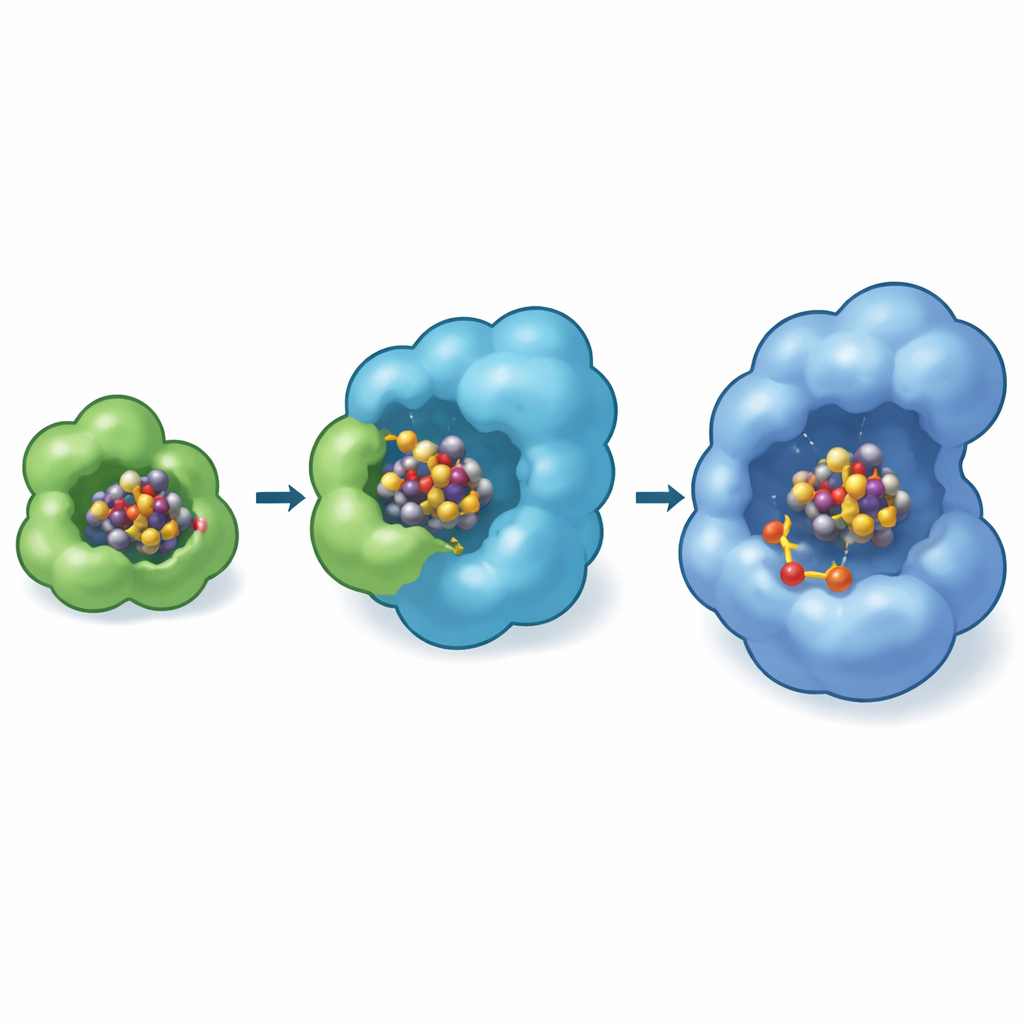
Lo studio si concentra su un passaggio tardivo chiave di questa linea di montaggio. In questa fase, un altro enzima, NifB, ha già forgiato un grande ammasso ferro–zolfo chiamato NifB-co. Questo ammasso fragile deve essere trasferito a una coppia di proteine impalcatura, NifEN, dove verrà convertito nel FeMo-cofattore finale. Una piccola proteina trasportatrice, NifX, funge da corriere che preleva NifB-co dal suo luogo di nascita e lo porta a NifEN. Utilizzando crio–microscopia elettronica ad alta risoluzione, gli autori hanno catturato NifEN insieme a NifX e NifB-co, congelando di fatto il passaggio a metà movimento. Hanno osservato che NifX è ancorata a NifEN tramite la sua coda ma mantiene il corpo principale flessibile, permettendole di oscillare e collocare il suo carico nella posizione corretta.
Vedere il passaggio in dettaglio atomico
Le immagini rivelano che NifB-co si ancora prima sulla superficie esterna di NifEN, dove due aminoacidi contenenti zolfo all'inizio della subunità NifE afferrano l'ammasso alle estremità opposte. In uno stato speciale di “trasferimento”, un'estremità dell'ammasso è ancora tenuta da un'istidina su NifX mentre l'altra è catturata da NifE. Questo crea un momento breve in cui il carico è letteralmente condiviso tra corriere e impalcatura, garantendo un passaggio diretto e sicuro che minimizza l'esposizione all'ambiente. Test biochimici su ceppi mutanti del batterio fissatore d'azoto Azotobacter vinelandii hanno mostrato che quando questo anello di presa N-terminale su NifE viene rimosso, le cellule faticano a crescere basandosi solo sull'azoto molecolare, specialmente quando NifB-co è scarso, sottolineando quanto sia vitale questo sito di ancoraggio per una produzione efficiente del cofattore.
Un laboratorio nascosto all'interno dell'impalcatura
Curiosamente, il sito di ancoraggio osservato sperimentalmente su NifEN si trova vicino alla superficie della proteina, mentre nell'enzima nitrogenasi maturo il FeMo-cofattore si trova in profondità all'interno di una cavità. Per colmare questa distanza, gli autori hanno utilizzato modelli computazionali avanzati (Boltz-2) per prevedere dove l'ammasso potrebbe spostarsi successivamente. Queste simulazioni hanno ripetutamente collocato NifB-co in una tasca interna di NifEN vicino a un residuo di cisteina specifico, noto per essere essenziale nella formazione del cofattore. I modelli hanno inoltre suggerito che questa tasca interna sia il luogo in cui molibdeno e omocitrato vengono aggiunti all'ammasso, trasformando NifB-co nel FeMo-cofattore completo. Nello stesso quadro modellistico, NifX lega il suo carico in una tasca carica positivamente che corrisponde alla struttura sperimentale, rafforzando l'idea di una rotta definita: NifX → sito ricevente sulla superficie di NifE → camera di conversione interna.
Perché questo ballo invisibile è importante
Messi insieme, gli istantanee strutturali e le simulazioni delineano una sequenza coreografata per costruire il cuore della nitrogenasi: un costoso ammasso metallico viene fabbricato, passato dal trasportatore all'impalcatura, spostato in una camera interna e solo allora aggiornato con molibdeno e omocitrato prima di essere consegnato all'enzima finale. Per il lettore generale, il messaggio chiave è che la vita investe grande cura nella gestione di parti chimiche preziose, usando una catena di proteine specializzate per proteggerle e affinarle. Chiarendo come funziona questa staffetta molecolare, lo studio aggiunge un tassello importante alla nostra comprensione della fissazione biologica dell'azoto, un processo che sostiene la fertilità del suolo e la produzione alimentare in tutto il mondo e che un giorno potrebbe ispirare modi più puliti e sostenibili di produrre fertilizzanti.
Citazione: Schneider, F.F., Martin del Campo, J.S., Zhang, L. et al. Trafficking of a nitrogenase FeMo-cofactor assembly intermediate. Nat Chem Biol 22, 822–828 (2026). https://doi.org/10.1038/s41589-026-02179-0
Parole chiave: fissazione dell'azoto, nitrogenasi, cofattori metallici, crio-microscopia elettronica, assemblaggio enzimatico