Clear Sky Science · sv
IL-1 avgränsar effektivitet och reaktogenicitet hos squalenbaserade adjuvanser på celltypsspecifikt sätt
Varför vaccin‑tillsatser spelar roll
Moderna vaccin behöver ofta en extra skjuts för att fungera optimalt, och den skjutsen kommer från ingredienser som kallas adjuvanser. Dessa hjälpämnen kan göra vacciner mycket mer skyddande, men de kan också ge ömma armar eller kortvarig feber. Denna studie granskar noggrant en mycket använd klass av oljebaserade adjuvanser och ställer en central fråga: kan vi behålla deras starka skydd samtidigt som vi minskar biverkningarna?
Oljedroppar som väcker immunsystemet
Forskarna fokuserade på squalenbaserade adjuvanser — små olja‑i‑vatten‑droppar som redan används i influensa‑ och covid‑19‑vacciner. Två av dessa, inklusive covid‑19‑adjuvansen A‑910823, innehåller en form av vitamin E kallad α‑tokoferol, vilket tidigare kopplats till starkare antikroppssvar men också till mer inflammation. Med ett covid‑19‑spikeproteinvaccin i möss jämförde teamet adjuvanser med och utan α‑tokoferol och undersökte den närliggande muskeln och dränerande lymfkörtlar, där immunsvar först organiseras. De fann att α‑tokoferol gjorde stor skillnad: det slog på många fler gener kopplade till inflammation och cellrörelse, särskilt i lymfkörtlarna.
Signalen IL‑1 i centrum
Bland alla genförändringar framträdde en väg särskilt tydligt — signalering driven av en familj molekyler som kallas IL‑1. Hos möss som gavs A‑910823 ökade både IL‑1α och IL‑1β kraftigt, men i olika celltyper. IL‑1α kom främst från eosinofiler, en typ av vita blodkroppar som ofta förknippas med allergi och astma. IL‑1β ökade däremot i flera myeloida celler, inklusive neutrofiler, monocyter och dendritiska celler. När forskarna tog bort α‑tokoferol från adjuvansen minskade särskilt IL‑1β markant. Liknande mönster framkom när de testade mänskligt godkända motsvarigheter till andra squalenadjuvanser, vilket visar att detta beteende är ett gemensamt kännetecken för oljemulsioner som innehåller α‑tokoferol. 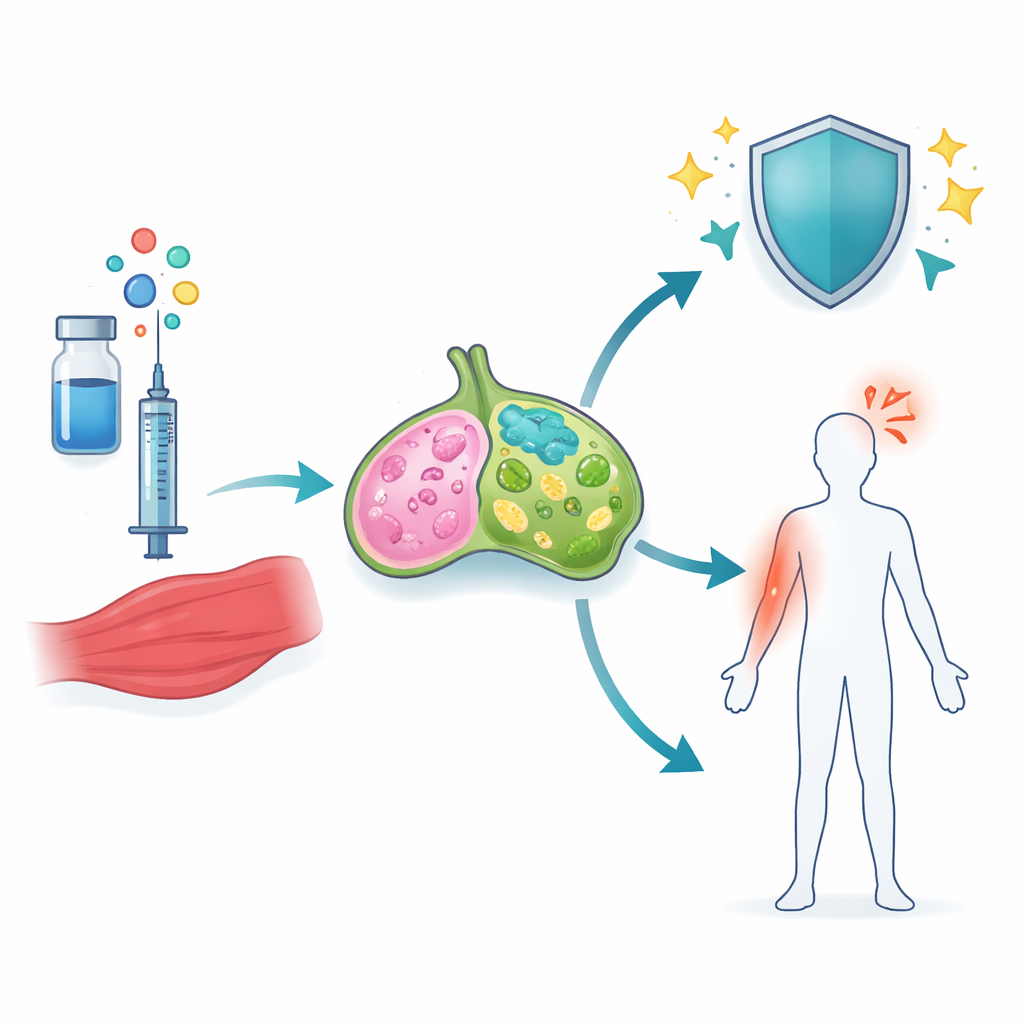
Att separera skydd från biverkningar
Teamet undersökte sedan hur dessa IL‑1‑signaler översätts till verkliga utfall: skyddande antikroppar och kortvariga reaktioner som svullnad och feber. Genom att använda möss som saknade specifika receptorer eller signalsubstanser, och genom att blockera IL‑1β, kartlade de skilda kretsar. Starka antikroppssvar och bildandet av specialiserade hjälpar‑T‑celler samt germinalcentra‑B‑celler drevs av en IL‑1β‑beroende väg via adaptorproteinet MyD88 i CD11c‑positiva celler såsom dendritiska celler. Lokal svullnad i armen berodde däremot främst på IL‑1α från eosinofiler nära injektionsstället. Systemisk feber följde ännu en annan väg: IL‑1β utlöste frisättning av IL‑6, vilket i sin tur aktiverade enzymet COX2, en välkänd drivkraft för feber som kan hämmas av vanliga antiinflammatoriska läkemedel. När IL‑6 eller COX2 hämmades minskade febern men antikroppssvaren förblev starka. 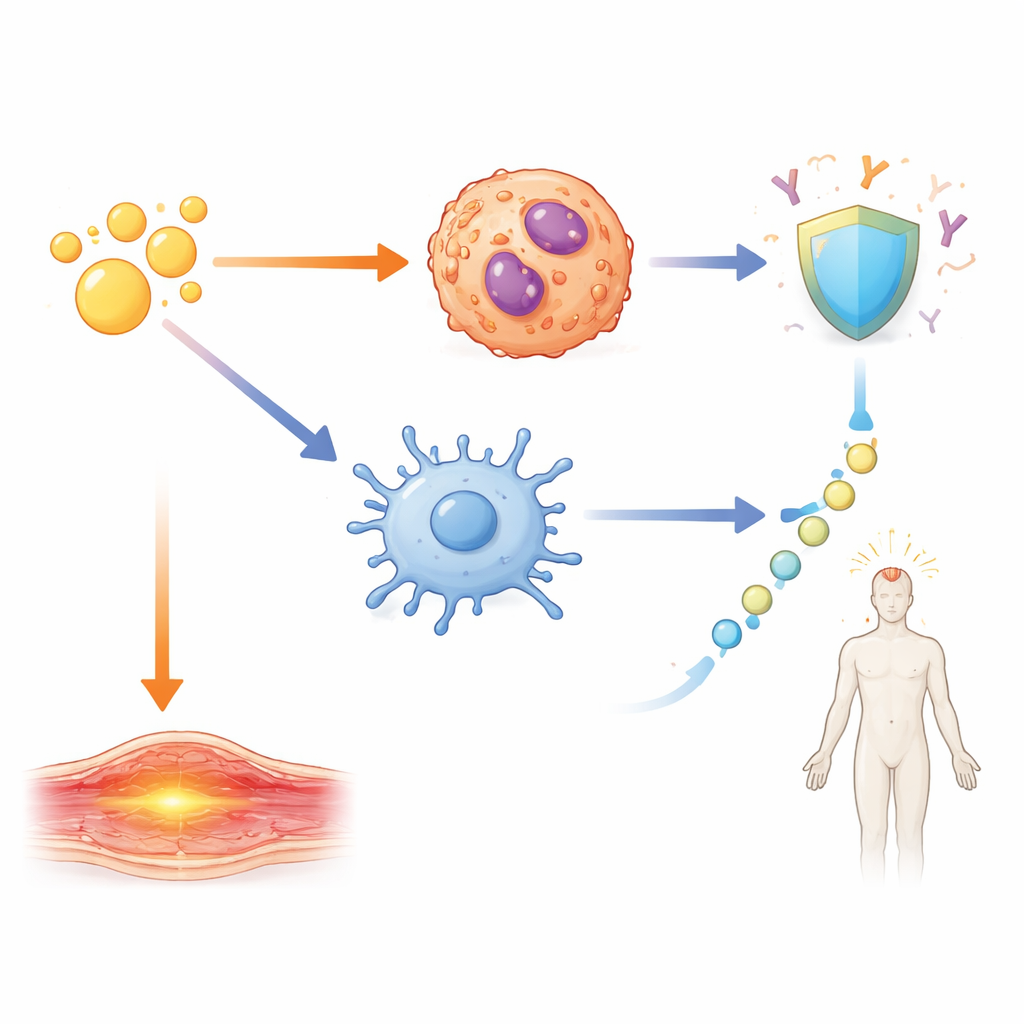
Från möss till människor
För att kontrollera om dessa fynd kan vara relevanta för människor exponerade forskarna humana blodceller från friska frivilliga för olika adjuvanser i labbet. Precis som hos möss fick squalenemulsioner som innehöll α‑tokoferol eosinofiler att producera IL‑1α, medan liknande emulsioner utan α‑tokoferol inte gjorde det. Andra typer av adjuvanser, inklusive aluminumsalter och saponinbaserade formuleringar, framkallade lite eller ingen IL‑1α i eosinofiler. Detta tyder på att α‑tokoferol‑driven IL‑1‑signalering, särskilt i eosinofiler, är ett distinkt fingeravtryck för denna adjuvansfamilj och kan fungera som en markör för lokal reaktogenicitet i framtida humanstudier.
Att utforma säkrare, starkare vaccin
Sammantaget visar studien att samma adjuvans kan använda skilda celltyper och signalvägar för att generera skydd respektive orsaka kortlivade reaktioner. IL‑1β som verkar via dendritiska celler är avgörande för starka, långvariga antikroppssvar, medan IL‑1α från eosinofiler och en IL‑1β–IL‑6–COX2‑kedja styr svullnad och feber. För vaccindesign betyder detta att effektivitet och reaktogenicitet inte är låsta tillsammans; de kan i princip justeras oberoende. Genom att rikta in sig på eller modulera de specifika grenar som driver biverkningar — utan att rubba den gren som ger immunitet — skulle framtida adjuvanser kunna ge vacciner som både är mycket effektiva och lättare att tolerera.
Citering: Yoshioka, Y., Nishinaka-Yoshioka, A., Kobiyama, K. et al. IL-1 delineates squalene-based adjuvant efficacy and reactogenicity in a cell-type-specific manner. npj Vaccines 11, 67 (2026). https://doi.org/10.1038/s41541-026-01420-0
Nyckelord: vaccinadjuvanser, squalenemulsion, interleukin-1, reaktogenicitet, alfatokoferol