Clear Sky Science · de
IL-1 grenzt die Wirksamkeit und Reaktogenität squalenbasierter Adjuvantien zelltypspezifisch ein
Warum Impfstoff-Zusätze wichtig sind
Moderne Impfstoffe benötigen häufig eine Verstärkung, damit sie optimal wirken — diese Verstärkung liefern Inhaltsstoffe, die Adjuvantien genannt werden. Solche Helfer können Impfstoffe deutlich wirksamer machen, gleichzeitig aber auch Schmerzen am Arm oder kurze Fieberreaktionen auslösen. Die vorliegende Studie untersucht eingehend eine weit verbreitete Klasse ölbasierter Adjuvantien und stellt eine zentrale Frage: Lassen sich starke Schutzwirkungen beibehalten und gleichzeitig die Nebenwirkungen reduzieren?
Öltropfen, die das Immunsystem wecken
Die Forschenden konzentrierten sich auf squalenbasierte Adjuvantien — winzige Öl-in-Wasser-Tropfen, die bereits in Grippe- und COVID-19-Impfstoffen verwendet werden. Zwei davon, darunter das COVID-19-Adjuvans A-910823, enthalten eine Form von Vitamin E, genannt α-Tocopherol, die mit stärkeren Antikörperantworten, aber auch mit erhöhter Entzündung in Verbindung gebracht worden war. Anhand eines COVID-19-Spike-Protein-Impfstoffs bei Mäusen verglich das Team Adjuvantien mit und ohne α-Tocopherol und untersuchte den benachbarten Muskel sowie die drainierenden Lymphknoten, wo Immunantworten zuerst organisiert werden. Sie stellten fest, dass α-Tocopherol einen großen Unterschied machte: Es schaltete deutlich mehr Gene ein, die mit Entzündung und Zellbewegung verknüpft sind, besonders in den Lymphknoten.
Das Signal IL-1 im Zentrum der Geschichte
Unter allen Genveränderungen hob sich ein Weg besonders hervor — die Signalgebung durch eine Familie von Molekülen, die als IL-1 bekannt sind. Bei Mäusen, die A-910823 erhielten, waren sowohl IL-1α als auch IL-1β stark erhöht, jedoch in unterschiedlichen Zelltypen. IL-1α stammte hauptsächlich von Eosinophilen, einer weißen Blutkörperchenart, die vor allem aus Allergien und Asthma bekannt ist. IL-1β dagegen stieg in mehreren myeloischen Zellen an, darunter Neutrophile, Monozyten und dendritische Zellen. Entfernten die Forschenden α-Tocopherol aus dem Adjuvans, fiel insbesondere IL-1β deutlich ab. Ähnliche Muster zeigten sich, als sie von Menschen zugelassene Nachahmer anderer Squalenadjuvantien testeten, was darauf hindeutet, dass dieses Verhalten ein gemeinsames Merkmal α-Tocopherol-haltiger Ölemulsionen ist. 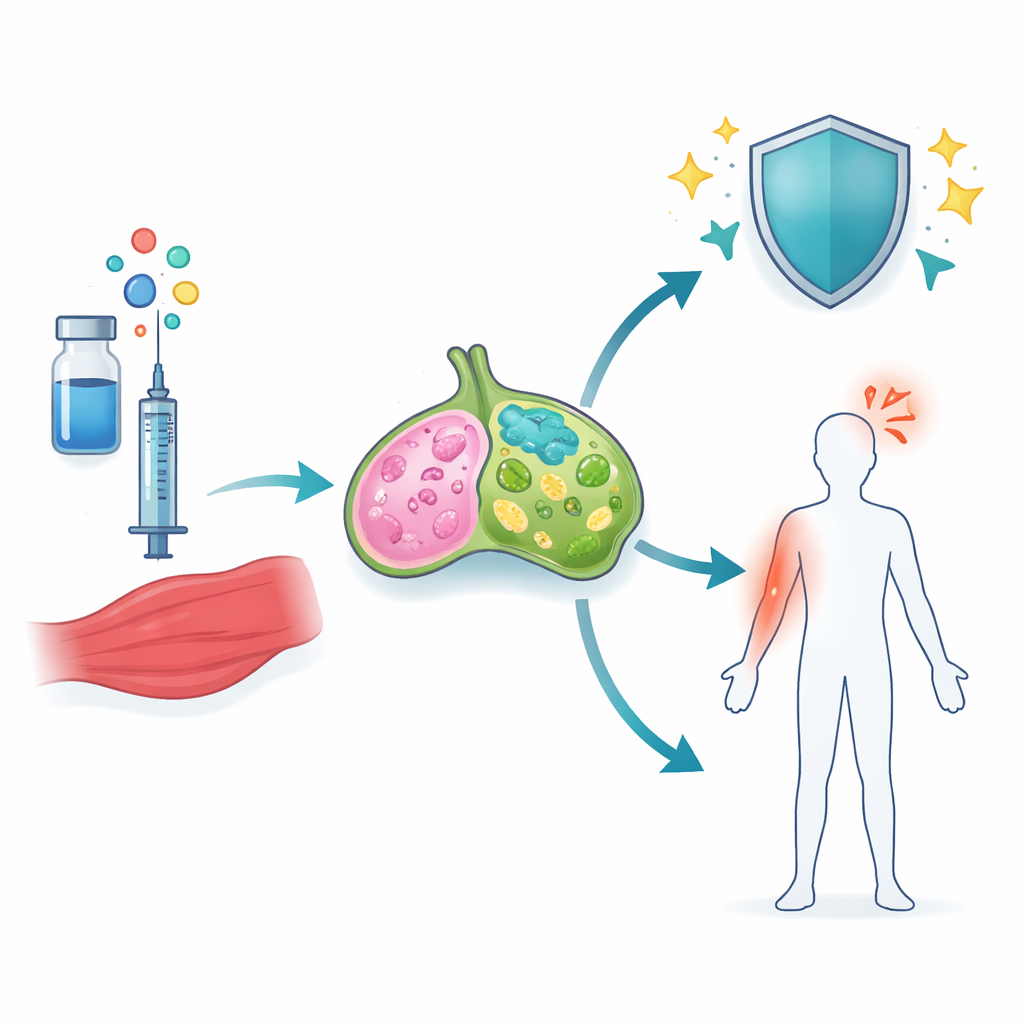
Schutz von Nebenwirkungen trennen
Das Team fragte dann, wie sich diese IL-1-Signale in konkrete Ergebnisse übersetzen: schützende Antikörper und kurzzeitige Reaktionen wie Schwellung und Fieber. Durch den Einsatz von Mäusen ohne bestimmte Rezeptoren oder Signalmoleküle und durch Blockade von IL-1β kartierten sie unterschiedliche Schaltkreise. Starke Antikörperantworten sowie die Bildung spezialisierter Helfer-T-Zellen und Keimzentrum-B-Zellen wurden von einem IL-1β-abhängigen Weg angetrieben, der über das wichtige Adapterprotein MyD88 in CD11c-positiven Zellen wie dendritischen Zellen wirkt. Lokale Armschwellung hing hingegen hauptsächlich von IL-1α ab, das von Eosinophilen in der Nähe der Injektionsstelle stammte. Systemisches Fieber folgte einem weiteren Pfad: IL-1β löste die Freisetzung von IL-6 aus, das wiederum das Enzym COX2 aktivierte — ein bekannter Fiebertreiber, der durch gängige entzündungshemmende Medikamente blockiert werden kann. Wurden IL-6 oder COX2 gehemmt, nahm das Fieber ab, während die Antikörperantworten stark blieben. 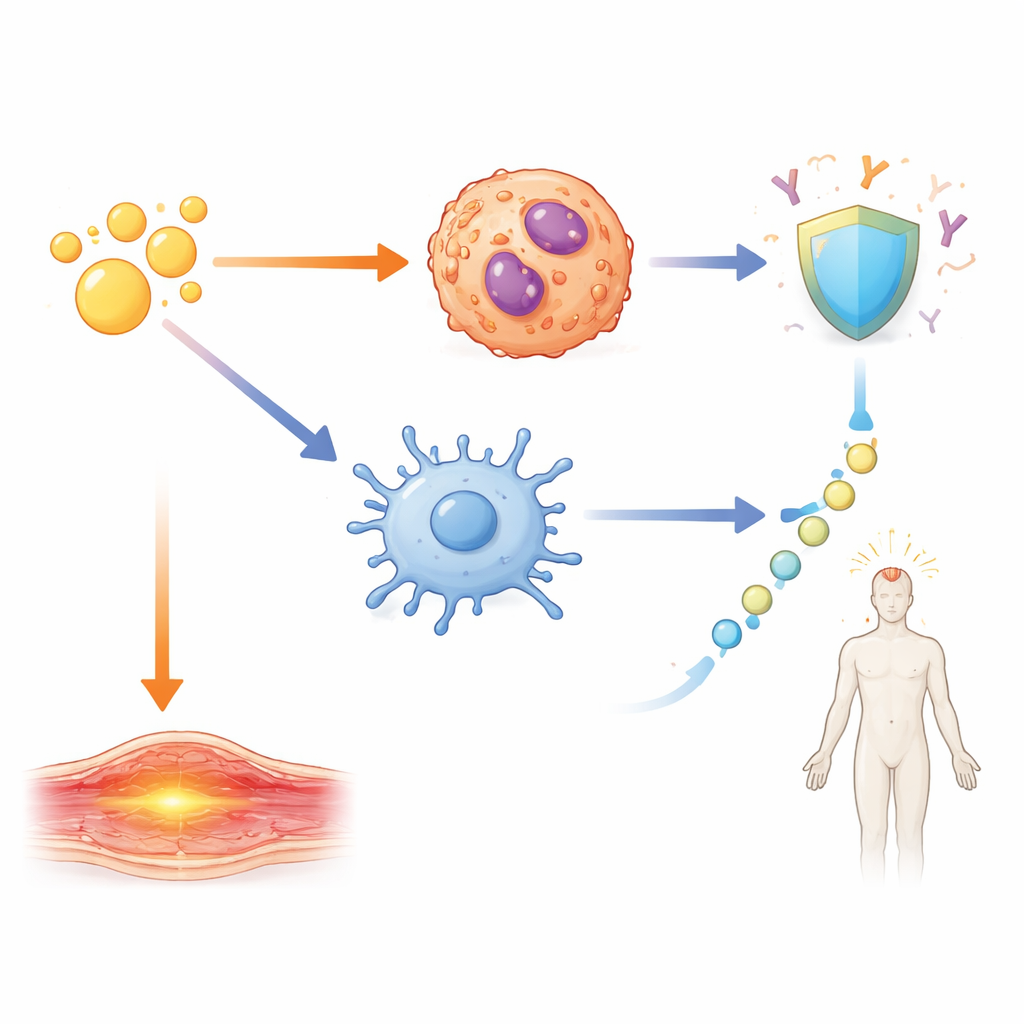
Von Mäusen zu Menschen
Um zu prüfen, ob diese Befunde beim Menschen relevant sein könnten, setzten die Forschenden Blutzellen gesunder Freiwilliger im Labor verschiedenen Adjuvantien aus. Wie bei Mäusen veranlassten α-Tocopherol-haltige Squalenemulsionen Eosinophile zur Produktion von IL-1α, während ähnliche Emulsionen ohne α-Tocopherol dies nicht taten. Andere Adjuvanztypen, darunter Aluminiumsalze und saponinbasierte Formulierungen, erzeugten in Eosinophilen wenig oder gar kein IL-1α. Das deutet darauf hin, dass α-Tocopherol-getriebene IL-1-Signalgebung, insbesondere in Eosinophilen, ein charakteristischer Fingerabdruck dieser Adjuvansfamilie ist und in künftigen Studien am Menschen als Marker lokaler Reaktogenität dienen könnte.
Sicherere, stärkere Impfstoffe entwerfen
Insgesamt zeigt die Studie, dass dasselbe Adjuvans unterschiedliche Zelltypen und Signalwege nutzen kann, um Schutz zu erzeugen und zeitlich begrenzte Reaktionen zu verursachen. IL-1β, das über dendritische Zellen wirkt, ist entscheidend für starke, lang anhaltende Antikörperantworten, während IL-1α aus Eosinophilen und eine IL-1β–IL-6–COX2-Kaskade Schwellungen und Fieber steuern. Für die Impfstoffgestaltung bedeutet dies, dass Wirksamkeit und Reaktogenität nicht zwangsläufig miteinander verbunden sind; sie lassen sich prinzipiell unabhängig voneinander feinjustieren. Durch gezieltes Ansteuern oder Modulieren der spezifischen Zweige, die Nebenwirkungen auslösen — ohne den Zweig zu stören, der die Immunität antreibt — könnten künftige Adjuvantien Impfstoffe liefern, die sowohl hochwirksam als auch besser verträglich sind.
Zitation: Yoshioka, Y., Nishinaka-Yoshioka, A., Kobiyama, K. et al. IL-1 delineates squalene-based adjuvant efficacy and reactogenicity in a cell-type-specific manner. npj Vaccines 11, 67 (2026). https://doi.org/10.1038/s41541-026-01420-0
Schlüsselwörter: Impfstoff-Adjuvanzien, Squalenemulsion, Interleukin-1, Reaktogenität, Alpha-Tocopherol