Clear Sky Science · he
IL-1 מגדיר באופן ספציפי לפי סוג תא את היעילות והרטקטוגניות של אדג'ובנטים מבוססי סקוואלן
מדוע תוספות לחיסונים חשובות
חיסונים מודרניים לעיתים זקוקים לחיזוק כדי לפעול באופן מיטבי, וחיזוק זה מגיע ממרכיבים המכונים אדג'ובנטים. אמנם עוזרים אלה יכולים להפוך חיסונים למגנים הרבה יותר, אך הם עלולים גם לגרום לזרוע כואבת או לחום קצר. המחקר הזה בוחן מקרוב כיתה נפוצה של אדג'ובנטים מבוססי שמן ושואל שאלה מרכזית: האם אפשר לשמור על ההגנה החזקה שלהם תוך הורדת תופעות הלוואי?
טיפות שמן שמעוררות את המערכת החיסונית
החוקרים התמקדו באדג'ובנטים מבוססי סקוואלן — טיפות שמן-במים זעירות שכבר נמצאות בשימוש בחיסוני שפעת ו-COVID-19. שניים מאלו, כולל האדג'ובנט של COVID-19 A-910823, מכילים צורת ויטמין E הנקראת α-טוקופרול, אשר נקשרה לתגובות נוגדנים חזקות יותר אך גם לדלקת מוגברת. בעזרת חיסון חלבון הספייק של COVID-19 בעכברים, הצוות השווה אדג'ובנטים עם ובלעדיי α-טוקופרול ובחן את השריר הסמוך ובלוטות הלימפה הנוספות, שם מאורגנות התגובות החיסוניות הראשונות. הם מצאו ש-α-טוקופרול עשה הבדל גדול: הוא הפעיל הרבה יותר גנים הקשורים לדלקת ותנועת תאים, במיוחד בבלוטות הלימפה.
האות שנקראת IL-1 במרכז הסיפור
מבין כל השינויים הגנטיים, נתיב אחד בלט — איתות מונע על ידי משפחת מולקולות הידועה כ-IL-1. בעכברים שקיבלו A-910823, הן IL-1α והן IL-1β הוגברו בחוזקה, אך בתאי סוגים שונים. IL-1α מקורו בעיקר באאוזנופילים, סוג של תאי דם לבנים הידועים בעיקר מאלרגיה ואסטמה. IL-1β, לעומת זאת, עלה בכמה תאי מיואיד, כולל נויטרופילים, מונוציטים ותאי דנדריט. כאשר החוקרים הסירו את ה-α-טוקופרול מהאדג'ובנט, IL-1β ירד באופן חזק במיוחד. דפוסים דומים הופיעו כאשר הם בחנו חיקויים מאושרים לאנשים של אדג'ובנטים סקוואלן אחרים, מה שמראה שהתנהגות זו היא תכונה משותפת של אמולסיות שמן המכילות α-טוקופרול. 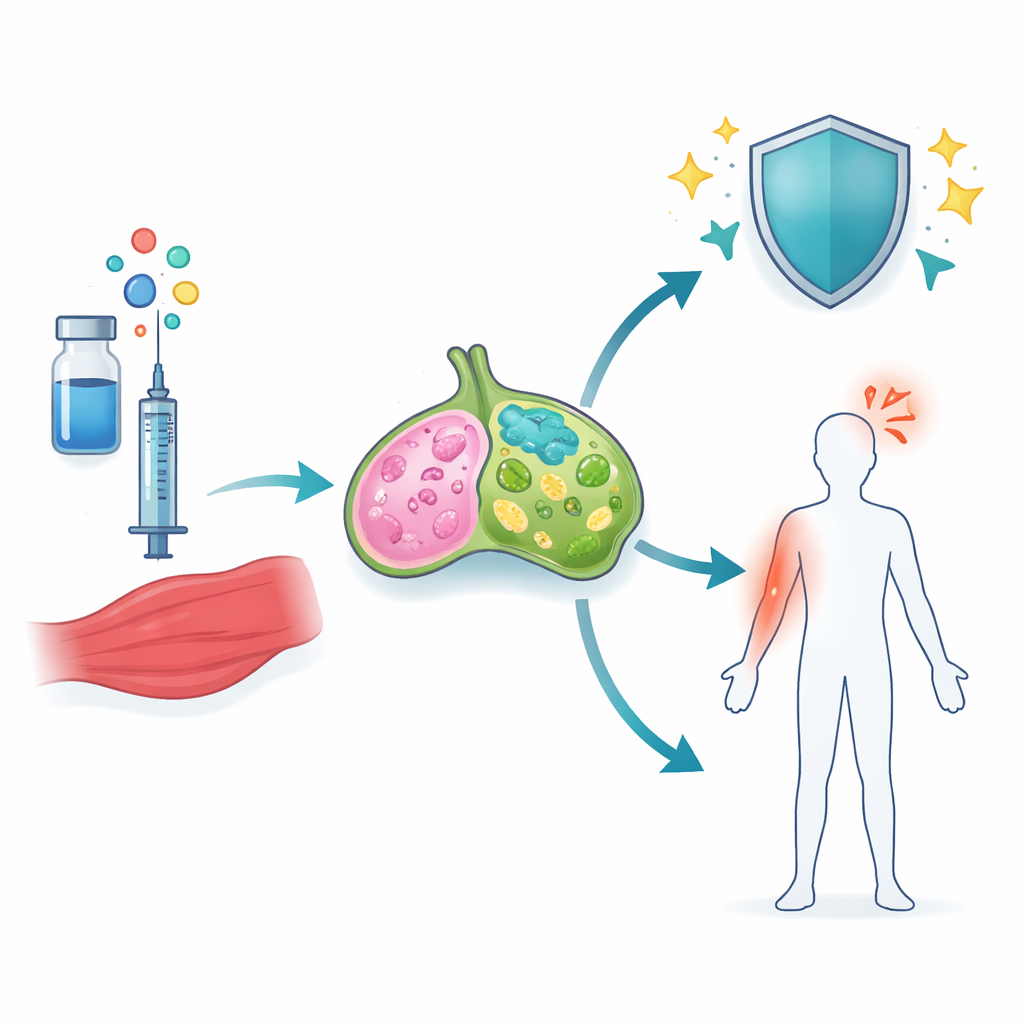
להפריד בין הגנה לתופעות לוואי
הצוות שאל אז כיצד אותות ה-IL-1 הללו מתורגמים לתוצאות במציאות: נוגדנים מגינים ותגובות קצרות טווח כמו נפיחות וחום. באמצעות שימוש בעכברים חסרי רצפטורים או מולקולות איתות ספציפיות, ובחסימת IL-1β, הם מיפו מעגלים נפרדים. תגובות נוגדנים חזקות והיווצרות תאי עזר מיוחדים של T ותאי B במרכזי נבט הונעו על ידי נתיב התלוי ב-IL-1β שפועל דרך חלבון המתאם המרכזי MyD88 בתוך תאים בעלי ביטוי CD11c כגון תאי דנדריט. עם זאת, נפיחות מקומית בזרוע תלתה בעיקר ב-IL-1α שמקורו באאוזנופילים בסמוך לאתר ההזרקה. החום הסיסטמי עבר נתיב נוסף: IL-1β גרם לשחרור IL-6, אשר בתורה הפעיל את האנזים COX2, מניע חום ידוע שניתן לחסום באמצעות תרופות אנטי-דלקתיות נפוצות. כאשר נעצר IL-6 או COX2, החום הופחת אך תגובות הנוגדנים נותרו חזקות. 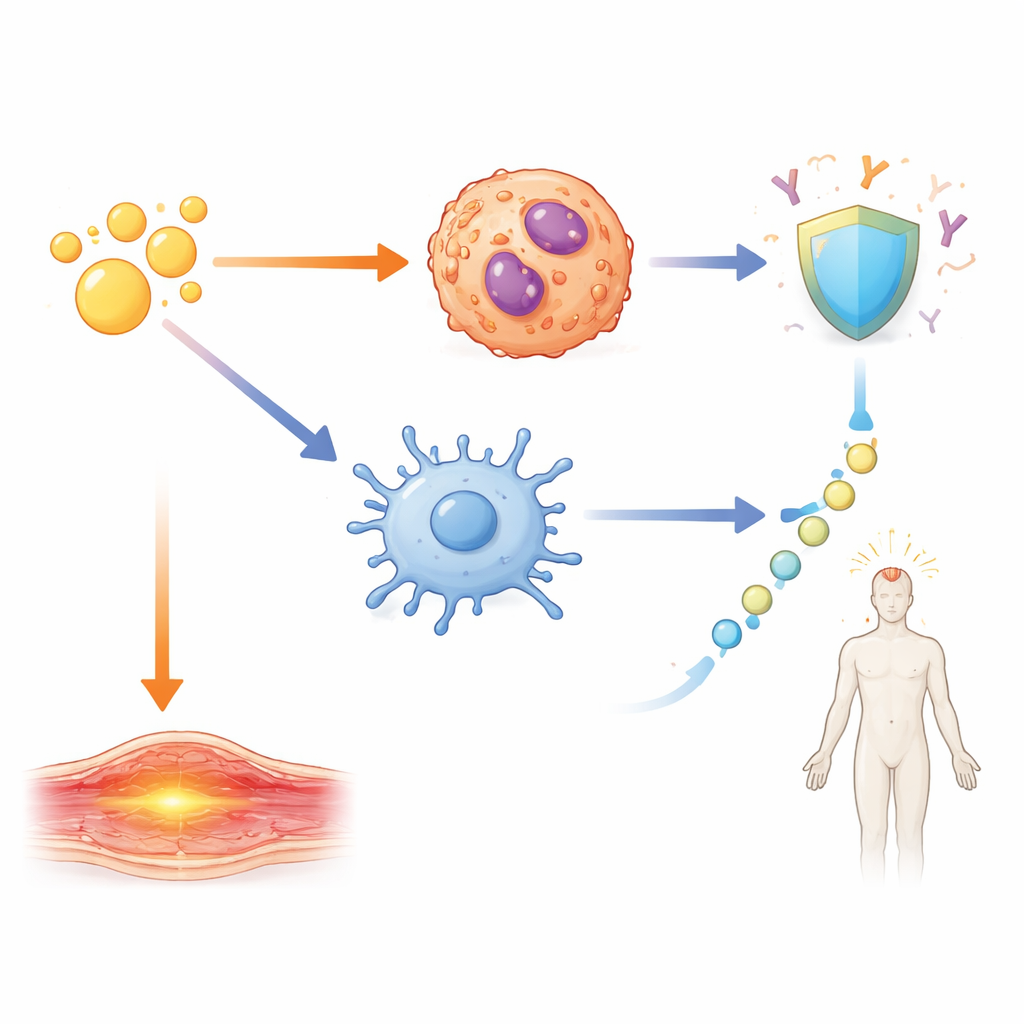
מעכברים לאדם
כדי לבדוק האם ממצאים אלו עשויים להיות רלוונטיים בבני אדם, החוקרים חשפו תאי דם אנושיים מתנדבים בריאים לאדג'ובנטים שונים במעבדה. בדיוק כפי שבעכברים, אמולסיות סקוואלן המכילות α-טוקופרול עוררו אאוזנופילים לייצר IL-1α, בעוד שאמולסיות דומות שחסרות α-טוקופרול לא עשו זאת. סוגים אחרים של אדג'ובנטים, כולל מלחים של אלומיניום ונוסחים מבוססי סאפונינים, ייצרו מעט או לא ייצרו IL-1α באאוזנופילים. הדבר מצביע על כך שאיתות IL-1 מונע על ידי α-טוקופרול, ובמיוחד באאוזנופילים, הוא טביעת אצבע מובחנת של משפחת אדג'ובנטים זו ויכול לשמש כסמן לרטקטוגניות מקומית במחקרים עתידיים בבני אדם.
עיצוב חיסונים בטוחים וחזקים יותר
בסך הכול, המחקר מראה שהאדג'ובנט עצמו יכול להשתמש בסוגי תאים ונתיבי איתות נפרדים כדי ליצור הגנה ולגרום לתגובות קצרות מועד. IL-1β הפועל דרך תאי דנדריט חיוני לתגובות נוגדנים חזקות ועמידות, בעוד IL-1α מאאוזנופילים ושרשרת IL-1β–IL-6–COX2 שולטים בנפיחות ובחום. עבור עיצוב חיסונים, משמעות הדבר היא שיעילות ורטקטוגניות אינן קשורות באופן אין־ברירה; הן ניתנות לכיוונון באופן נפרד. באמצעות מיקוד או מודולציה של הסניפים הספציפיים שמניעים תופעות לוואי — מבלי להפריע לסניף שמזין את החיסוניות — אדג'ובנטים עתידיים יכולים לספק חיסונים שעמידים ועם זאת קלים יותר לסבול.
ציטוט: Yoshioka, Y., Nishinaka-Yoshioka, A., Kobiyama, K. et al. IL-1 delineates squalene-based adjuvant efficacy and reactogenicity in a cell-type-specific manner. npj Vaccines 11, 67 (2026). https://doi.org/10.1038/s41541-026-01420-0
מילות מפתח: ממריצי חיסון, אמולסיית סקוואלן, אינטרלוקין-1, רטקטוגניות, אלפא-טוקופרול