Clear Sky Science · it
IL-1 distingue l’efficacia e la reattogenicità degli adiuvanti a base di squalene in modo specifico per tipo cellulare
Perché gli aggiustamenti dei vaccini sono importanti
I vaccini moderni spesso necessitano di uno stimolo per funzionare al meglio, e questo stimolo proviene da ingredienti chiamati adiuvanti. Pur rendendo i vaccini molto più protettivi, questi ausiliari possono anche causare dolore al braccio o febbri passeggere. Questo studio esamina da vicino una classe ampiamente utilizzata di adiuvanti oleosi e pone una domanda chiave: è possibile conservare la loro forte protezione riducendo gli effetti collaterali?
Gocce d’olio che risvegliano il sistema immunitario
I ricercatori si sono concentrati sugli adiuvanti a base di squalene — minuscole goccioline olio-in-acqua già impiegate nei vaccini antinfluenzali e contro il COVID-19. Due di questi, incluso l’adiuvante per COVID-19 A-910823, contengono una forma di vitamina E chiamata α-tocoferolo, collegata a risposte anticorpali più robuste ma anche a maggiore infiammazione. Usando un vaccino a proteina spike del COVID-19 in topi, il team ha confrontato adiuvanti con e senza α-tocoferolo ed ha esaminato il muscolo vicino e i linfonodi drenanti, dove le risposte immunitarie si organizzano inizialmente. Hanno scoperto che l’α-tocoferolo fa una grande differenza: attiva molti più geni associati all’infiammazione e al movimento cellulare, specialmente nei linfonodi.
Il segnale chiamato IL-1 al centro della storia
Tra tutti i cambiamenti genici, una via è risultata predominante — la segnalazione guidata da una famiglia di molecole note come IL-1. Nei topi trattati con A-910823, sia IL-1α sia IL-1β aumentavano nettamente, ma in tipi cellulari diversi. IL-1α proveniva principalmente dagli eosinofili, un tipo di globulo bianco noto per allergie e asma. IL-1β, al contrario, aumentava in diverse cellule mieloidi, inclusi neutrofili, monociti e cellule dendritiche. Quando i ricercatori rimossero l’α-tocoferolo dall’adiuvante, IL-1β in particolare calò drasticamente. Pattern simili emersero testando analoghi approvati per l’uomo di altri adiuvanti a base di squalene, mostrando che questo comportamento è una caratteristica condivisa delle emulsioni oleose che contengono α-tocoferolo. 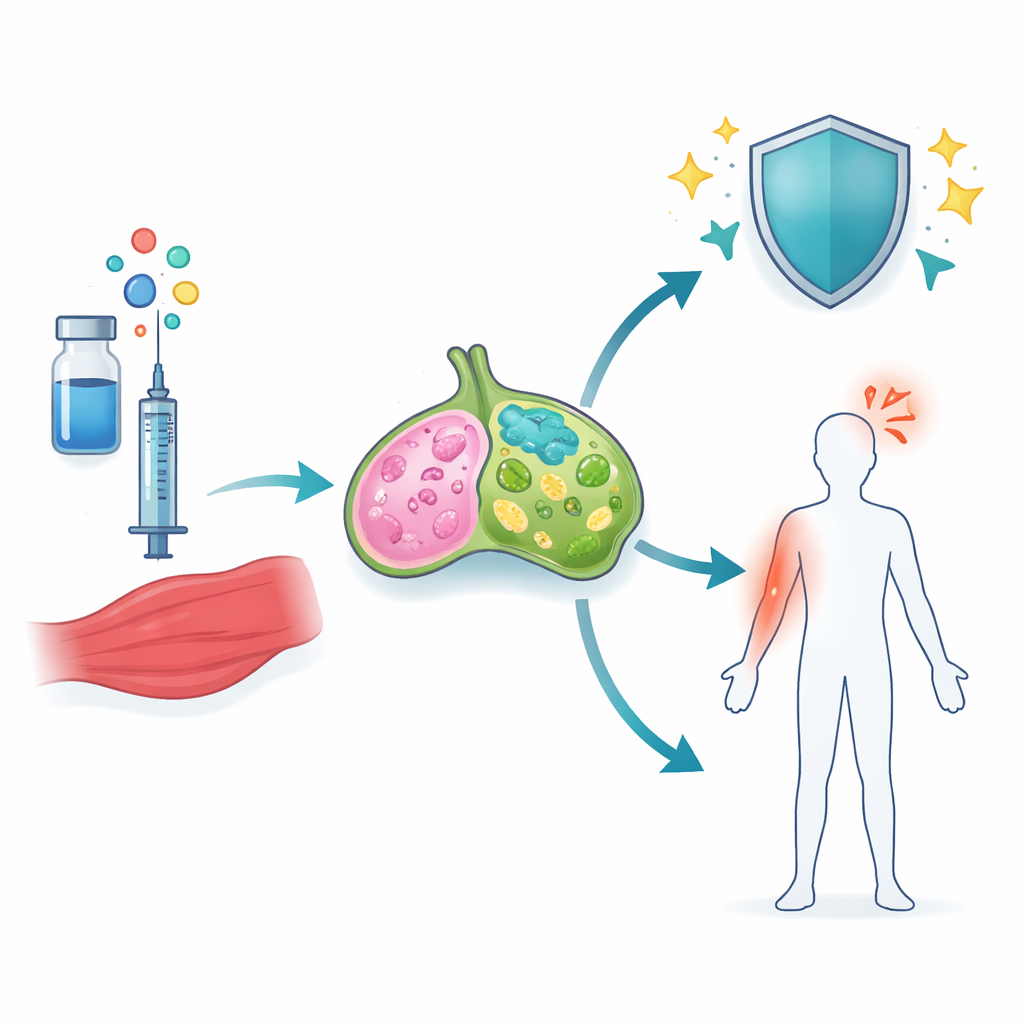
Separare protezione ed effetti collaterali
Il gruppo ha quindi indagato come questi segnali IL-1 si traducano in esiti concreti: anticorpi protettivi e reazioni a breve termine come gonfiore e febbre. Utilizzando topi privi di specifici recettori o molecole di segnalazione, e bloccando IL-1β, hanno mappato circuiti distinti. Forti risposte anticorpali e la formazione di cellule T helper specializzate e di cellule B del centro germinativo erano guidate da una via dipendente da IL-1β che agisce tramite una proteina adattatrice chiave, MyD88, all’interno di cellule CD11c-positive come le cellule dendritiche. Il gonfiore locale al braccio, invece, dipendeva principalmente da IL-1α rilasciata dagli eosinofili vicino al sito di iniezione. La febbre sistemica seguiva un’altra via: IL-1β induceva il rilascio di IL-6, che a sua volta attivava l’enzima COX2, noto promotore della febbre che può essere bloccato da comuni farmaci anti-infiammatori. Quando IL-6 o COX2 venivano inibiti, la febbre si riduceva ma le risposte anticorpali rimanevano robuste. 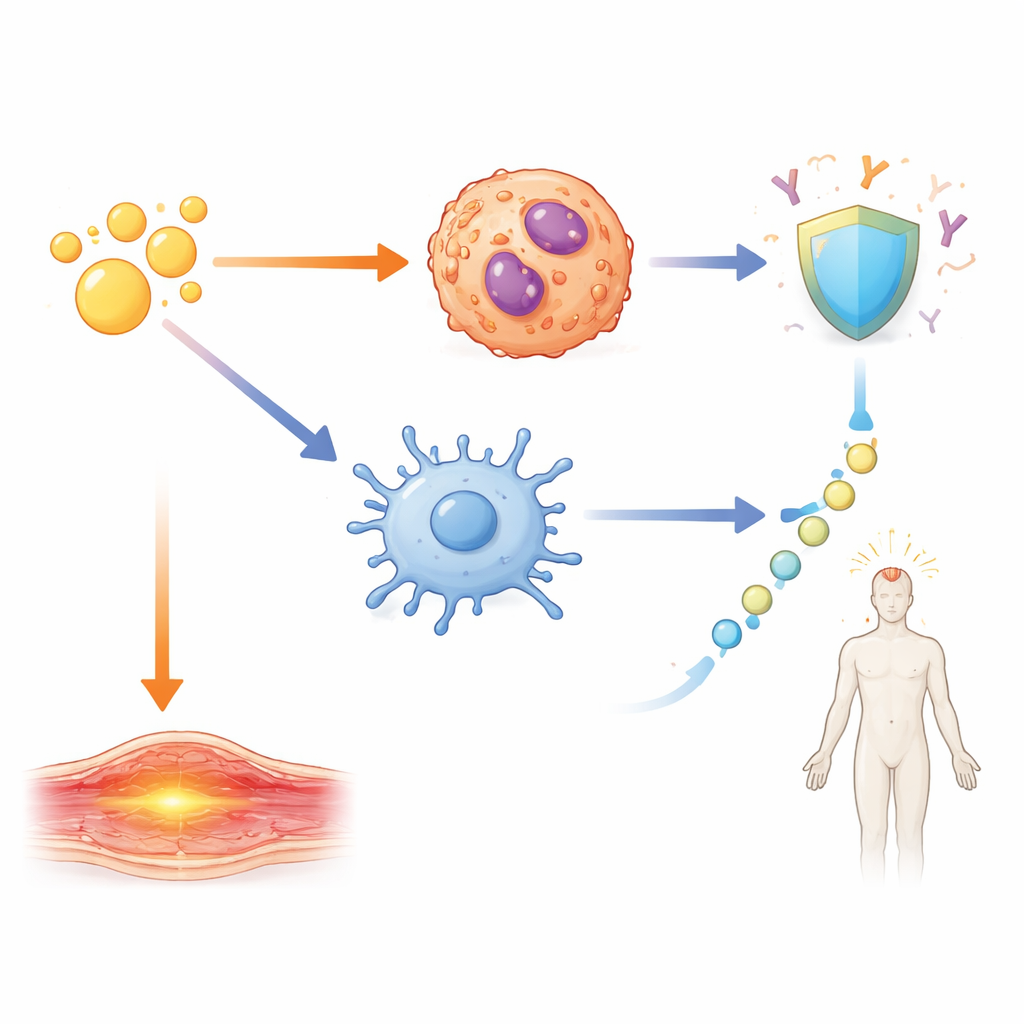
Dai topi agli esseri umani
Per verificare se questi risultati potessero avere rilevanza negli esseri umani, i ricercatori hanno esposto in laboratorio cellule del sangue umano prelevate da volontari sani a diversi adiuvanti. Proprio come nei topi, le emulsioni di squalene contenenti α-tocoferolo provocarono negli eosinofili la produzione di IL-1α, mentre emulsioni simili prive di α-tocoferolo non lo fecero. Altri tipi di adiuvanti, incluse le sali di alluminio e formulazioni a base di saponine, produssero poco o nessun IL-1α negli eosinofili. Questo suggerisce che la segnalazione IL-1 guidata dall’α-tocoferolo, specialmente negli eosinofili, è un’impronta distintiva di questa famiglia di adiuvanti e potrebbe servire da marcatore della reattogenicità locale in futuri studi nell’uomo.
Progettare vaccini più sicuri e più efficaci
Nel complesso, lo studio mostra che lo stesso adiuvante può usare tipi cellulari e vie di segnalazione separati per generare protezione e per causare reazioni di breve durata. IL-1β che agisce attraverso le cellule dendritiche è cruciale per risposte anticorpali forti e durature, mentre IL-1α dagli eosinofili e una catena IL-1β–IL-6–COX2 regolano gonfiore e febbre. Per la progettazione dei vaccini, ciò significa che efficacia e reattogenicità non sono vincolate insieme; in linea di principio, possono essere modulati indipendentemente. Mirando o modulando i rami specifici che guidano gli effetti collaterali — senza disturbare il ramo che alimenta l’immunità — i futuri adiuvanti potrebbero offrire vaccini sia altamente efficaci sia più tollerabili.
Citazione: Yoshioka, Y., Nishinaka-Yoshioka, A., Kobiyama, K. et al. IL-1 delineates squalene-based adjuvant efficacy and reactogenicity in a cell-type-specific manner. npj Vaccines 11, 67 (2026). https://doi.org/10.1038/s41541-026-01420-0
Parole chiave: adiuvanti vaccinali, emulsione di squalene, interleuchina-1, reattogenicità, alfa-tocoferolo