Clear Sky Science · fr
IL-1 délimite l’efficacité et la réactogénicité des adjuvants à base de squalène de manière spécifique au type cellulaire
Pourquoi les additifs aux vaccins comptent
Les vaccins modernes nécessitent souvent un coup de pouce pour offrir une protection optimale, et ce coup de pouce provient d’ingrédients appelés adjuvants. Si ces aides peuvent considérablement renforcer la protection vaccinale, elles peuvent aussi provoquer des douleurs au bras ou des fièvres passagères. Cette étude examine de près une vaste classe d’adjuvants à base d’huile et pose une question centrale : peut-on préserver leur forte efficacité tout en réduisant les effets indésirables ?
Gouttelettes d’huile qui réveillent le système immunitaire
Les chercheurs se sont concentrés sur les adjuvants à base de squalène — de minuscules gouttelettes huile-dans-eau déjà utilisées dans des vaccins contre la grippe et la COVID‑19. Deux de ces adjuvants, y compris l’adjuvant COVID‑19 A-910823, contiennent une forme de vitamine E appelée α‑tocophérol, associée à des réponses en anticorps plus fortes mais aussi à davantage d’inflammation. En utilisant un vaccin à protéine spike contre la COVID‑19 chez la souris, l’équipe a comparé des adjuvants avec et sans α‑tocophérol et a examiné le muscle voisin et les ganglions lymphatiques drainants, où les réponses immunitaires s’organisent d’abord. Ils ont constaté que l’α‑tocophérol faisait une grande différence : il activait beaucoup plus de gènes liés à l’inflammation et au mouvement cellulaire, en particulier dans les ganglions lymphatiques.
Le signal nommé IL‑1 au centre de l’histoire
Parmi tous les changements d’expression génétique, une voie a dominé — la signalisation pilotée par une famille de molécules connues sous le nom d’IL‑1. Chez les souris ayant reçu A‑910823, IL‑1α et IL‑1β augmentaient fortement, mais dans des types cellulaires différents. L’IL‑1α provenait principalement des éosinophiles, un type de globules blancs mieux connu pour son rôle dans les allergies et l’asthme. L’IL‑1β, en revanche, augmentait dans plusieurs cellules myéloïdes, notamment les neutrophiles, les monocytes et les cellules dendritiques. Lorsque les chercheurs ont retiré l’α‑tocophérol de l’adjuvant, l’IL‑1β a chuté de manière marquée. Des motifs similaires sont apparus lorsqu’ils ont testé des analogues approuvés pour l’homme d’autres adjuvants au squalène, montrant que ce comportement est une caractéristique partagée des émulsions huileuses contenant de l’α‑tocophérol. 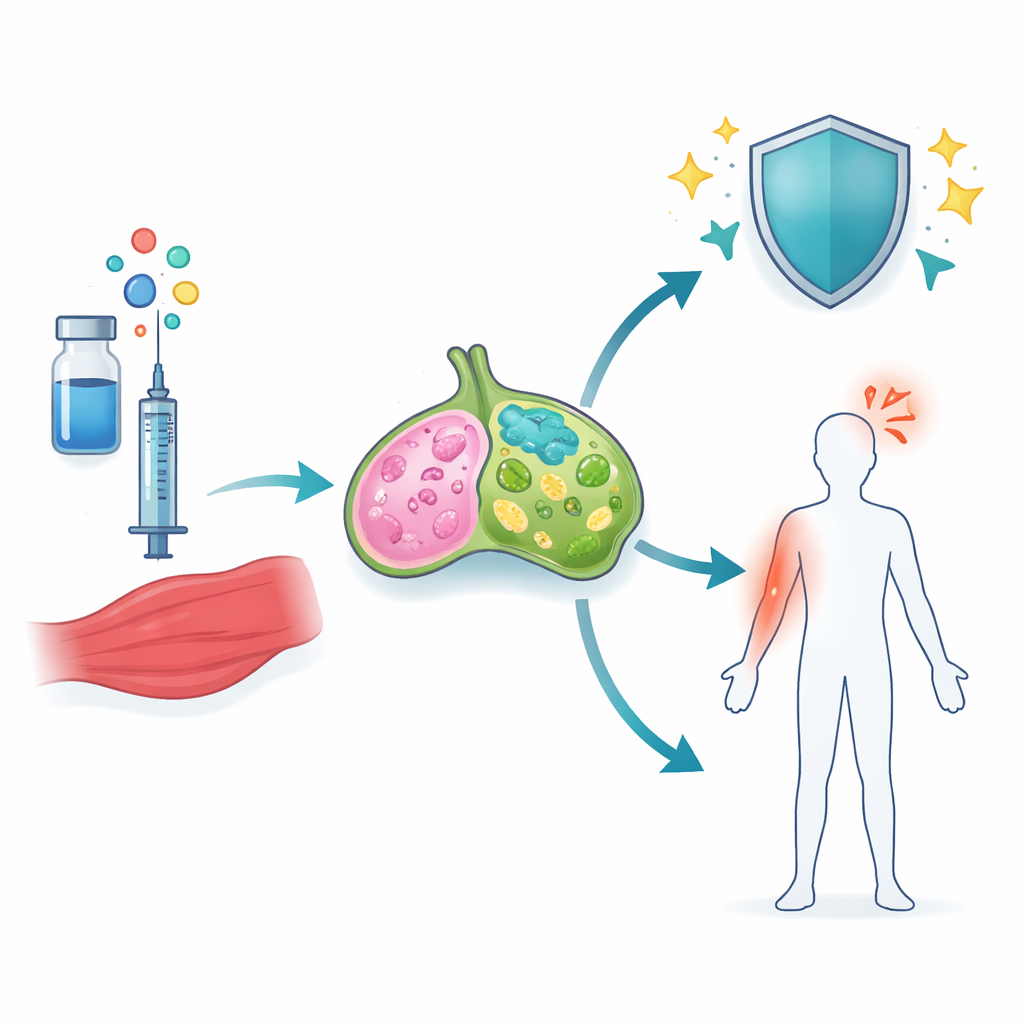
Séparer la protection des effets secondaires
L’équipe a ensuite cherché à savoir comment ces signaux IL‑1 se traduisent en résultats concrets : anticorps protecteurs et réactions à court terme comme le gonflement et la fièvre. En utilisant des souris dépourvues de récepteurs ou de molécules de signalisation spécifiques, et en bloquant l’IL‑1β, ils ont cartographié des circuits distincts. Les fortes réponses en anticorps et la formation de cellules T auxiliaires spécialisées et de cellules B des centres germinatifs étaient pilotées par une voie dépendante de l’IL‑1β agissant via une protéine adaptatrice clé, MyD88, au sein de cellules CD11c‑positives telles que les cellules dendritiques. Le gonflement local du bras dépendait toutefois principalement de l’IL‑1α provenant des éosinophiles proches du site d’injection. La fièvre systémique empruntait une autre voie : l’IL‑1β déclenchait la libération d’IL‑6, qui à son tour activait l’enzyme COX2, un moteur bien connu de la fièvre et bloquable par des anti-inflammatoires courants. Lorsque l’IL‑6 ou COX2 était inhibé, la fièvre diminuait mais les réponses en anticorps restaient robustes. 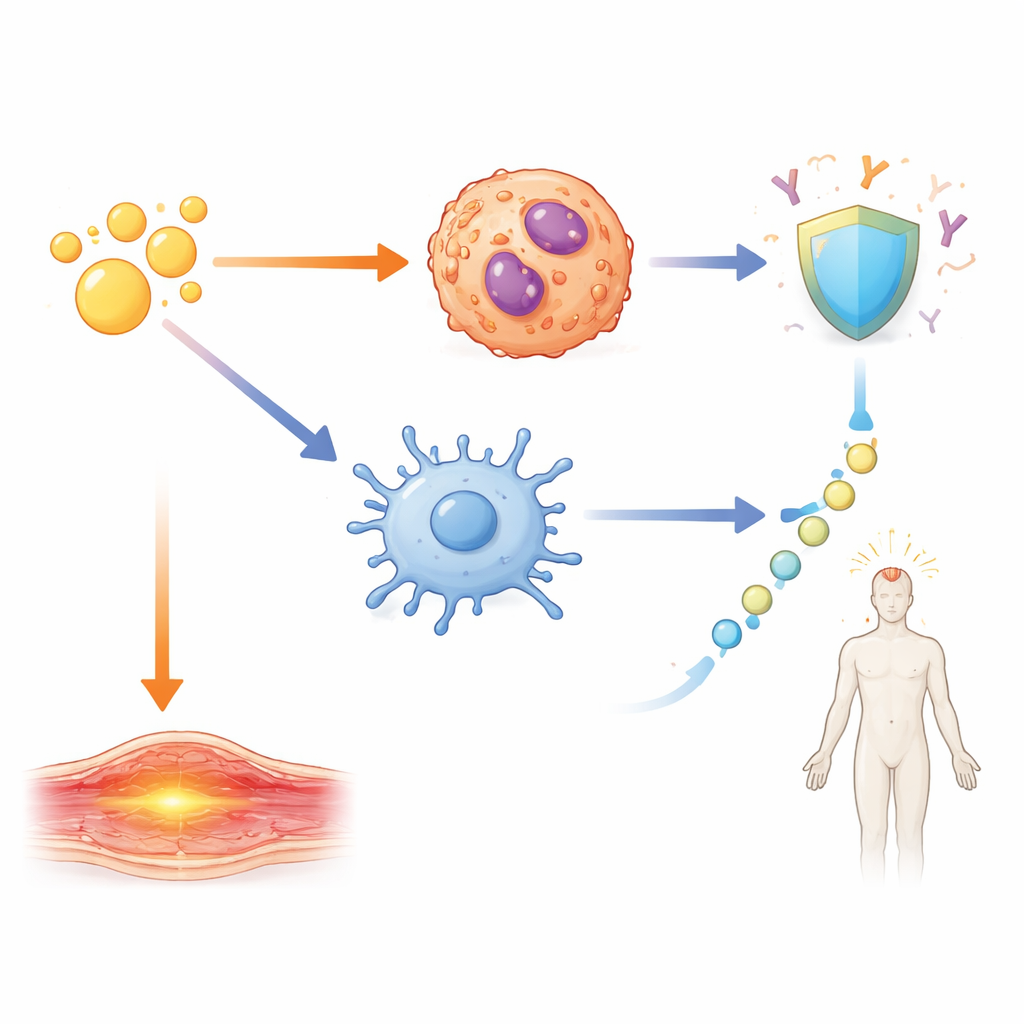
Des souris aux humains
Pour vérifier si ces découvertes pouvaient avoir une portée chez l’homme, les chercheurs ont exposé in vitro des cellules sanguines humaines provenant de volontaires sains à différents adjuvants. Tout comme chez la souris, les émulsions de squalène contenant de l’α‑tocophérol ont provoqué la production d’IL‑1α par les éosinophiles, tandis que des émulsions similaires sans α‑tocophérol ne l’ont pas fait. D’autres types d’adjuvants, y compris les sels d’aluminium et les formulations à base de saponines, ont produit peu ou pas d’IL‑1α dans les éosinophiles. Cela suggère que la signalisation IL‑1 induite par l’α‑tocophérol, en particulier dans les éosinophiles, est une signature distinctive de cette famille d’adjuvants et pourrait servir de marqueur de la réactogénicité locale dans de futures études humaines.
Concevoir des vaccins plus sûrs et plus puissants
Globalement, l’étude montre qu’un même adjuvant peut utiliser des types cellulaires et des voies de signalisation séparés pour générer la protection et provoquer des réactions de courte durée. L’IL‑1β agissant via les cellules dendritiques est cruciale pour des réponses en anticorps fortes et durables, tandis que l’IL‑1α des éosinophiles et une chaîne IL‑1β–IL‑6–COX2 gouvernent le gonflement et la fièvre. Pour la conception vaccinale, cela signifie que l’efficacité et la réactogénicité ne sont pas indissociables ; elles peuvent, en principe, être modulées indépendamment. En ciblant ou en modulant les branches spécifiques qui causent les effets secondaires — sans perturber la branche qui alimente l’immunité — les futurs adjuvants pourraient permettre des vaccins à la fois très efficaces et mieux tolérés.
Citation: Yoshioka, Y., Nishinaka-Yoshioka, A., Kobiyama, K. et al. IL-1 delineates squalene-based adjuvant efficacy and reactogenicity in a cell-type-specific manner. npj Vaccines 11, 67 (2026). https://doi.org/10.1038/s41541-026-01420-0
Mots-clés: adjuvants vaccinaux, émulsion de squalène, interleukine-1, réactogénicité, alpha-tocophérol