Clear Sky Science · pl
IL-1 wyznacza skuteczność i reaktywność adjuwantów na bazie skwalenu w sposób specyficzny dla typów komórek
Dlaczego dodatki do szczepionek mają znaczenie
Nowoczesne szczepionki często potrzebują wsparcia, by działać optymalnie — tym wsparciem są składniki zwane adjuwantami. Choć te dodatki mogą znacznie zwiększyć ochronę, mogą też powodować ból ramienia lub krótkotrwałą gorączkę. W tym badaniu szczegółowo przyglądano się szeroko stosowanej klasie adjuwantów olejowych i zadano kluczowe pytanie: czy można zachować ich silną ochronę przy jednoczesnym zmniejszeniu skutków ubocznych?
Kropelki oleju, które budzą układ odpornościowy
Naukowcy skoncentrowali się na adjuwantach opartych na skwalenie — maleńkich kropelkach oleju w wodzie, już stosowanych w szczepionkach przeciw grypie i COVID-19. Dwa z nich, w tym adjuwant A-910823 używany w szczepionkach przeciw COVID-19, zawierają postać witaminy E zwaną α-tokoferolem, która była powiązana zarówno z silniejszą odpowiedzią przeciwciał, jak i ze zwiększonym stanem zapalnym. Używając szczepionki z białkiem kolca wirusa SARS-CoV-2 u myszy, zespół porównał adjuwanty z α-tokoferolem i bez niego oraz zbadał pobliskie mięśnie i drenujące węzły chłonne, gdzie organizowane są pierwsze odpowiedzi odpornościowe. Stwierdzili, że α-tokoferol robi dużą różnicę: uruchamia znacznie więcej genów związanych z zapaleniem i ruchem komórek, zwłaszcza w węzłach chłonnych.
Sygnał zwany IL-1 w centrum opowieści
Wśród wszystkich zmian w ekspresji genów jedna ścieżka wyróżniała się — sygnalizacja napędzana przez rodzinę cząsteczek znanych jako IL-1. U myszy otrzymujących A-910823 silnie wzrosły poziomy zarówno IL-1α, jak i IL-1β, lecz w różnych typach komórek. IL-1α pochodziła głównie od eozynofilów, rodzaju białych krwinek znanych z alergii i astmy. IL-1β natomiast wzrastała w kilku komórkach mieloidalnych, w tym w neutrofilach, monocytach i komórkach dendrytycznych. Gdy badacze usunęli α-tokoferol z adjuwantu, szczególnie IL-1β spadła gwałtownie. Podobne wzorce zaobserwowano przy testowaniu dopuszczonych do użytku ludzkiego odpowiedników innych adjuwantów skwalenowych, co pokazuje, że to zachowanie jest wspólną cechą emulsji olejowych zawierających α-tokoferol. 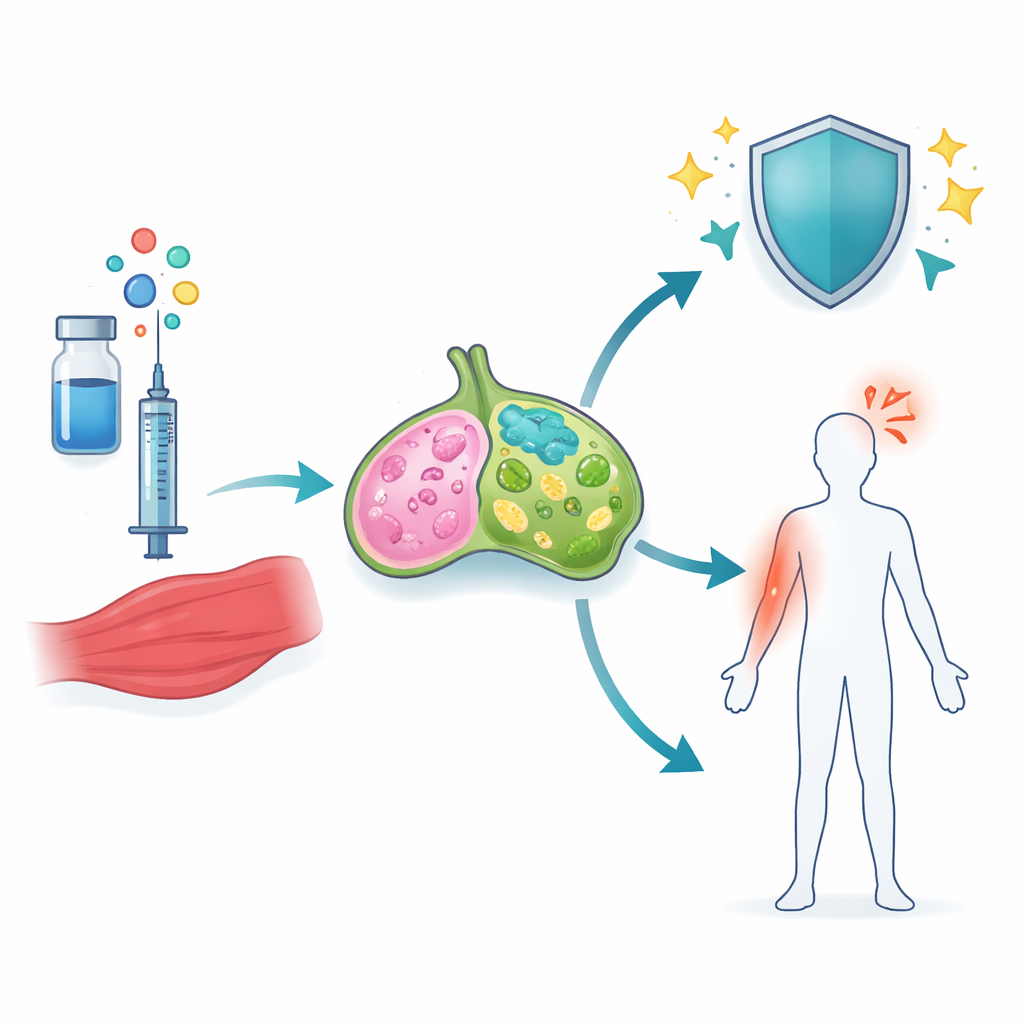
Oddzielanie ochrony od skutków ubocznych
Zespół następnie zbadał, jak te sygnały IL-1 przekładają się na rzeczywiste efekty: ochronne przeciwciała i krótkotrwałe reakcje, takie jak obrzęk i gorączka. Wykorzystując myszy pozbawione określonych receptorów lub cząsteczek sygnałowych oraz blokując IL-1β, zmapowali odrębne obwody. Silne odpowiedzi przeciwciałowe oraz tworzenie wyspecjalizowanych pomocniczych komórek T i komórek B w centrach zarodkowych były napędzane przez drogę zależną od IL-1β działającą przez kluczowy adaptor MyD88 wewnątrz komórek CD11c-dodatnich, takich jak komórki dendrytyczne. Lokalne puchnięcie ramienia zależało jednak głównie od IL-1α pochodzącego od eozynofilów w pobliżu miejsca wstrzyknięcia. Gorączka ogólnoustrojowa następowała inną drogą: IL-1β wywoływała uwalnianie IL-6, które z kolei aktywowało enzym COX2, dobrze znany induktor gorączki, który można zablokować powszechnie stosowanymi lekami przeciwzapalnymi. Gdy IL-6 lub COX2 były hamowane, gorączka była mniejsza, ale odpowiedzi przeciwciałowe pozostawały silne. 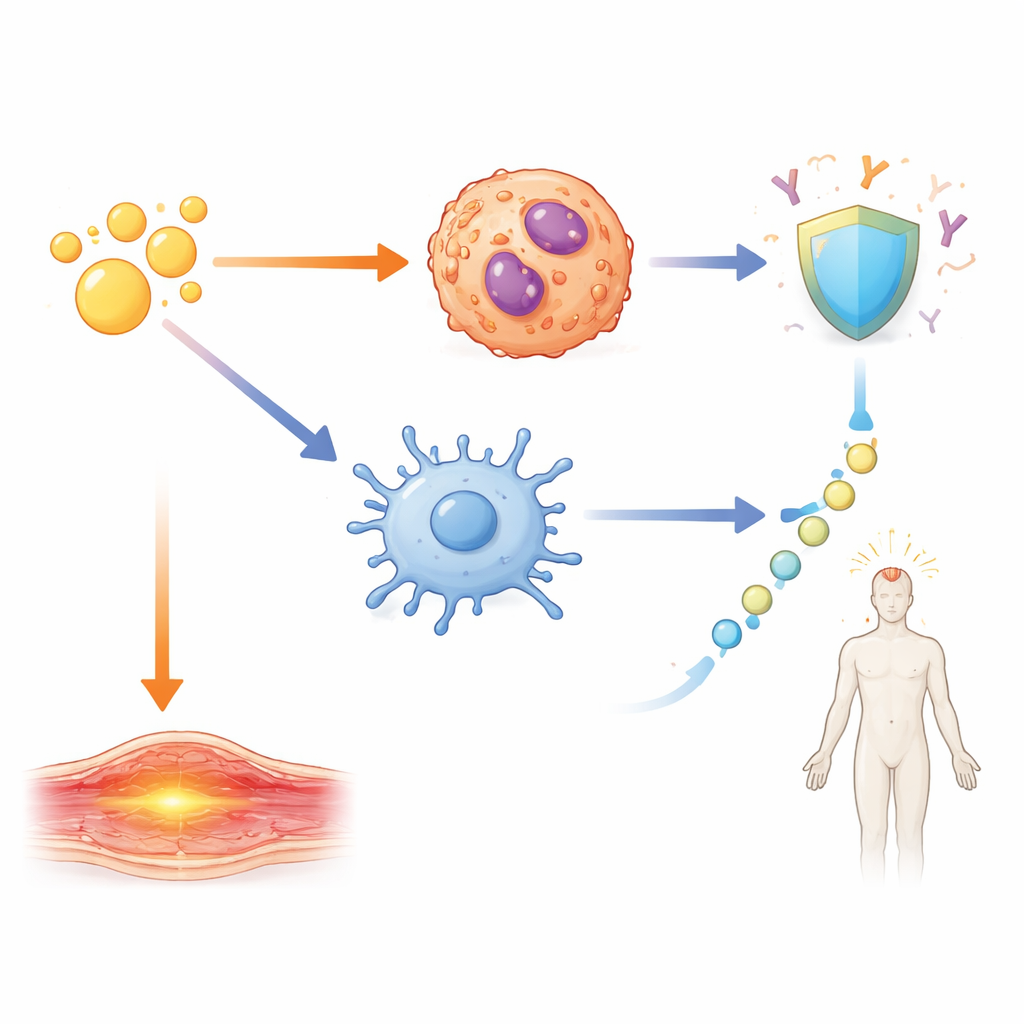
Od myszy do ludzi
Aby sprawdzić, czy te ustalenia mają znaczenie dla ludzi, badacze wystawili ludzkie komórki krwi od zdrowych ochotników na działanie różnych adjuwantów w laboratorium. Podobnie jak u myszy, emulsje skwalenowe zawierające α-tokoferol prowokowały eozynofile do produkcji IL-1α, podczas gdy podobne emulsje pozbawione α-tokoferolu tego nie robiły. Inne rodzaje adjuwantów, w tym sole glinu i formuły oparte na saponinach, wytwarzały niewiele lub wcale IL-1α w eozynofilach. Sugeruje to, że sygnalizacja IL-1 napędzana przez α-tokoferol, zwłaszcza w eozynofilach, jest charakterystycznym odciskiem palca tej rodziny adjuwantów i może służyć jako marker lokalnej reaktywności w przyszłych badaniach u ludzi.
Projektowanie bezpieczniejszych, silniejszych szczepionek
Podsumowując, badanie pokazuje, że ten sam adjuwant może wykorzystywać odrębne typy komórek i ścieżki sygnałowe do generowania ochrony oraz wywoływania krótkotrwałych reakcji. IL-1β działająca przez komórki dendrytyczne jest kluczowa dla silnych, długotrwałych odpowiedzi przeciwciałowych, podczas gdy IL-1α z eozynofilów i łańcuch IL-1β–IL-6–COX2 kontrolują obrzęk i gorączkę. Dla projektowania szczepionek oznacza to, że skuteczność i reaktywność nie są ze sobą nierozłącznie związane; w zasadzie można je dostroić niezależnie. Skierowując lub modulując konkretne odgałęzienia odpowiedzialne za skutki uboczne — bez zakłócania gałęzi napędzającej odporność — przyszłe adjuwanty mogłyby dostarczać szczepionki jednocześnie wysoce skuteczne i łatwiejsze do zniesienia.
Cytowanie: Yoshioka, Y., Nishinaka-Yoshioka, A., Kobiyama, K. et al. IL-1 delineates squalene-based adjuvant efficacy and reactogenicity in a cell-type-specific manner. npj Vaccines 11, 67 (2026). https://doi.org/10.1038/s41541-026-01420-0
Słowa kluczowe: adjuwanty szczepionkowe, emulsja skwalenowa, interleukina-1, reaktywność, alpha-tokoferol