Clear Sky Science · nl
IL-1 onderscheidt de werkzaamheid en reactogeniciteit van squalene-gebaseerde adjuvantia op celdelingsspecifieke wijze
Waarom vaccin-bijmiddelen ertoe doen
Moderne vaccins hebben vaak een extra impuls nodig om optimaal te werken; die impuls komt van ingrediënten die adjuvantia worden genoemd. Hoewel deze hulpstoffen vaccins veel beschermender kunnen maken, kunnen ze ook plaatselijke pijn of kortdurende koorts veroorzaken. Deze studie onderzoekt nauwgezet een veelgebruikte klasse olie-gebaseerde adjuvantia en stelt een centrale vraag: kunnen we de sterke bescherming behouden en tegelijk de bijwerkingen verminderen?
Vloeistofdruppels die het immuunsysteem wekken
De onderzoekers richtten zich op squalene-gebaseerde adjuvantia — kleine olie-in-waterdruppeltjes die al worden gebruikt in griep- en COVID-19-vaccins. Twee hiervan, waaronder het COVID-19-adjuvans A-910823, bevatten een vorm van vitamine E genaamd α-tocoferol, die was gekoppeld aan sterkere antilichaamreacties maar ook aan meer ontsteking. Met een COVID-19 spike-eiwitvaccin in muizen vergeleek het team adjuvantia met en zonder α-tocoferol en onderzocht ze de nabijgelegen spier en de afvoerende lymfeklieren, waar immuunreacties eerst worden georganiseerd. Ze vonden dat α-tocoferol een groot verschil maakte: het schakelde veel meer genen in die verband houden met ontsteking en celdynamiek, vooral in de lymfeklieren.
Het signaal IL-1 in het centrum van het verhaal
Onder alle genveranderingen stak één route er bovenuit — signalering aangedreven door een familie moleculen bekend als IL-1. In muizen die A-910823 kregen, waren zowel IL-1α als IL-1β sterk verhoogd, maar in verschillende celtypen. IL-1α kwam voornamelijk uit eosinofielen, een type witte bloedcel dat vooral bekend is uit allergie en astma. IL-1β daarentegen nam toe in verschillende myeloïde cellen, waaronder neutrofielen, monocyten en dendritische cellen. Toen de onderzoekers α-tocoferol uit het adjuvans verwijderden, daalde met name IL-1β scherp. Vergelijkbare patronen verschenen toen ze goedgekeurde menselijke varianten van andere squalene-adjuvantia testten, wat laat zien dat dit gedrag een gemeenschappelijke eigenschap is van olie-emulsies die α-tocoferol bevatten. 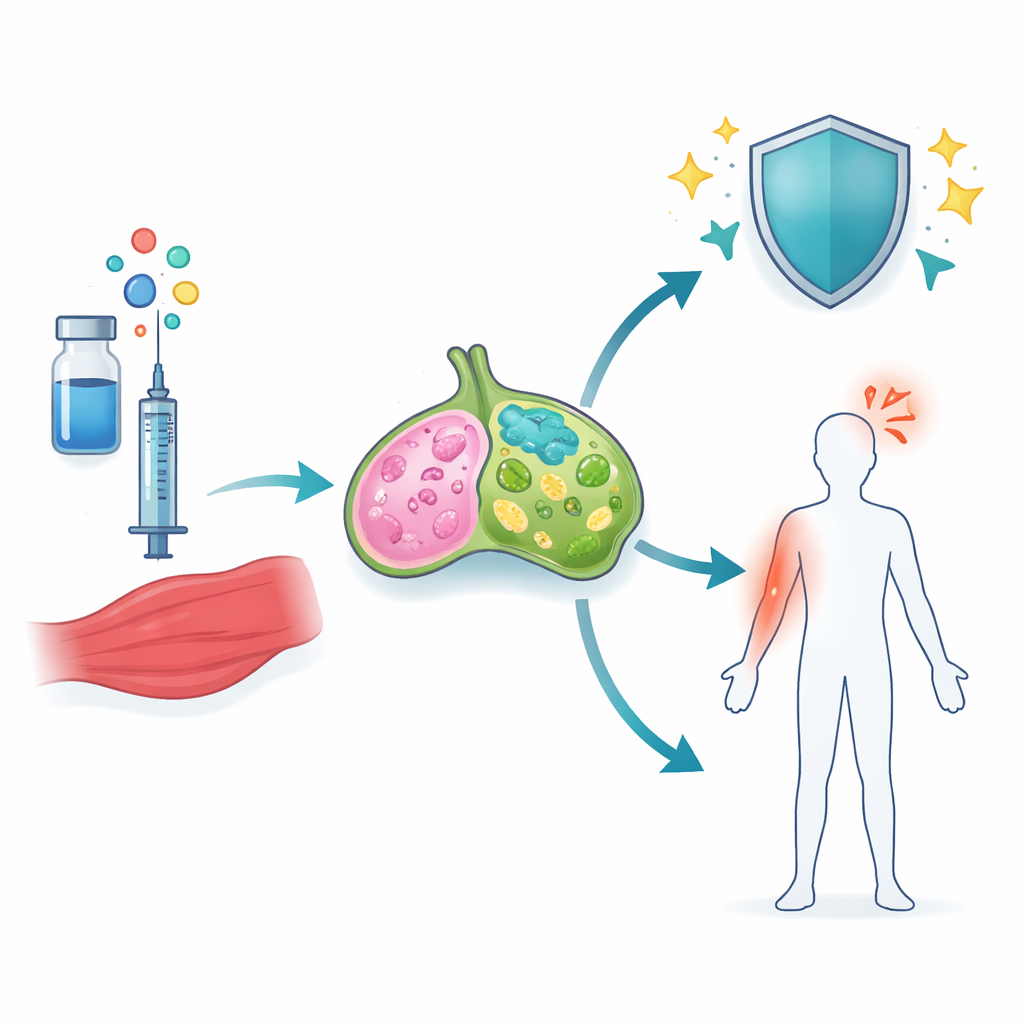
Bescherming scheiden van bijwerkingen
Het team vroeg zich vervolgens af hoe deze IL-1-signalen zich vertalen naar reële uitkomsten: beschermende antilichamen en kortdurende reacties zoals zwelling en koorts. Door muizen zonder specifieke receptoren of signaalmoleculen te gebruiken en door IL-1β te blokkeren, brachten ze afzonderlijke circuits in kaart. Sterke antilichaamreacties en de vorming van gespecialiseerde helper-T-cellen en kiemcentrum B-cellen werden aangedreven door een IL-1β-afhankelijke route die via het adaptor-eiwit MyD88 binnen CD11c-positieve cellen, zoals dendritische cellen, werkt. Lokale zwelling van de arm hing daarentegen vooral af van IL-1α afkomstig van eosinofielen in de buurt van de injectieplaats. Systemische koorts volgde weer een andere route: IL-1β veroorzaakte de afgifte van IL-6, dat op zijn beurt het enzym COX2 activeerde, een bekende aanjager van koorts die geblokkeerd kan worden door gangbare ontstekingsremmers. Wanneer IL-6 of COX2 werd geremd, nam de koorts af maar bleven de antilichaamreacties sterk. 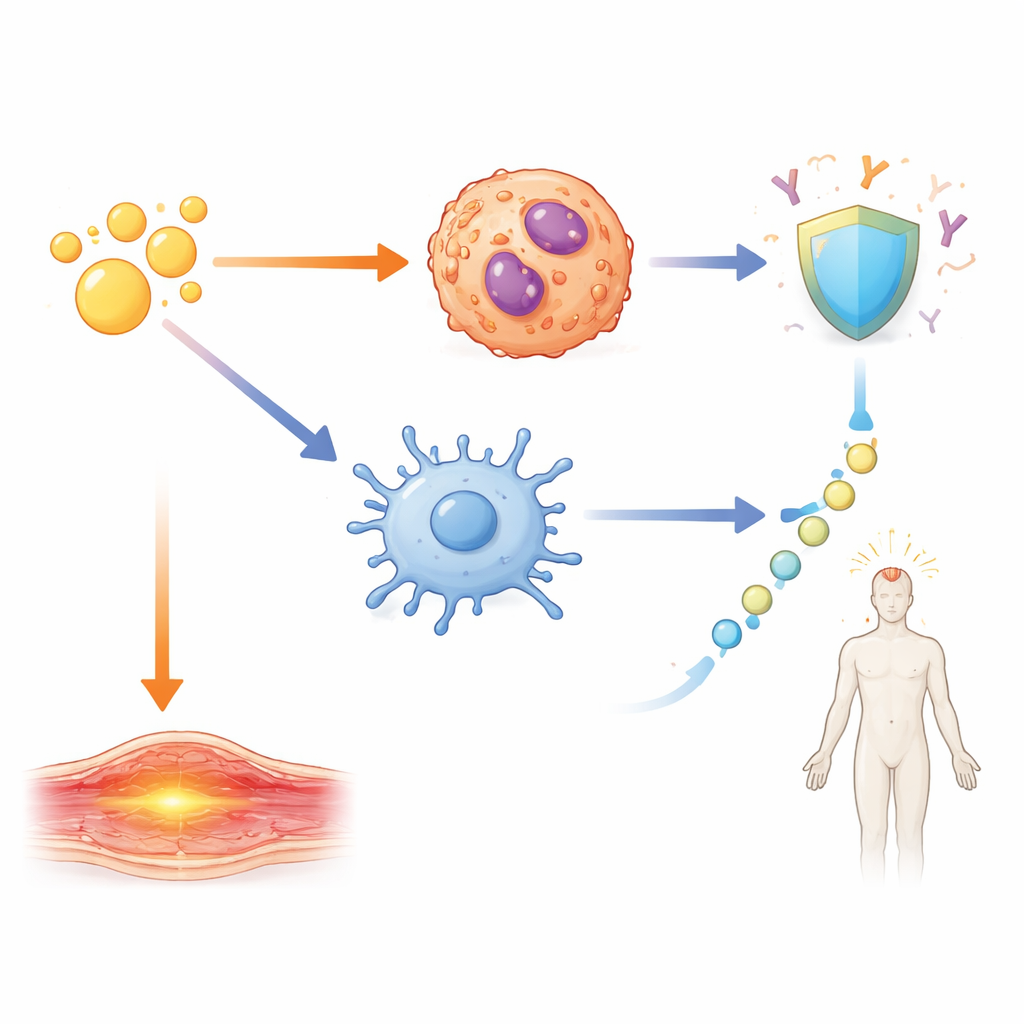
Van muizen naar mensen
Om te controleren of deze bevindingen ook voor mensen relevant kunnen zijn, stelden de onderzoekers bloedcellen van gezonde vrijwilligers in het lab bloot aan verschillende adjuvantia. Net als bij muizen zetten squalene-emulsies met α-tocoferol eosinofielen aan tot het produceren van IL-1α, terwijl vergelijkbare emulsies zonder α-tocoferol dat niet deden. Andere typen adjuvantia, waaronder aluminiumzouten en saponine-gebaseerde formuleringen, produceerden weinig tot geen IL-1α in eosinofielen. Dit suggereert dat door α-tocoferol aangedreven IL-1-signaleringsreacties, met name in eosinofielen, een kenmerkend vingerafdruk zijn van deze adjuvantiafamilie en als marker voor lokale reactogeniciteit in toekomstige humane studies kunnen dienen.
Veiliger en krachtiger vaccins ontwerpen
Al met al toont de studie aan dat hetzelfde adjuvans verschillende celtypen en signaalroutes kan gebruiken om bescherming te genereren en om kortdurende reacties te veroorzaken. IL-1β die via dendritische cellen werkt is essentieel voor sterke, langdurige antilichaamreacties, terwijl IL-1α uit eosinofielen en een IL-1β–IL-6–COX2-keten zwelling en koorts regelen. Voor vaccinontwerp betekent dit dat werkzaamheid en reactogeniciteit niet onveranderlijk aan elkaar gekoppeld zijn; ze kunnen in principe onafhankelijk worden bijgestuurd. Door de specifieke takken die bijwerkingen aandrijven te richten of te moduleren — zonder de tak die immuniteit aandrijft te verstoren — zouden toekomstige adjuvantia vaccins kunnen opleveren die zowel zeer effectief als gemakkelijker te verdragen zijn.
Bronvermelding: Yoshioka, Y., Nishinaka-Yoshioka, A., Kobiyama, K. et al. IL-1 delineates squalene-based adjuvant efficacy and reactogenicity in a cell-type-specific manner. npj Vaccines 11, 67 (2026). https://doi.org/10.1038/s41541-026-01420-0
Trefwoorden: vaccin-adjuvantia, squalene-emulsie, interleukine-1, reactogeniciteit, alpha-tocoferol