Clear Sky Science · sv
Proviral NUP153 bindning till virusproteiner och RNA reglerar förhållandet mellan strukturella och icke-strukturella proteiner vid ortoflavivirusinfektion
Hur virus förvandlar cellens grindvakt till en medhjälpare
Många farliga virus som sprids av myggor och fästingar, inklusive de som orsakar dengue, Zika, West Nile-feber och fästingburen encefalit, saknar fortfarande specifika behandlingar. Denna studie visar hur dessa virus kapar ett mänskligt protein kallat NUP153—normalt en del av cellens grindvakt runt kärnan—för att öka sin egen produktion. Att förstå denna bortkapning på molekylär nivå kan öppna för breda antivirala strategier som riktar sig mot värden i stället för mot viruset.
En virusfamilj utan botemedel
Orthoflavivirus är små RNA-virus som bärs av myggor och fästingar och kan orsaka allvarliga hjärninfektioner, blödningssjukdomar och livslånga komplikationer. Deras genom är en enda lång RNA‑sträng som avläses till ett jättestort polyprotein, vilket sedan klyvs till tio delar: tre som bildar virusets kapsid och sju som fungerar som interna verktyg för kopiering och sammanfogning av nya partiklar. För att föröka sig ombyggnad dessa virus cellens endoplasmatiska retikulum (ER)—ett membrannätverk nära kärnan—till en specialiserad "förstärkningsplats" där virus‑RNA kopieras, proteiner tillverkas och nya partklar monteras. Eftersom det inte finns godkända antivirala läkemedel för denna grupp, undersöker forskare i allt högre grad viktiga värdfaktorer som virusen är beroende av som potentiella läkemedelsmål.
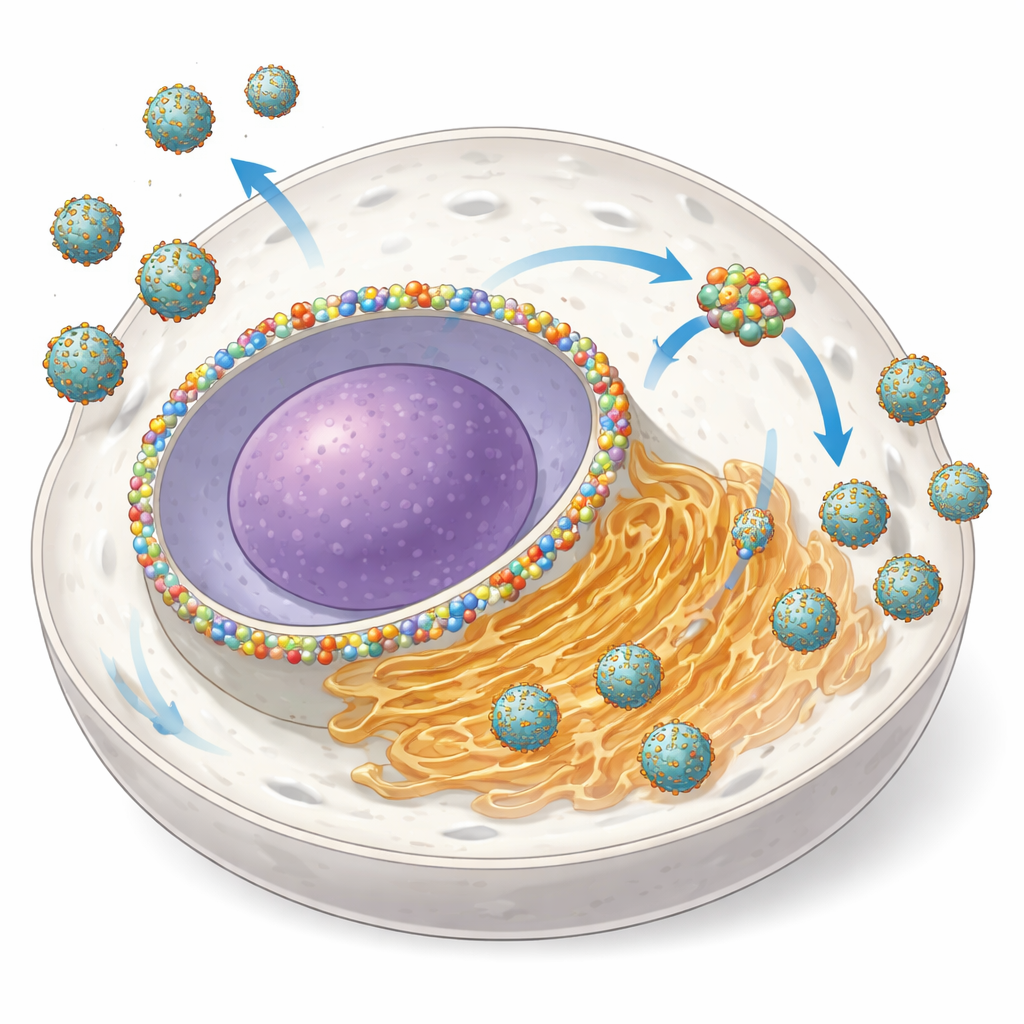
Att förvandla en kärnport till en virusverkstad
NUP153 är vanligtvis en komponent i nukleoporinkomplexet, en enorm struktur som reglerar trafik av RNA och proteiner mellan kärnan och det omgivande cytoplasman. Författarna upptäckte att under infektion med flera orthoflavivirus ökar cellerna mängden NUP153 och omfördelar en del av det från kärnmembranet till ER‑baserade virusförstärkningsplatser. Med avancerad mikroskopi visade de att NUP153 klustrar ihop sig med virusproteinerna NS3 och NS5 och med virus‑RNA nära ER‑membran, samtidigt som det i stort sett är skilt från de små vesikler där själva RNA‑kopieringen sker. När de snabbt degraderade NUP153 i genmodifierade celler minskade antalet infekterade celler och mängden utsläppt virus sjönk med upp till 80–95 %, särskilt tidigt i infektionen—tydliga tecken på att NUP153 fungerar som en "proviral" medhjälpare.
Direkt kontakt med virusproteiner och RNA
För att förstå hur NUP153 hjälper viruset drog forskarna ner NUP153 från infekterade celler och identifierade dess partners med masspektrometri och RNA‑sekvensering. De fann att NUP153 binder direkt till två viktiga virala enzymer, NS3 och NS5, utan att behöva RNA som brygga, och att det också fäster vid specifika regioner av det virala RNA:t självt. En av dessa RNA‑regioner ligger i slutet av genavsnittet som kodar för ytproteinet E och är rik på nukleotiden guanin. Detta stycke är starkt bevarat bland många orthoflavivirus, vilket antyder en viktig gemensam funktion. Biofysiska tester visade att NUP153:s RNA‑bindande domän känner igen denna G‑rika sekvens, särskilt när den inte är veckad till en kompakt fyrsträngad "G‑kvadrupel". Samma domän krävs också för att NUP153 ska flytta från kärnan till virusets förstärkningsplats och för att viruset ska replikera effektivt.
Omfördelning av virusets delar
Nya viruspartiklar kan bara bildas om cellen producerar rätt blandning av strukturella och icke‑strukturella proteiner från det enda virala polyproteinet. Forskarna testade om NUP153 påverkar denna balans. I in vitro‑översättningsförsök med virusliknande RNA ändrade tillsats av NUP153:s RNA‑bindande domän vilka proteinprodukter som bildades: den minskade produktionen av en nedströms rapportör samtidigt som den gynnade kortare produkter som motsvarar de strukturella proteinerna. I infekterade celler utan NUP153 sjönk den totala nivån av virala proteiner, men förhållandena förändrades: strukturella proteiner som E var relativt underrepresenterade, medan flera icke‑strukturella proteiner (inklusive NS1, NS2B, NS3 och NS5) blev mer rikliga i förhållande till E. Denna förskjutning berodde inte på snabbare proteinnedbrytning, utan tyder istället på förändrad översättning av det virala polyproteinet. Som en följd hade virus i NUP153‑defekta celler svårt att tidigt montera och släppa kompletta partiklar, vilket fördröjde spridningen till närliggande celler.
En gemensam svag punkt hos flera virus
Författarna breddade sina observationer bortom ett enda virus. Vid infektion med Zika, japansk encefalit, West Nile, gula febern och dengue förflyttade sig NUP153 återigen mot platser med virus‑RNA och dess avlägsnande minskade konsekvent både andelen infekterade celler och antalet producerade avkomspartklar. Eftersom den G‑rika RNA‑motiven som rekryterar NUP153 är bevarad över denna virusfamilj, och eftersom NUP153:s roll är att finslipa proteinblandningen som behövs för partikelmontering, föreslår studien en gemensam, utnyttjbar sårbarhet. Att rikta in sig på interaktionen mellan NUP153, virus‑RNA och virusproteiner—utan nödvändigtvis att förstöra NUP153:s väsentliga hushållsfunktioner—skulle kunna erbjuda en ny värdriktad strategi för bredspektrumantivirala medel.
Varför detta är viktigt för framtida behandlingar
I vardagliga termer visar arbetet att dessa virus utnyttjar en cellulär grindvakt och omvandlar den till en produktionschef, som styr cellen att tillverka fler av de yttre delarna som behövs för att bygga nya viruspartiklar vid rätt tidpunkt. När NUP153 tas bort eller blockeras blir "delistan" obalanserad: det finns gott om interna verktyg men inte tillräckligt med skaldelar, så betydligt färre infektiösa partiklar uppstår, särskilt tidigt i infektionen när timing är viktigast. Eftersom denna strategi verkar vara bevarad bland många medicinskt betydelsefulla flavivirus, kan en noggrant utformad störning av detta kapade samarbete mellan viruset och NUP153 en dag bidra till att förebygga eller begränsa svåra infektioner från en hel familj av i dag svårbehandlade patogener.
Citering: Peters, M.B.A., Lindqvist, R., Kassa, E. et al. Proviral NUP153 binding to viral proteins and RNA regulates structural–nonstructural protein ratios in orthoflavivirus infection. Nat Commun 17, 3402 (2026). https://doi.org/10.1038/s41467-026-71449-1
Nyckelord: orthoflavivirus, NUP153, översättning av virusproteiner, värd–virus-interaktion, Brett spektrum antivirala medel