Clear Sky Science · he
קשירת NUP153 פרו-ויראלית לחלבוני הוירוס ול‑RNA מווסתת את יחס החלבונים המבניים־הלא־מבניים בזיהום אורתופלביוויס
כיצד וירוסים הופכים שומר סף של התא לעוזר
רבים מהוירוסים המסוכנים שמועברים על‑ידי יתושים וקרציות, כולל אלה הגורמים לדנגי, זיקה, קדחת מערב הנילוס ודלקת המוח הנשאית בקרציות, עדיין אין להם טיפולים ספציפיים. המחקר הזה חושף כיצד וירוסים אלה חוטפים חלבון אנושי בשם NUP153—שלרוב מהווה חלק ממערכת השמירה סביב הגרעין—כדי להגביר את ייצורם. הבנת השתלטות זו ברמת המולקולה עשויה לפתוח דלת לאסטרטגיות אנטי‑ויראליות רחבות חדשות שמכוונות למארח במקום לוירוס.
משפחה של וירוסים ללא תרופה
אורתופלביוויסים הם וירוסים קטנים בעלי RNA הנישאים על ידי יתושים וקרציות, ויכולים לגרום לדלקות מוח קשות, מחלות מדממות וסיבוכים לכל החיים. הגנום שלהם הוא גדיל RNA ארוך שנקרא אחד ליצירת פוליפרוטאין ענק, שמפורק אחר כך לעשר יחידות: שלוש בונות את מעטפת הוירוס ושבע משמשות ככלים פנימיים להעתקה ולהרכבה של חלקיקים חדשים. כדי להתרבות, וירוסים אלה מעצבים מחדש את הרשת הקרומית של הרטיקולום האנדופלזמי (ER) — ממברנה סמוכה לגרעין — לאתר התמחות של "הגברה" שבו מעתיקים את ה‑RNA הויראלי, מייצרים חלבונים ומרכיבים חלקיקים חדשים. מאחר שאין תרופות מאושרות לקבוצה זו, חוקרים פונים יותר ויותר לגורמי מארח חיוניים שעליהם הוירוסים נשענים כיעד פוטנציאלי לטיפול.
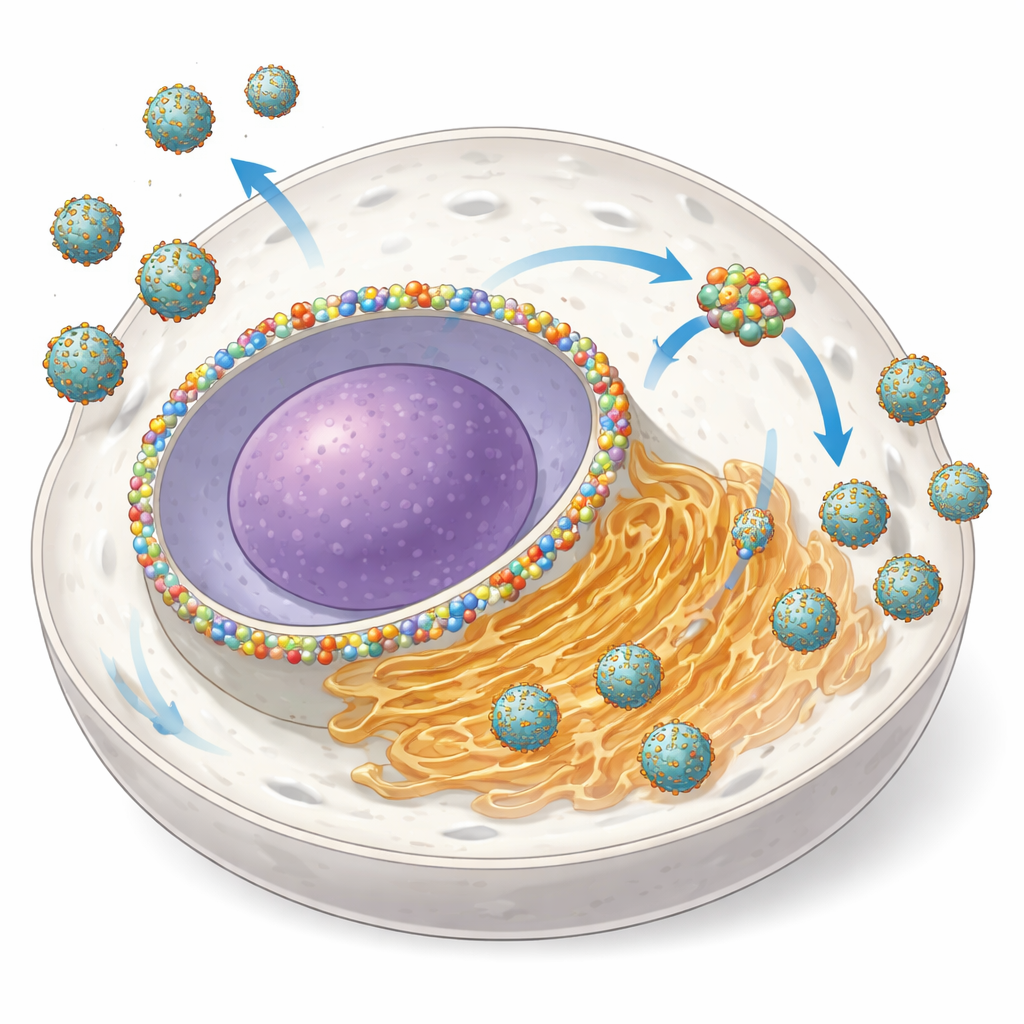
הפיכת שער גרעיני למפעל ויראלי
NUP153 בדרך‑כלל מהווה מרכיב של קומפלקס נקבובית הגרעין (nuclear pore complex), מבנה עצום שמווסת תנועה של RNA וחלבונים בין הגרעין לציטופלזמה. החוקרים גילו שבמהלך זיהום במספר אורתופלביוויסים, תאים מעלים את הכמות של NUP153 ומפזרים חלק ממנה ממעטפת הגרעין אל אתר ההגברה התלוי ב‑ER. באמצעות מיקרוסקופיה מתקדמת הראו כי NUP153 מאטם יחד עם חלבוני הוירוס NS3 ו‑NS5 ועם RNA ויראלי בסמיכות לממברנות ה‑ER, בעוד שהוא נשאר ברובו מופרד מהוואזיקולות הקטנות שבהן מתרחשת שעתוק ה‑RNA עצמו. כאשר פירקו במהירות את NUP153 בתאים מהונדסים, מספר התאים הנדבקים ירד וכמות הוירוס המשוחררת פחתה עד 80–95%—בייחוד בשלבים המוקדמים של הזיהום—מה שמעיד ש‑NUP153 פועל כעוזר "פרו‑ויראלי".
מגע ישיר עם חלבוני הוירוס ו‑RNA
כדי להבין כיצד NUP153 מסייע לווירוס, החוקרים ביצעו משיכה של NUP153 מתאים מזוהמים וזיהו את שותפיו באמצעות ספקטרומטריה של מסה וריצוף RNA. הם מצאו ש‑NUP153 קושר ישירות שני אנזימים ויראליים מרכזיים, NS3 ו‑NS5, ללא צורך ב‑RNA כגשר, וכן נצמדה לאזורי RNA ספציפיים של הוירוס עצמו. אחד האזורים הללו נמצא בסוף מקטע הגן המקודד לחלבון המעטפה החיצוני E ועשיר בניוקלאוטיד גואנין. מקטע זה שמור בחוזקה בין רבים מאורתופלביוויסים, רמז לפונקציה משותפת חשובה. ניסויים בביופיזיקה הראו שתחום קשירת ה‑RNA של NUP153 מזהה את הרצף העשיר‑G הזה, במיוחד כשהוא אינו מקופל לצורת "G‑קוואדראפלקס" צפופה בעלת ארבע גלים. אותו תחום גם נחוץ ליציאת NUP153 מהגרעין אל אתר ההגברה הויראלי ולרפליקציה יעילה של הוירוס.
איזון מחדש של רשימת הרכיבים הויראלית
חלקיקים ויראליים חדשים יכולים להיווצר רק אם התא מייצר את התמהיל הנכון של חלבונים מבניים ולא־מבניים מהפוליפרוטאין הויראלי האחד. הקבוצה בדקה האם NUP153 משפיע על איזון זה. בניסויי תרגום מבחנה עם RNA המדמה את הוירוס, הוספת תחום קשירת ה‑RNA של NUP153 שינתה אילו תוצרי חלבון נוצרים: היא הקטינה את הייצור של מדד במיקום האחורי בעוד שהיא הטביעה קיטון בתוצרים ארוכים יותר והעדיפה תוצרים קצרים יותר התואמים לחלבונים המבניים. בתאים מודבקים חסרי NUP153 רמות החלבון הויראלי הכוללות ירדו, אך היחסים השתנו: חלבונים מבניים כמו E היו יחסית חסרים יותר, בעוד מספר חלבונים לא‑מבניים (כולל NS1, NS2B, NS3 ו‑NS5) הפכו לשכיחים יותר ביחס ל‑E. שינוי זה לא נבע מפירוק מהיר יותר של חלבונים, אלא מרמז על תרגום שונה של הפוליפרוטאין הויראלי. כתוצאה מכך, בשלבים המוקדמים של הזיהום, וירוסים בתאים חסרי NUP153 נאבקו בהרכבה ובשחרור של חלקיקים שלמים, ומאחרים להדביק תאים שכנים.
נקודת חולשה משותפת למספר וירוסים
המחברים הרחיבו את התצפיות שלהם מעבר לוירוס יחיד. במהלך זיהום בזיקה, דלקת מוח יפנית, מערב הנילוס, קדחת צהובה ודנגי, NUP153 שוב נדד לאתרי ה‑RNA הויראלי והסרתו הקטינה בעקביות הן את החלק של התאים הנדבקים והן את מספר החלקיקים שהופקו. מאחר שמוטיב ה‑G‑עשיר שמגייס את NUP153 שמור לאורך משפחת הוירוסים הזו, וכיוון שתפקידו של NUP153 הוא לכוונן את תמהיל החלבונים הדרוש להרכבת חלקיקים, המחקר מציע נקודת תורפה משותפת שניתן לנצל. מיקוד האינטראקציה בין NUP153, ה‑RNA הויראלי וחלבוני הוירוס—בלי לפגוע בהכרח בתפקידי הבית החיוניים של NUP153—יכול לספק יום אחד אסטרטגיה מכוונת למארח לאנטי‑וירוסים רחבי‑טווח.
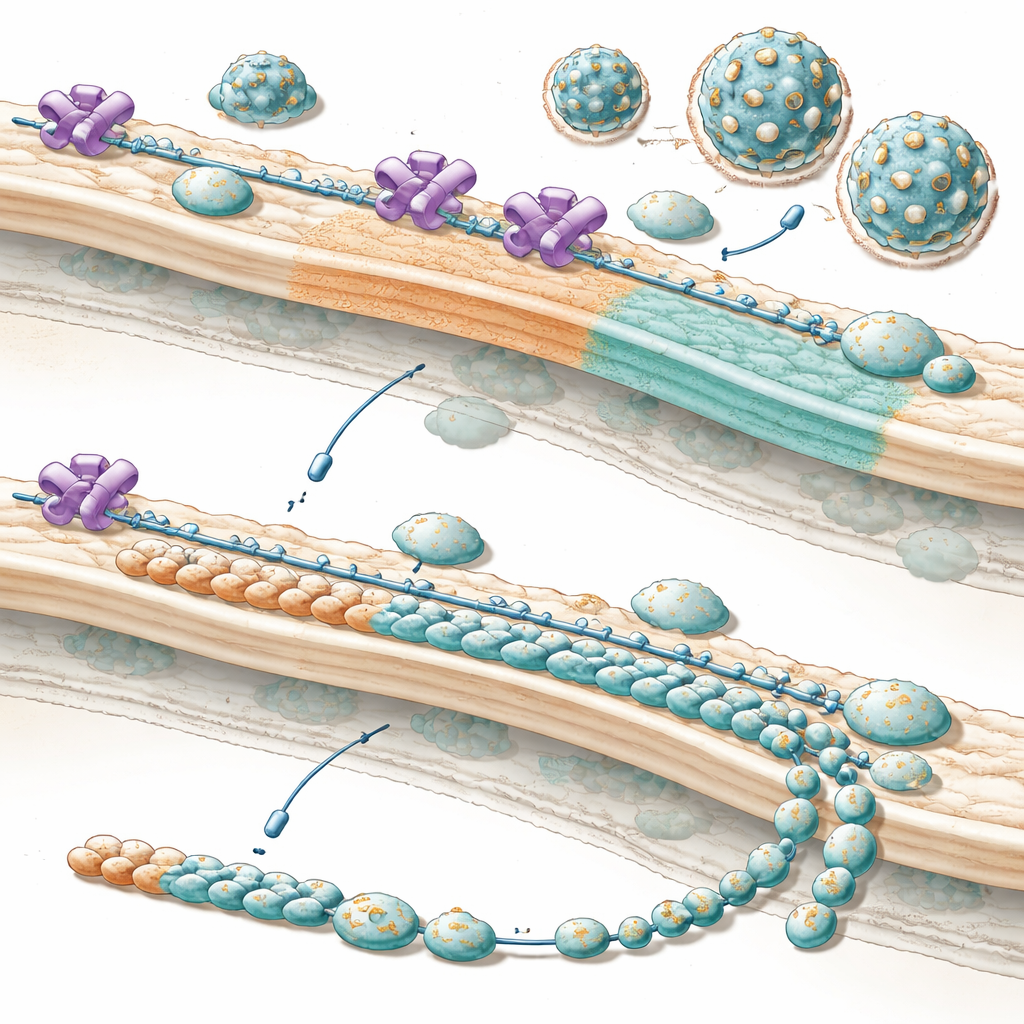
מדוע זה חשוב עבור טיפולים עתידיים
במילים פשוטות, העבודה מראה שוירוסים אלה מטעינים שומר סף תאי ומייעדים אותו כמנהל ייצור, שמכוון את התא לייצר יותר מרכיבים חיצוניים הדרושים לבניית חלקיקים חדשים בדיוק בזמן המתאים. כאשר NUP153 מוסר או נחסם, "רשימת החלקים" מאבדת איזון: יש שפע של כלים פנימיים, אבל לא מספיק חתיכות מעטפת, ולכן יוצאים הרבה פחות חלקיקים מדבקים—במיוחד בשלבי הזיהום המוקדמים שבהם הזמנים קריטיים. מכיוון שאסטרטגיה זו נראית שמורה בקרב רבים מהפלביוויסים החשובים ברפואה, הפרעה מושכלת לשותפות החטופה בין הוירוס ל‑NUP153 עשויה יום אחד לסייע במניעה או בהגבלת זיהומים קשים מצד משפחה של פתוגנים שקשה לטפל בהם כיום.
ציטוט: Peters, M.B.A., Lindqvist, R., Kassa, E. et al. Proviral NUP153 binding to viral proteins and RNA regulates structural–nonstructural protein ratios in orthoflavivirus infection. Nat Commun 17, 3402 (2026). https://doi.org/10.1038/s41467-026-71449-1
מילות מפתח: אורתופלביוויס, NUP153, תרגום חלבוני ויראלי, אינטראקציה מארח–וירוס, נוגדי‑וירוס רחבי‑טווח