Clear Sky Science · pl
Wiązanie prowirusowe NUP153 z białkami wirusowymi i RNA reguluje stosunek białek strukturalnych do niestrukturalnych w zakażeniu orthoflawirusem
Jak wirusy zamieniają strażnika komórki w pomocnika
Wiele niebezpiecznych wirusów przenoszonych przez komary i kleszcze, w tym wywołujące dengę, Zikę, gorączkę Zachodniego Nilu i kleszczowe zapalenie mózgu, wciąż nie ma specyficznych terapii. Badanie to ujawnia, w jaki sposób te wirusy przejmują ludzkie białko o nazwie NUP153 — normalnie będące elementem systemu kontroli przy jądrze komórkowym — aby zwiększyć własną produkcję. Zrozumienie tego przejęcia na poziomie molekularnym może otworzyć drogę do nowych strategii przeciwwirusowych o szerokim spektrum, które celowałyby w gospodarza zamiast w sam wirus.
Rodzina wirusów bez leku
Orthoflawirusy to małe wirusy RNA przenoszone przez komary i kleszcze, które mogą powodować ciężkie infekcje mózgu, choroby krwotoczne i długotrwałe powikłania. Ich genom to pojedyncza długa nić RNA, która jest odczytywana jako jeden gigantyczny poliprotein, następnie pocięty na dziesięć fragmentów: trzy tworzą osłonkę wirusa, a siedem pełni role wewnętrznych narzędzi do kopiowania i składania nowych cząstek. Aby się namnażać, te wirusy przebudowują siateczkę śródplazmatyczną (ER) — sieć błon w pobliżu jądra — w wyspecjalizowane „miejsce amplifikacji”, gdzie kopiowane jest RNA wirusa, syntetyzowane białka i składane nowe cząstki wirusa. Ponieważ dla tej grupy nie istnieją zatwierdzone leki przeciwwirusowe, naukowcy coraz częściej badają niezbędne czynniki gospodarza, od których wirusy zależą, jako potencjalne cele terapeutyczne.
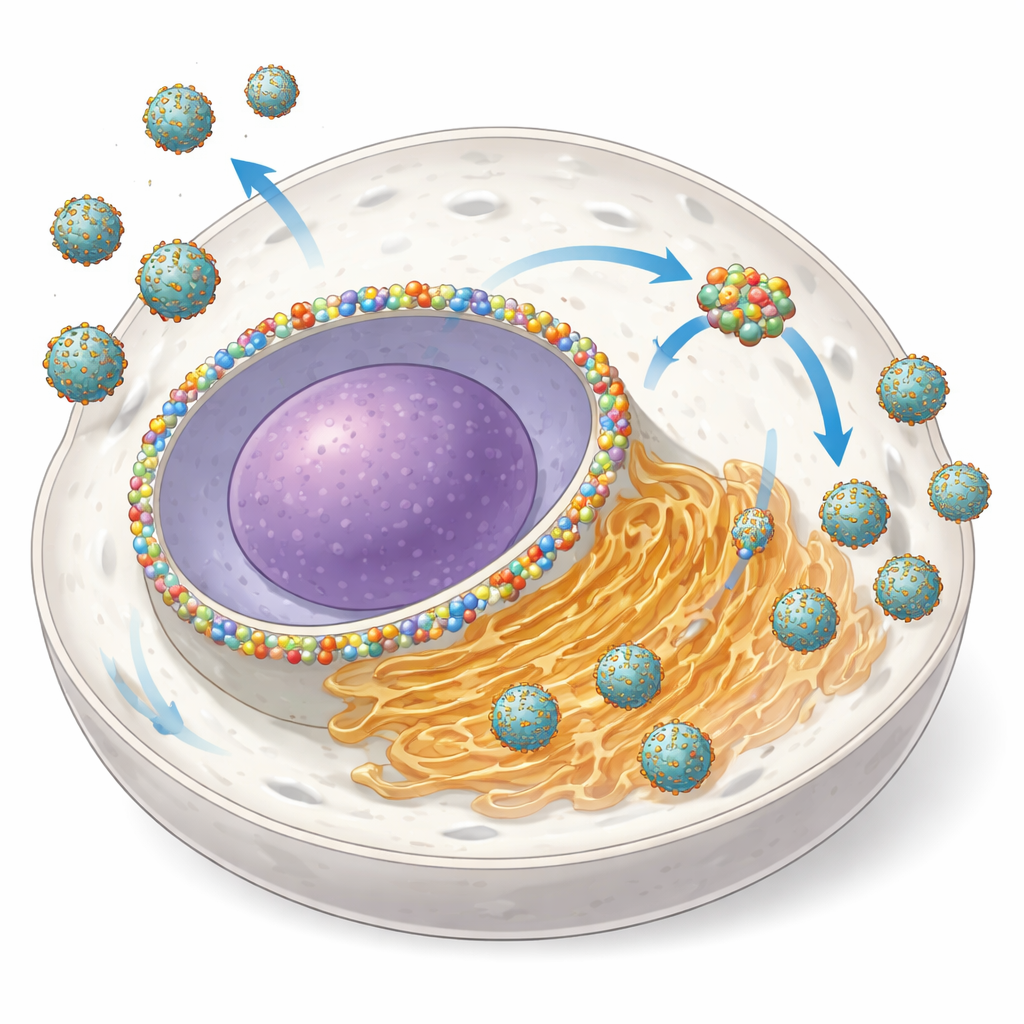
Przekształcenie bramki jądrowej w warsztat wirusa
NUP153 jest zwykle składnikiem kompleksu porów jądrowych, ogromnej struktury regulującej ruch RNA i białek między jądrem a otaczającą cytoplazmą. Autorzy odkryli, że podczas zakażenia kilkoma orthoflawirusami komórki zwiększają ilość NUP153 i redystrybuują część tego białka z otoczki jądrowej do opartego na ER miejsca amplifikacji wirusa. Za pomocą zaawansowanej mikroskopii pokazali, że NUP153 skupia się razem z białkami wirusowymi NS3 i NS5 oraz z RNA wirusa w pobliżu błon ER, pozostając w dużej mierze odseparowanym od małych pęcherzyków, gdzie samo kopiowanie RNA zachodzi. Gdy szybko usuwali NUP153 w zmodyfikowanych komórkach, liczba zakażonych komórek spadła, a ilość uwolnionego wirusa zmniejszyła się nawet o 80–95%, szczególnie we wczesnym etapie zakażenia — wyraźne oznaki, że NUP153 działa jako prowirusowy pomocnik.
Bezpośredni kontakt z białkami wirusa i RNA
Aby zrozumieć, jak NUP153 pomaga wirusowi, badacze izolowali NUP153 z zakażonych komórek i identyfikowali jego partnerów za pomocą spektrometrii mas i sekwencjonowania RNA. Stwierdzili, że NUP153 bezpośrednio wiąże dwa kluczowe enzymy wirusowe, NS3 i NS5, bez potrzeby obecności RNA jako mostka, oraz przyczepia się do specyficznych regionów samego RNA wirusa. Jeden z tych regionów znajduje się na końcu segmentu genowego kodującego zewnętrzne białko osłonowe E i jest bogaty w nukleotyd guaninę. Ten fragment jest silnie zachowany w wielu orthoflawirusach, co sugeruje ważną wspólną funkcję. Testy biofizyczne wykazały, że domena wiążąca RNA NUP153 rozpoznaje tę sekwencję bogatą w G, szczególnie gdy nie jest ona złożona w zwartą, czterniciową strukturę „G-quadruplex”. Ta sama domena jest również wymagana, by NUP153 przeniósł się z jądra do miejsca amplifikacji wirusa i by wirus efektywnie się replikował.
Przestawienie listy części wirusa
Nowe cząstki wirusa mogą powstać tylko wtedy, gdy komórka wytworzy właściwy miks białek strukturalnych i niestrukturalnych z pojedynczego poliproteiny wirusowego. Zespół sprawdził, czy NUP153 wpływa na to wyważenie. W doświadczeniach translacyjnych in vitro wykorzystujących RNA przypominające wirus, dodanie domeny wiążącej RNA NUP153 zmieniło, które produkty białkowe były wytwarzane: zmniejszyło produkcję dalszego reportera przy jednoczesnym faworyzowaniu krótszych produktów odpowiadających białkom strukturalnym. W zakażonych komórkach pozbawionych NUP153 całkowity poziom białek wirusowych spadł, ale proporcje uległy zmianie: białka strukturalne, takie jak E, były relatywnie niedoreprezentowane, podczas gdy kilka białek niestrukturalnych (w tym NS1, NS2B, NS3 i NS5) stało się bardziej obfitych względem E. Ta zmiana nie wynikała ze szybszego rozpadu białek, lecz z zaburzonego tłumaczenia poliproteiny wirusowej. W efekcie, we wczesnym etapie zakażenia wirusy w komórkach pozbawionych NUP153 miały trudności z złożeniem i uwolnieniem kompletnych cząstek, opóźniając rozprzestrzenianie się na sąsiednie komórki.
Wspólny słaby punkt wielu wirusów
Autorzy rozszerzyli swoje obserwacje poza pojedynczy wirus. Podczas zakażeń wirusami Zika, japońskiego zapalenia mózgu, Zachodniego Nilu, żółtej gorączki i dengą, NUP153 ponownie przesuwał się w kierunku miejsc z RNA wirusa, a jego usunięcie konsekwentnie zmniejszało zarówno odsetek zakażonych komórek, jak i liczbę wytwarzanych cząstek potomnych. Ponieważ motyw RNA bogaty w G, który rekrutuje NUP153, jest zachowany w całej tej rodzinie wirusów, a rola NUP153 polega na dopracowaniu mieszanki białek potrzebnych do składania cząstek, badanie sugeruje wspólną, możliwą do wykorzystania podatność. Celowanie w interakcję między NUP153, RNA wirusa i białkami wirusa — bez konieczności niszczenia zasadniczych funkcji porządkowych NUP153 — mogłoby dostarczyć nowej strategii skierowanej na gospodarza dla leków o szerokim spektrum.
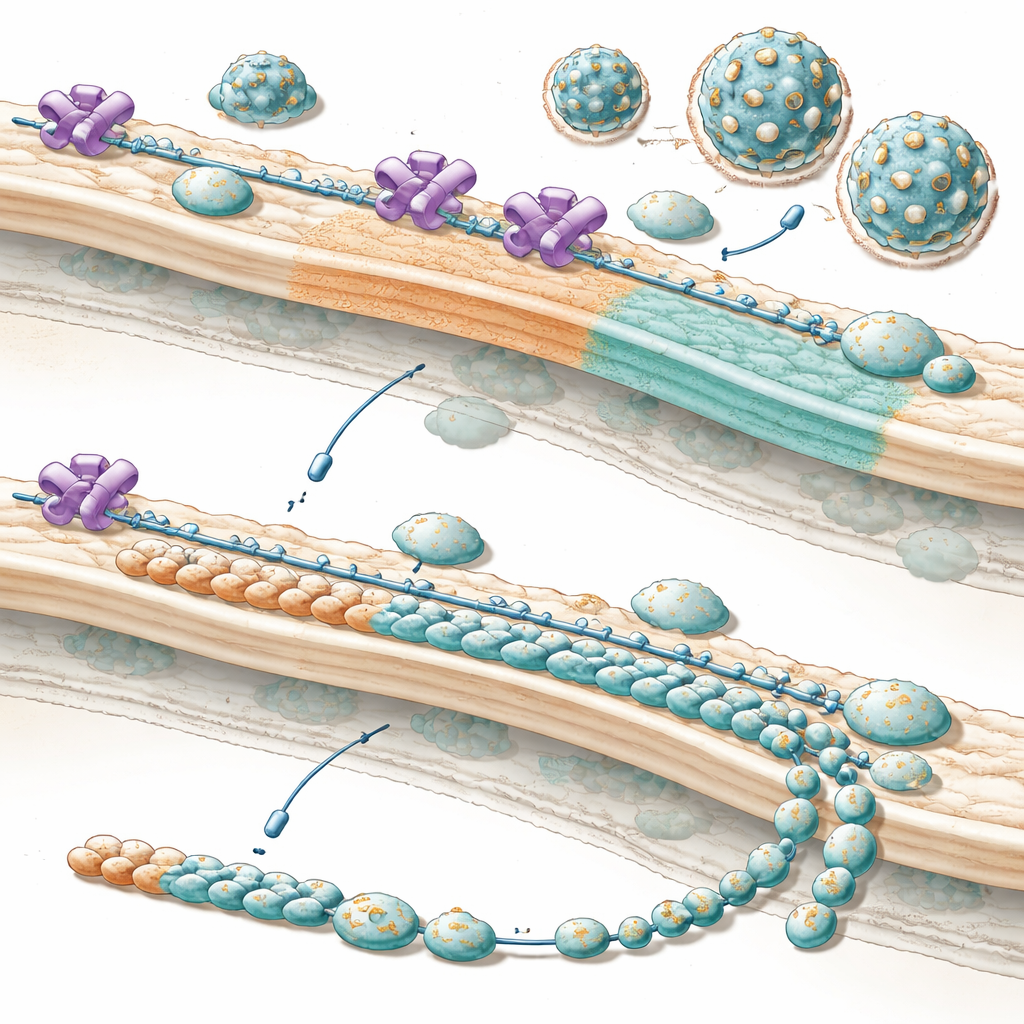
Dlaczego to ma znaczenie dla przyszłych terapii
Mówiąc prościej, praca pokazuje, że te wirusy wykorzystują komórkowego strażnika i przekształcają go w kierownika produkcji, nakierowując komórkę, by wytwarzała więcej zewnętrznych elementów potrzebnych do zbudowania nowych cząstek wirusa we właściwym momencie. Gdy NUP153 zostaje usunięty lub zablokowany, „lista części” staje się niezrównoważona: jest dużo narzędzi wewnętrznych, lecz za mało elementów osłonowych, w efekcie znacznie mniej powstaje zakaźnych cząstek, zwłaszcza we wczesnym etapie zakażenia, kiedy czas ma kluczowe znaczenie. Ponieważ strategia ta wydaje się być zachowana wśród wielu medycznie istotnych flawiwirusów, ostrożne zakłócenie tego przejętego partnerstwa między wirusem a NUP153 może pewnego dnia pomóc zapobiegać lub ograniczać ciężkie zakażenia całej rodziny obecnie trudnych do leczenia patogenów.
Cytowanie: Peters, M.B.A., Lindqvist, R., Kassa, E. et al. Proviral NUP153 binding to viral proteins and RNA regulates structural–nonstructural protein ratios in orthoflavivirus infection. Nat Commun 17, 3402 (2026). https://doi.org/10.1038/s41467-026-71449-1
Słowa kluczowe: orthoflavivirus, NUP153, tłumaczenie białek wirusowych, interakcja gospodarza z wirusem, leki przeciwwirusowe o szerokim spektrum