Clear Sky Science · de
Provirale NUP153-Bindung an Virusproteine und RNA reguliert das Verhältnis von Struktur- zu Nichtstrukturproteinen bei einer Orthoflavivirus-Infektion
Wie Viren den zellulären Türsteher zum Helfer machen
Viele gefährliche, von Mücken und Zecken übertragene Viren – darunter Erreger von Dengue, Zika, West-Nil-Fieber und zeckenübertragener Enzephalitis – haben nach wie vor keine spezifischen Therapien. Diese Studie zeigt, wie diese Viren ein menschliches Protein namens NUP153 kapern – normalerweise Bestandteil des zellulären Torwächters rund um den Zellkern – und es zur Steigerung ihrer eigenen Produktion nutzen. Das molekulare Verständnis dieser Übernahme könnte den Weg zu breiten neuen antiviralen Ansätzen öffnen, die den Wirt statt das Virus anvisieren.
Eine Virusfamilie ohne Heilmittel
Orthoflaviviruses sind kleine RNA-Viren, die von Mücken und Zecken übertragen werden und schwere Hirninfektionen, hämorrhagische Krankheitsverläufe und lebenslange Komplikationen verursachen können. Ihr Genom besteht aus einem einzelnen langen RNA-Strang, der als ein großes Polyprotein abgelesen wird, das anschließend in zehn Teile geschnitten wird: drei bilden die Virushülle, sieben dienen als interne Werkzeuge zum Kopieren und Zusammenbauen neuer Partikel. Zum Vermehren bauen diese Viren das endoplasmatische Retikulum (ER) der Zelle – ein Membrannetzwerk in Kernnähe – in eine spezialisierte „Verstärkungsstelle“ um, in der virale RNA kopiert, Proteine synthetisiert und neue Viruspartikel montiert werden. Da für diese Gruppe keine zugelassenen antiviralen Medikamente existieren, richten Forscher ihr Augenmerk zunehmend auf essentielle Wirtsfaktoren, auf die Viren angewiesen sind und die als potenzielle Wirkziele dienen könnten.
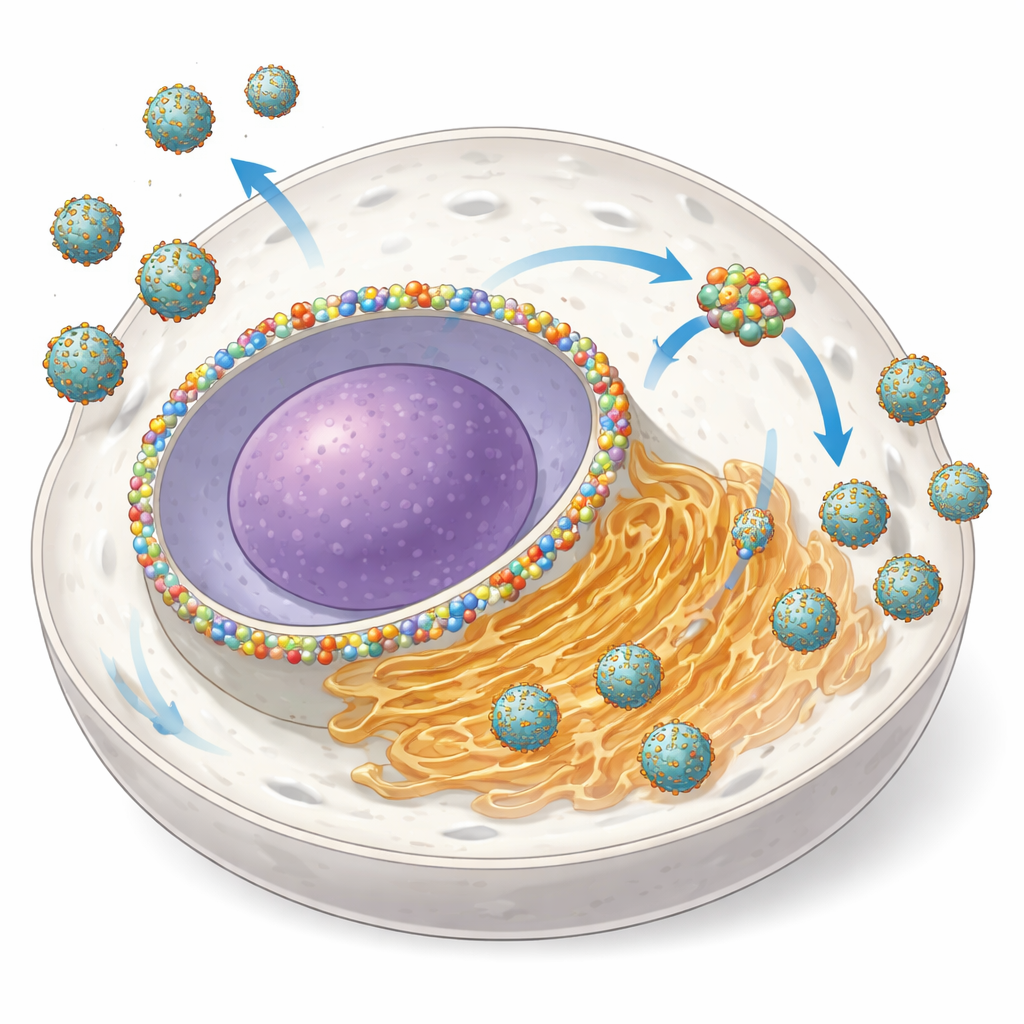
Aus einem nukleären Tor wird eine Viruswerkstatt
NUP153 ist gewöhnlich Bestandteil des Kernporenkomplexes, einer riesigen Struktur, die den Verkehr von RNA und Proteinen zwischen Kern und umgebendem Zytoplasma reguliert. Die Autoren entdeckten, dass Zellen während einer Infektion mit mehreren Orthoflaviviren die Menge an NUP153 erhöhen und einen Teil davon von der Kernhülle zu den ER-basierten viralen Verstärkungsstellen umverteilen. Mittels hochauflösender Mikroskopie zeigten sie, dass NUP153 sich zusammen mit den viralen Proteinen NS3 und NS5 sowie mit viraler RNA in der Nähe von ER-Membranen zu Clustern formiert, während es weitgehend getrennt von den kleinen Vesikeln bleibt, in denen die RNA-Replikation selbst stattfindet. Wenn sie NUP153 in gentechnisch veränderten Zellen rasch abbauten, sank die Zahl infizierter Zellen und die freigesetzte Virusmenge fiel um bis zu 80–95 %, besonders in frühen Infektionsphasen – klare Anzeichen dafür, dass NUP153 als „proviraler“ Helfer fungiert.
Direkter Kontakt mit Virusproteinen und RNA
Um zu verstehen, wie NUP153 dem Virus hilft, zogen die Forscher NUP153 aus infizierten Zellen heraus und identifizierten seine Partner mittels Massenspektrometrie und RNA-Sequenzierung. Sie fanden, dass NUP153 zwei wichtige virale Enzyme, NS3 und NS5, direkt bindet, ohne RNA als Brücke zu benötigen, und dass es sich außerdem an spezifische Regionen der viralen RNA anlagert. Eine dieser RNA-Regionen liegt am Ende des codierenden Abschnitts für das Außenschalenprotein E und ist reich an dem Nukleotid Guanin. Dieser Abschnitt ist über viele Orthoflaviviren hinweg stark konserviert, was auf eine gemeinsame wichtige Funktion hindeutet. Biophysikalische Tests zeigten, dass die RNA-bindende Domäne von NUP153 diese G-reiche Sequenz erkennt, insbesondere wenn sie nicht in eine kompakte, viersträngige „G-Quadruplex“-Struktur gefaltet ist. Dieselbe Domäne ist auch erforderlich, damit NUP153 vom Kern zur viralen Verstärkungsstelle umzieht und damit für eine effiziente Virusreplikation.
Umschichtung der viralen Teileliste
Neue Viruspartikel können nur entstehen, wenn die Zelle das richtige Verhältnis von Struktur- und Nichtstrukturproteinen aus dem einzigen viralen Polyprotein produziert. Das Team prüfte, ob NUP153 dieses Gleichgewicht beeinflusst. In In-vitro-Translationsversuchen mit viraler Nachahmer-RNA veränderte das Hinzufügen der RNA-bindenden Domäne von NUP153 die hergestellten Proteinprodukte: Die Produktion eines downstream liegenden Reporters wurde reduziert, während kürzere Produkte, die den Strukturproteinen entsprechen, bevorzugt wurden. In infizierten Zellen ohne NUP153 sanken die Gesamtviralproteinmengen, aber die Verhältnisse verschoben sich: Strukturproteine wie E waren relativ unterrepräsentiert, während mehrere Nichtstrukturproteine (darunter NS1, NS2B, NS3 und NS5) im Vergleich zu E häufiger waren. Diese Verschiebung rührte nicht von schnellerem Proteinabbau her, sondern deutet auf veränderte Translation des viralen Polyproteins hin. Infolgedessen hatten Viren in NUP153-defizienten Zellen in frühen Infektionsstadien Schwierigkeiten, komplette Partikel zusammenzubauen und freizusetzen, was die Ausbreitung auf Nachbarzellen verzögerte.
Eine gemeinsame Schwachstelle mehrerer Viren
Die Autoren erweiterten ihre Beobachtungen über ein einzelnes Virus hinaus. Bei Infektionen mit Zika-, Japanischer-Enzephalitis-, West-Nil-, Gelbfieber- und Dengue-Viren wanderte NUP153 ebenfalls zu Orten viraler RNA, und sein Entfernen verringerte durchweg sowohl den Anteil infizierter Zellen als auch die Anzahl produzierter Nachkommenpartikel. Da das G-reiche RNA-Motiv, das NUP153 anzieht, in dieser Virusfamilie konserviert ist und NUP153s Rolle darin besteht, das für den Partikelaufbau benötigte Proteinmischungsverhältnis fein abzustimmen, legt die Studie eine gemeinsame, ausnutzbare Verwundbarkeit nahe. Die gezielte Störung der Interaktion zwischen NUP153, viraler RNA und Virusproteinen – ohne notwendigerweise NUP153s essentielle Haushaltsfunktionen zu zerstören – könnte einen neuen, wirtgerichteten Ansatz für breit wirksame antivirale Mittel bieten.
Warum das für künftige Behandlungen wichtig ist
Anschaulich zeigt die Arbeit, dass diese Viren einen zellulären Türsteher kapern und ihn als Produktionsleiter umfunktionieren, sodass die Zelle zur rechten Zeit mehr von den äußeren Bauteilen herstellt, die zum Zusammenbau neuer Viruspartikel nötig sind. Wenn NUP153 entfernt oder blockiert wird, gerät die „Teileliste“ aus dem Gleichgewicht: Viele interne Werkzeuge sind vorhanden, aber zu wenige Hüllbestandteile, sodass deutlich weniger infektiöse Partikel entstehen, besonders früh in der Infektion, wenn Timing entscheidend ist. Da diese Strategie offenbar bei vielen medizinisch relevanten Flaviviren erhalten ist, könnte das gezielte Stören dieser gekaperten Partnerschaft zwischen Virus und NUP153 eines Tages helfen, schwere Erkrankungen durch eine ganze Familie derzeit schwer zu behandelnder Erreger zu verhindern oder abzumildern.
Zitation: Peters, M.B.A., Lindqvist, R., Kassa, E. et al. Proviral NUP153 binding to viral proteins and RNA regulates structural–nonstructural protein ratios in orthoflavivirus infection. Nat Commun 17, 3402 (2026). https://doi.org/10.1038/s41467-026-71449-1
Schlüsselwörter: orthoflavivirus, NUP153, Translation viraler Proteine, Wirt–Virus-Interaktion, breit wirkende antivirale Mittel