Clear Sky Science · fr
La liaison provirale de NUP153 aux protéines virales et à l’ARN régule les rapports protéines structurelles–non structurelles lors d’une infection par les orthoflavivirus
Comment les virus transforment le gardien de la cellule en un assistant
De nombreux virus dangereux transmis par les moustiques et les tiques, notamment ceux responsables de la dengue, du Zika, du virus du Nil occidental et de l’encéphalite à tiques, n’ont toujours pas de traitements spécifiques. Cette étude révèle comment ces virus détournent une protéine humaine appelée NUP153 — normalement partie intégrante du système de contrôle autour du noyau cellulaire — pour stimuler leur propre production. Comprendre ce détournement au niveau moléculaire pourrait ouvrir la voie à de nouvelles stratégies antivirales à large spectre ciblant l’hôte plutôt que le virus.
Une famille de virus sans remède
Les orthoflavivirus sont de petits virus à ARN véhiculés par les moustiques et les tiques, pouvant provoquer des infections cérébrales sévères, des formes hémorragiques et des complications durables. Leur génome est un long brin d’ARN traduit en une polyprotéine géante, ensuite clivée en dix fragments : trois qui forment l’enveloppe virale et sept qui agissent comme des outils internes pour copier et assembler de nouveaux virions. Pour se multiplier, ces virus réorganisent le réticulum endoplasmique (RE) de la cellule — un réseau membranaire proche du noyau — en un « site d’amplification » spécialisé où l’ARN viral est copié, les protéines sont synthétisées et de nouveaux particules virales sont assemblées. En l’absence de médicaments antiviraux approuvés pour ce groupe, les chercheurs s’intéressent de plus en plus aux facteurs essentiels de l’hôte sur lesquels les virus comptent, comme cibles potentielles de médicaments.
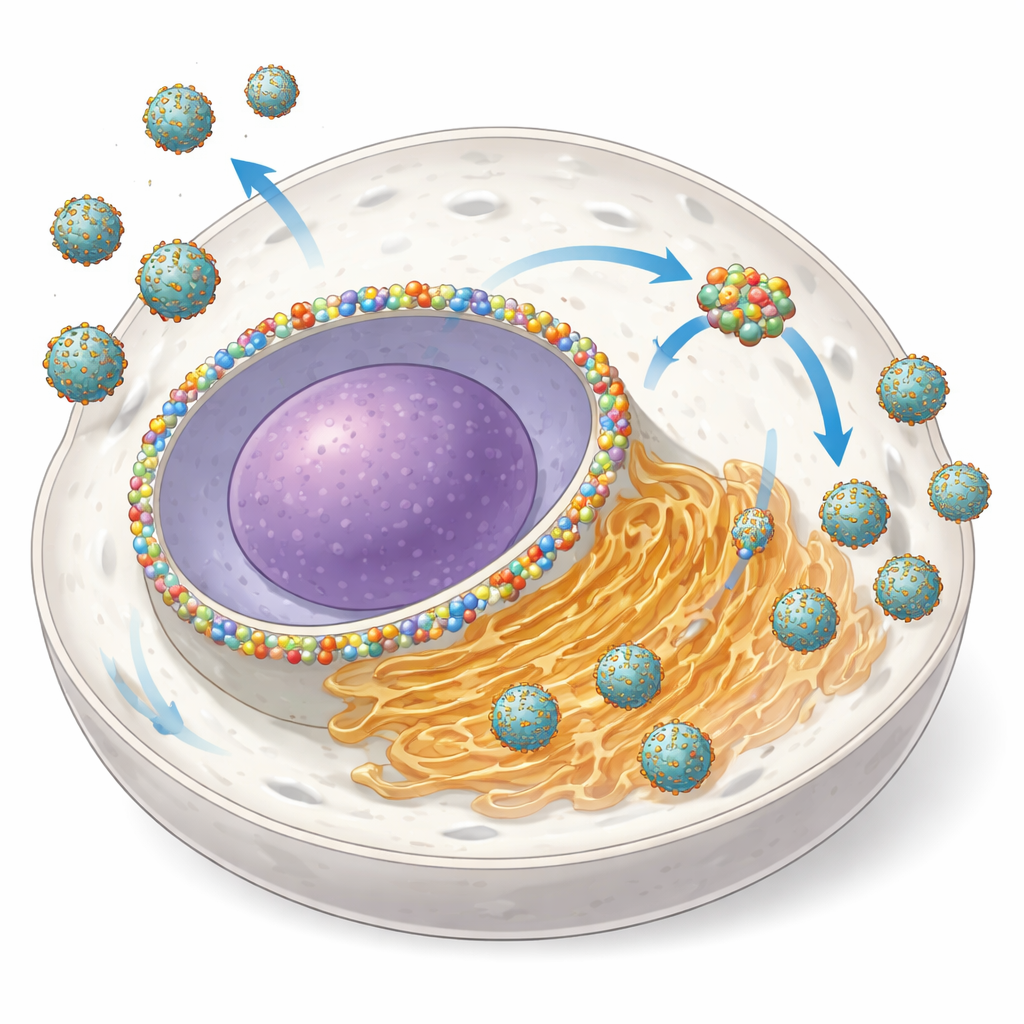
Transformer une porte nucléaire en atelier viral
NUP153 est habituellement un composant du complexe poreux nucléaire, une gigantesque structure qui régule le trafic d’ARN et de protéines entre le noyau et le cytoplasme. Les auteurs ont découvert que lors d’infections par plusieurs orthoflavivirus, les cellules augmentent la quantité de NUP153 et redistribuent une partie de cette protéine depuis l’enveloppe nucléaire vers le site d’amplification viral associé au RE. Grâce à des techniques de microscopie avancées, ils ont montré que NUP153 se regroupe avec les protéines virales NS3 et NS5 et avec l’ARN viral près des membranes du RE, tout en restant en grande partie séparé des petites vésicules où se déroule la réplication de l’ARN. Lorsqu’ils ont dégradé rapidement NUP153 dans des cellules génétiquement modifiées, le nombre de cellules infectées a diminué et la quantité de virus libérée a chuté de 80 à 95 % au maximum, en particulier en début d’infection — des signes clairs que NUP153 agit comme un auxiliaire « proviral ».
Contacts directs avec protéines et ARN viraux
Pour comprendre comment NUP153 aide le virus, les chercheurs ont isolé NUP153 à partir de cellules infectées et identifié ses partenaires par spectrométrie de masse et séquençage de l’ARN. Ils ont trouvé que NUP153 se lie directement à deux enzymes virales clés, NS3 et NS5, sans qu’un ARN agit de pont, et qu’elle s’attache aussi à des régions spécifiques de l’ARN viral lui‑même. Une de ces régions d’ARN se situe à la fin du segment codant la protéine de l’enveloppe externe E et est riche en guanine. Cet élément est fortement conservé chez de nombreux orthoflavivirus, ce qui suggère une fonction importante partagée. Des essais biophysiques ont montré que le domaine de liaison à l’ARN de NUP153 reconnaît cette séquence riche en G, en particulier quand elle n’est pas repliée en une structure compacte en quadruplex G à quatre brins. Le même domaine est également requis pour que NUP153 passe du noyau au site d’amplification viral et pour que la réplication virale soit efficace.
Rééquilibrer la liste des pièces virales
De nouveaux virions ne peuvent se former que si la cellule produit le bon mélange de protéines structurelles et non structurelles à partir de la polyprotéine virale unique. L’équipe a testé si NUP153 influence cet équilibre. Dans des expériences de traduction in vitro utilisant de l’ARN viral simulé, l’ajout du domaine de liaison à l’ARN de NUP153 modifiait les produits protéiques obtenus : il réduisait la production d’un rapporteur situé en aval tout en favorisant des produits plus courts correspondant aux protéines structurelles. Dans des cellules infectées dépourvues de NUP153, les niveaux totaux de protéines virales diminuaient, mais les ratios changeaient : les protéines structurelles comme E étaient relativement sous‑représentées, tandis que plusieurs protéines non structurelles (y compris NS1, NS2B, NS3 et NS5) devenaient plus abondantes par rapport à E. Ce décalage ne résultait pas d’une dégradation protéique plus rapide, ce qui indique plutôt une modification de la traduction de la polyprotéine virale. En conséquence, en début d’infection, les virus dans les cellules déficientes en NUP153 peinaient à assembler et à libérer des particules complètes, retardant la propagation vers les cellules voisines.
Un point faible partagé par plusieurs virus
Les auteurs ont étendu leurs observations au‑delà d’un seul virus. Lors d’infections par les virus Zika, de l’encéphalite japonaise, du Nil occidental, de la fièvre jaune et de la dengue, NUP153 se déplaçait également vers les sites de l’ARN viral et son élimination réduisait de façon constante à la fois la fraction de cellules infectées et le nombre de particules produites. Comme le motif ARN riche en G qui recrute NUP153 est conservé dans cette famille virale, et puisque le rôle de NUP153 est d’ajuster finement le mélange de protéines nécessaire à l’assemblage des particules, l’étude suggère une vulnérabilité commune et exploitable. Cibler l’interaction entre NUP153, l’ARN viral et les protéines virales — sans nécessairement détruire les fonctions essentielles d’entretien de NUP153 — pourrait offrir une nouvelle stratégie dirigée contre l’hôte pour des antiviraux à large spectre.
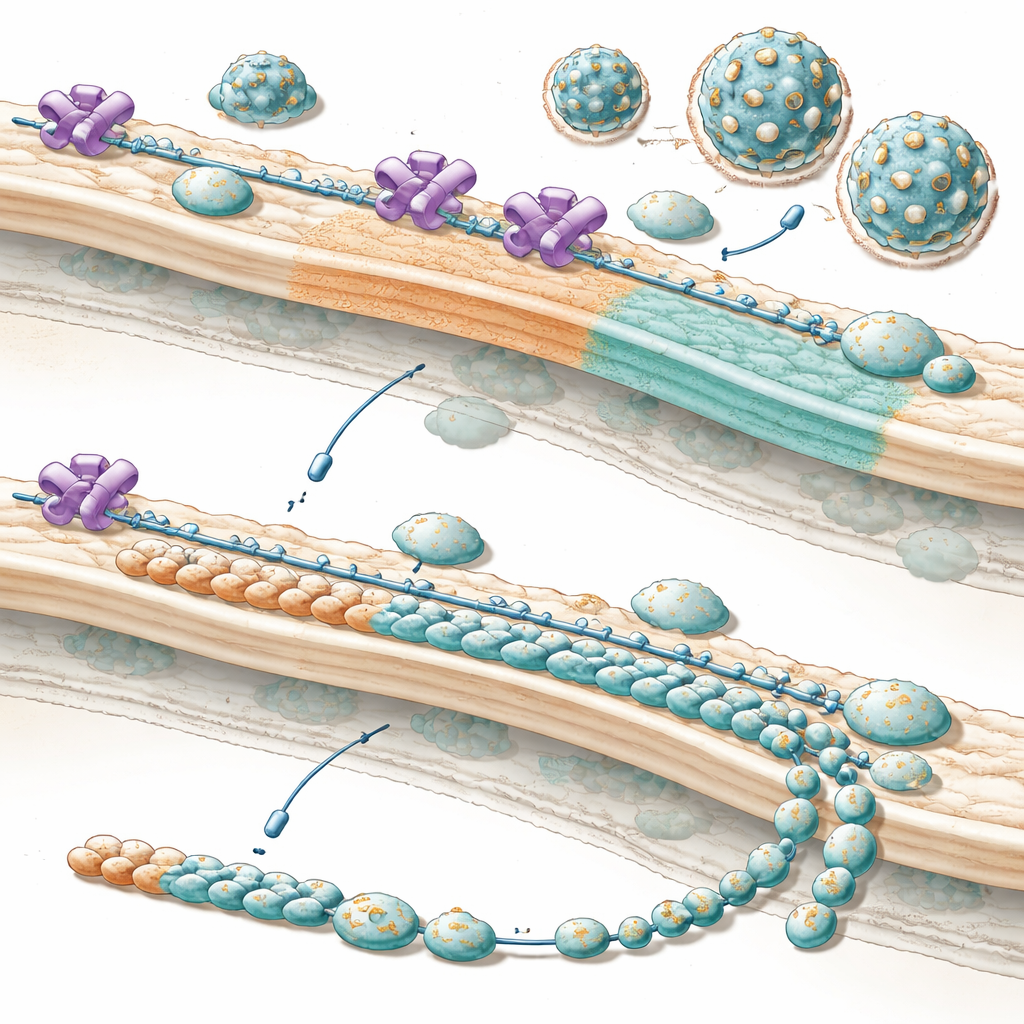
Pourquoi cela compte pour les traitements futurs
En termes simples, ce travail montre que ces virus détournent un gardien cellulaire et le réaffectent en gestionnaire de production, orientant la cellule pour qu’elle fabrique davantage des composants externes nécessaires à la construction de nouveaux virions au moment opportun. Quand NUP153 est retiré ou bloqué, la « liste des pièces » se déséquilibre : beaucoup d’outils internes, mais pas assez d’éléments de coque, si bien que beaucoup moins de particules infectieuses émergent, surtout en début d’infection quand le timing est crucial. Comme cette stratégie semble conservée chez de nombreux flavivirus d’importance médicale, perturber soigneusement ce partenariat détourné entre le virus et NUP153 pourrait un jour aider à prévenir ou limiter des infections graves d’une famille entière d’agents pathogènes actuellement difficiles à traiter.
Citation: Peters, M.B.A., Lindqvist, R., Kassa, E. et al. Proviral NUP153 binding to viral proteins and RNA regulates structural–nonstructural protein ratios in orthoflavivirus infection. Nat Commun 17, 3402 (2026). https://doi.org/10.1038/s41467-026-71449-1
Mots-clés: orthoflavivirus, NUP153, traduction des protéines virales, interaction hôte–virus, antiviraux à large spectre