Clear Sky Science · pt
A ligação proviral de NUP153 a proteínas e RNA virais regula as proporções de proteínas estruturais–não estruturais na infecção por ortoflavivírus
Como os vírus transformam o porteiro da célula em um ajudante
Muitos vírus perigosos transmitidos por mosquitos e carrapatos, incluindo os que causam dengue, Zika, febre do Nilo Ocidental e encefalite transmitida por carrapatos, ainda não têm tratamentos específicos. Este estudo revela como esses vírus sequestram uma proteína humana chamada NUP153—normalmente parte do sistema de vigilância ao redor do núcleo celular—para aumentar sua própria produção. Compreender essa tomada de controle em nível molecular pode abrir caminho para novas estratégias antivirais de amplo espectro que miram o hospedeiro em vez do vírus.
Uma família de vírus sem cura
Os ortoflavivírus são vírus de RNA pequenos, transmitidos por mosquitos e carrapatos, que podem causar infecções cerebrais graves, doenças hemorrágicas e sequelas permanentes. Seu genoma é uma única longa fita de RNA que é lida como uma grande poli-proteína, a qual é então cortada em dez partes: três que formam o capsídeo viral e sete que atuam como ferramentas internas para copiar e montar novas partículas. Para se multiplicarem, esses vírus remodelam o retículo endoplasmático (RE)—uma rede de membranas perto do núcleo—transformando-o num “sítio de amplificação” especializado onde o RNA viral é copiado, proteínas são produzidas e novas partículas virais são montadas. Como não existem antivirais aprovados para esse grupo, pesquisadores estão cada vez mais investigando fatores essenciais do hospedeiro que os vírus dependem como potenciais alvos terapêuticos.
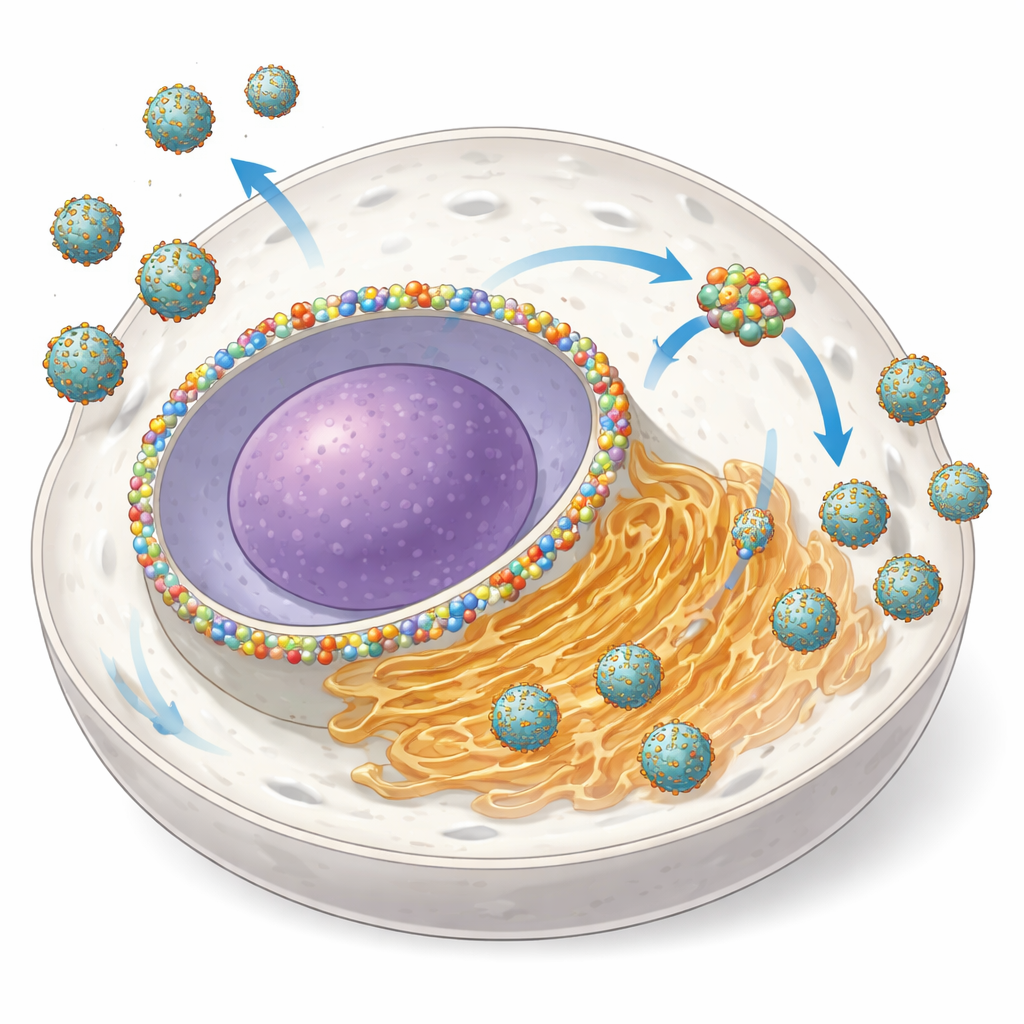
Transformando um portão nuclear numa oficina viral
A NUP153 é normalmente um componente do complexo do poro nuclear, uma estrutura enorme que regula o tráfego de RNA e proteínas entre o núcleo e o citoplasma circundante. Os autores descobriram que, durante a infecção por vários ortoflavivírus, as células aumentam a quantidade de NUP153 e redistribuem parte dela da membrana nuclear para o sítio de amplificação viral no RE. Usando microscopia avançada, mostraram que a NUP153 se agrega junto às proteínas virais NS3 e NS5 e ao RNA viral perto das membranas do RE, permanecendo em grande parte separada das pequenas vesículas onde a própria cópia do RNA ocorre. Quando degradaram rapidamente a NUP153 em células geneticamente modificadas, o número de células infectadas diminuiu e a quantidade de vírus liberada caiu entre 80%–95%, especialmente no início da infecção—sinais claros de que NUP153 atua como um ajudante “proviral”.
Contato direto com proteínas e RNA virais
Para entender como a NUP153 ajuda o vírus, os pesquisadores puxaram a NUP153 de células infectadas e identificaram seus parceiros por espectrometria de massa e sequenciamento de RNA. Eles descobriram que a NUP153 liga-se diretamente a duas enzimas virais-chave, NS3 e NS5, sem precisar do RNA como ponte, e também se conecta a regiões específicas do RNA viral. Uma dessas regiões fica no final do segmento gênico que codifica a proteína de envelope externa E e é rica no nucleotídeo guanina. Esse trecho é fortemente conservado entre muitos ortoflavivírus, sugerindo uma função compartilhada importante. Ensaios biofísicos mostraram que o domínio de ligação ao RNA da NUP153 reconhece essa sequência rica em G, especialmente quando ela não está dobrada numa compacta estrutura de quatro fitas chamada “G-quadruplex”. O mesmo domínio também é necessário para a NUP153 se deslocar do núcleo para o sítio de amplificação viral e para que o vírus replique eficientemente.
Reajustando a lista de peças virais
Novas partículas virais só podem se formar se a célula produzir a mistura correta de proteínas estruturais e não estruturais a partir da única poli-proteína viral. A equipe testou se a NUP153 influencia esse equilíbrio. Em experimentos de tradução in vitro usando RNA semelhante ao viral, adicionar o domínio de ligação ao RNA da NUP153 alterou quais produtos proteicos eram feitos: reduziu a produção de um repórter situado a jusante enquanto favorecia produtos mais curtos correspondentes às proteínas estruturais. Em células infectadas sem NUP153, os níveis totais de proteína viral diminuíram, mas as proporções mudaram: proteínas estruturais como E ficaram relativamente sub-representadas, enquanto várias proteínas não estruturais (incluindo NS1, NS2B, NS3 e NS5) tornaram-se mais abundantes em relação a E. Essa mudança não resultou de degradação proteica mais rápida, apontando em vez disso para uma tradução alterada da poli-proteína viral. Como resultado, no início da infecção, vírus em células deficientes em NUP153 tiveram dificuldade em montar e liberar partículas completas, retardando a disseminação para células vizinhas.
Uma vulnerabilidade comum entre vários vírus
Os autores estenderam suas observações além de um único vírus. Durante infecções por Zika, encefalite japonesa, Nilo Ocidental, febre amarela e dengue, a NUP153 novamente migrou em direção a sítios de RNA viral e sua remoção reduziu de forma consistente tanto a fração de células infectadas quanto o número de partículas progenitoras produzidas. Como o motivo de RNA rico em G que recruta a NUP153 é conservado nessa família viral, e porque o papel da NUP153 é ajustar a mistura de proteínas necessária para a montagem de partículas, o estudo sugere uma vulnerabilidade comum explorável. Mirar a interação entre NUP153, RNA viral e proteínas virais—sem necessariamente destruir as funções essenciais de manutenção da NUP153—poderia oferecer uma nova estratégia dirigida ao hospedeiro para antivirais de amplo espectro.
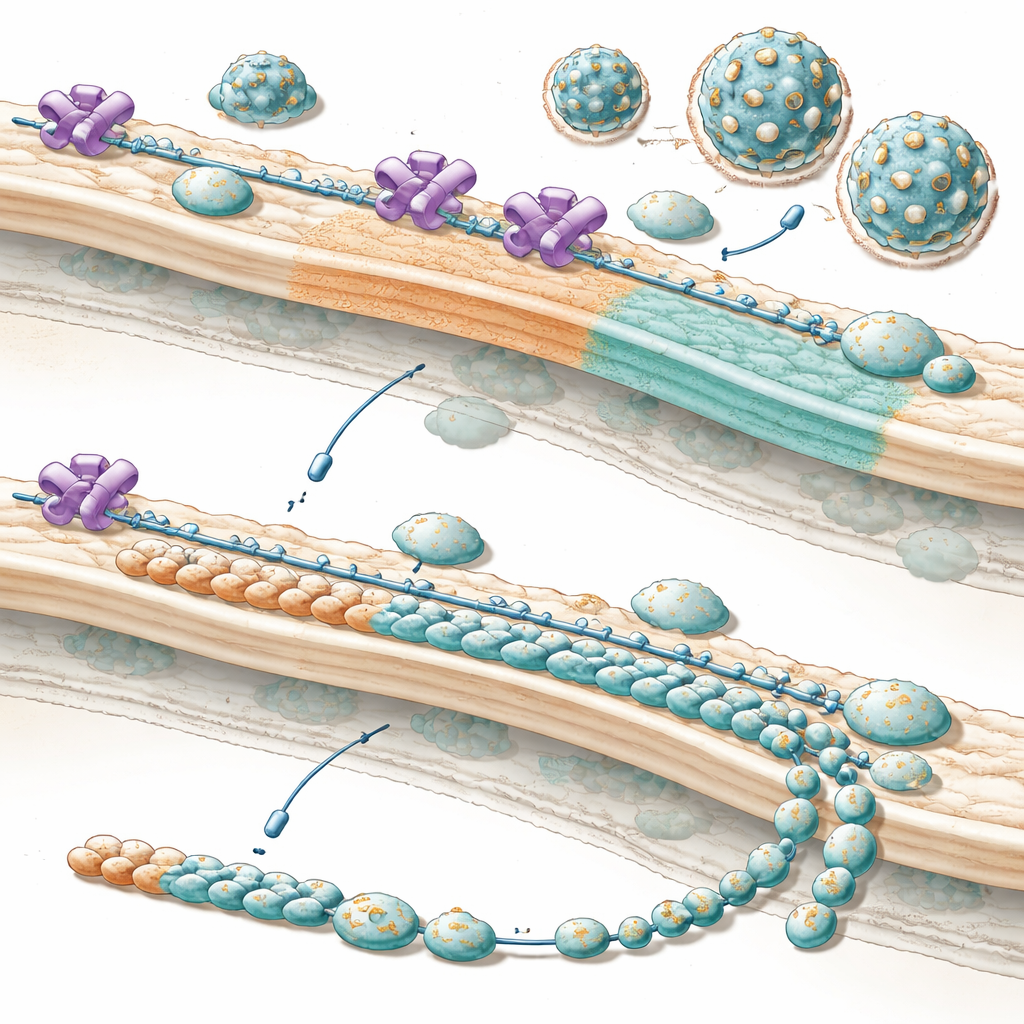
Por que isso importa para tratamentos futuros
Em termos simples, o trabalho mostra que esses vírus cooptam um porteiro celular e o reaproveitam como gerente de produção, orientando a célula a fabricar mais das peças externas necessárias para construir novas partículas virais no momento certo. Quando a NUP153 é removida ou bloqueada, a “lista de peças” fica desequilibrada: muitas ferramentas internas, mas não peças de capa suficientes, de modo que emergem muito menos partículas infecciosas, especialmente no início da infecção, quando o tempo é crítico. Como essa estratégia parece ser conservada entre muitos flavivírus de importância médica, desestabilizar cuidadosamente essa parceria sequestrada entre o vírus e a NUP153 pode um dia ajudar a prevenir ou limitar infecções graves de toda uma família de patógenos atualmente difíceis de tratar.
Citação: Peters, M.B.A., Lindqvist, R., Kassa, E. et al. Proviral NUP153 binding to viral proteins and RNA regulates structural–nonstructural protein ratios in orthoflavivirus infection. Nat Commun 17, 3402 (2026). https://doi.org/10.1038/s41467-026-71449-1
Palavras-chave: orthoflavivirus, NUP153, tradução de proteína viral, interação hospedeiro–vírus, antivirais de amplo espectro