Clear Sky Science · nl
Provirale NUP153-binding aan virale eiwitten en RNA reguleert verhoudingen structureel–niet-structureel eiwit bij orthoflavivirusinfectie
Hoe virussen de poortwachter van een cel tot helper maken
Veel gevaarlijke door muggen en teken overgedragen virussen, waaronder die verantwoordelijk voor dengue, Zika, West-Nijlkoorts en tekenencefalitis, hebben nog geen gerichte behandelingen. Deze studie toont hoe deze virussen een menselijk eiwit, NUP153 — normaal onderdeel van het poortbewakingssysteem rond de celkern — kapen om hun eigen productie te bevorderen. Inzicht in deze kaping op moleculair niveau kan de deur openen naar brede nieuwe antivirale strategieën die de gastheer in plaats van het virus zelf als doelwit nemen.
Een familie van virussen zonder remedie
Orthoflavivirussen zijn kleine RNA-virussen die door muggen en teken worden overgedragen en ernstige herseninfecties, bloedingsziekten en levenslange complicaties kunnen veroorzaken. Hun genoom bestaat uit één lange streng RNA die wordt afgelezen tot één groot polyproteïne, dat vervolgens in tien stukken wordt geknipt: drie die de virusmantel vormen en zeven die functioneren als interne hulpmiddelen voor kopiëren en assembleren van nieuwe deeltjes. Om zich te vermenigvuldigen, herstructureren deze virussen het endoplasmatisch reticulum (ER) van de cel — een membraannetwerk nabij de kern — tot een gespecialiseerd "versterkingsstation" waar viraal RNA wordt gekopieerd, eiwitten worden gemaakt en nieuwe virusdeeltjes worden geassembleerd. Omdat er geen goedgekeurde antivirale middelen voor deze groep bestaan, richten onderzoekers zich steeds meer op essentiële gastheerfactoren waarop virussen vertrouwen als potentiële medicijntargets.
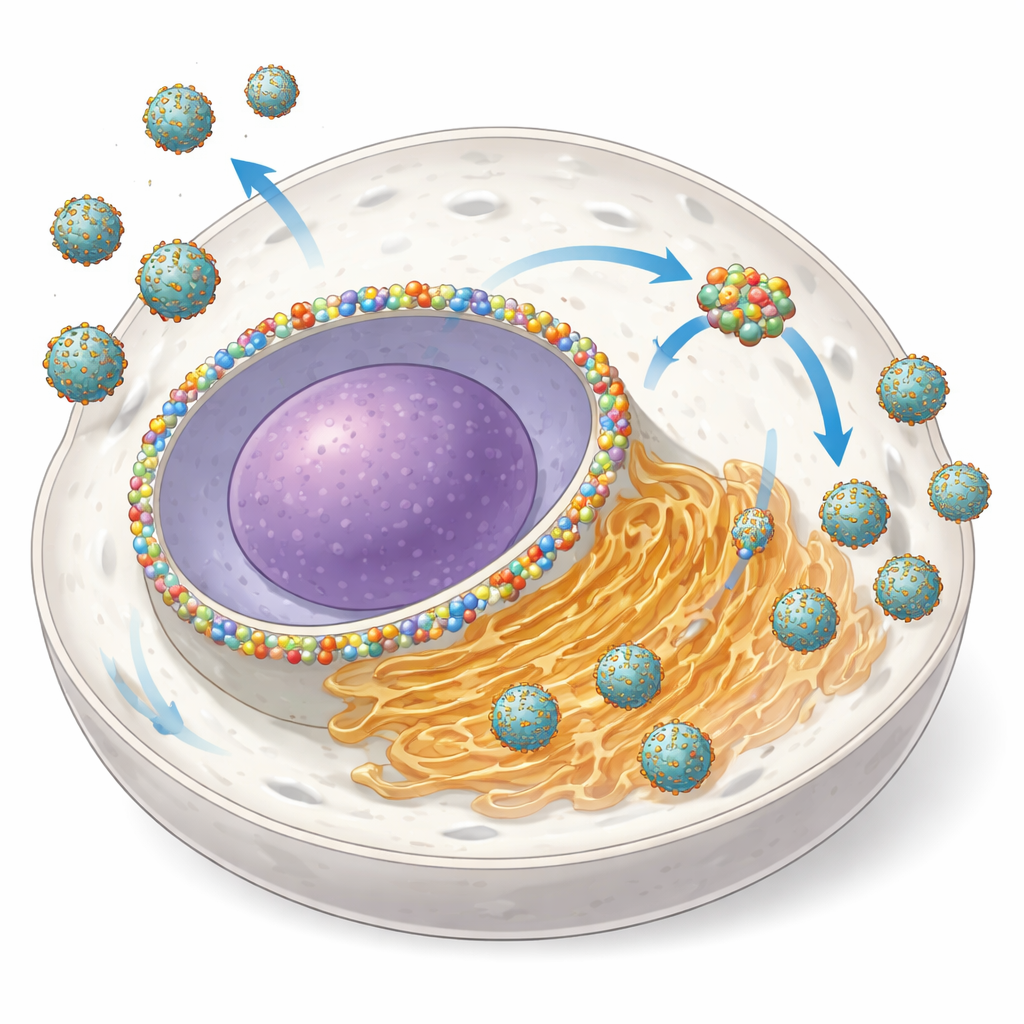
Van nucleaire poort naar viruswerkplaats
NUP153 is doorgaans een onderdeel van het nucleaire poriecomplex, een enorm bouwwerk dat het verkeer van RNA en eiwitten tussen de kern en het omliggende cytoplasma reguleert. De auteurs ontdekten dat tijdens infectie met meerdere orthoflavivirussen cellen de hoeveelheid NUP153 verhogen en een deel ervan verplaatsen van het nucleaire omhulsel naar het ER-gebaseerde virale versterkingsstation. Met geavanceerde microscopie toonden ze aan dat NUP153 bijeenklontert met de virale eiwitten NS3 en NS5 en met viraal RNA nabij ER-membranen, terwijl het grotendeels gescheiden blijft van de kleine blaasjes waar het RNA zelf wordt gekopieerd. Wanneer ze NUP153 snel afbraken in getransformeerde cellen, daalde het aantal geïnfecteerde cellen en viel de hoeveelheid vrijkomend virus met 80–95% terug, vooral vroeg in de infectie — duidelijke aanwijzingen dat NUP153 als een "provirale" helper fungeert.
Direct contact met virale eiwitten en RNA
Om te begrijpen hoe NUP153 het virus helpt, haalden de onderzoekers NUP153 uit geïnfecteerde cellen en identificeerden ze zijn partners via massaspectrometrie en RNA-sequencing. Ze vonden dat NUP153 direct bindt aan twee cruciale virale enzymen, NS3 en NS5, zonder dat RNA als brug nodig is, en dat het ook aan specifieke regio’s van het virale RNA hecht. Een van deze RNA-regio’s bevindt zich aan het einde van het gensegment dat het buitenste mantelprotein E codeert en is rijk aan het nucleotide guanine. Deze sequentie is sterk geconserveerd bij veel orthoflavivirussen, wat wijst op een belangrijke gedeelde functie. Biofysische assays lieten zien dat het RNA-bindende domein van NUP153 deze G-rijke sequentie herkent, vooral wanneer deze niet is gevouwen in een compacte vierstrengige "G-quadruplex"-structuur. Datzelfde domein is ook nodig zodat NUP153 van de kern naar het virale versterkingsstation kan verhuizen en zodat het virus efficiënt kan repliceren.
Het herbalanceren van de virale onderdelenlijst
Nieuwe virusdeeltjes kunnen alleen gevormd worden als de cel de juiste mix van structurele en niet-structurele eiwitten produceert uit het enkele virale polyproteïne. Het team testte of NUP153 deze balans beïnvloedt. In vertaalexperimenten in vitro met viraal-achtig RNA veranderde het toevoegen van het RNA-bindende domein van NUP153 welke eiwitproducten werden gemaakt: de productie van een downstream reporter nam af, terwijl kortere producten, overeenkomend met de structurele eiwitten, werden bevoordeeld. In geïnfecteerde cellen zonder NUP153 daalden de totale niveaus van virale eiwitten, maar verschoven de verhoudingen: structurele eiwitten zoals E waren relatief ondervertegenwoordigd, terwijl meerdere niet-structurele eiwitten (inclusief NS1, NS2B, NS3 en NS5) relatief meer abundant werden vergeleken met E. Deze verschuiving was niet toe te schrijven aan snellere eiwitafbraak, wat wijst op een veranderde translatie van het virale polyproteïne. Daardoor hadden virussen in NUP153-deficiënte cellen vroeg in de infectie moeite met assembleren en loslaten van volledige deeltjes, wat de verspreiding naar naburige cellen vertraagde.
Een gedeelde zwakke plek bij meerdere virussen
De auteurs breidden hun waarnemingen uit tot meer dan één virus. Tijdens infectie met Zika-, Japans encefalitis-, West-Nijl-, geelkoorts- en denguevirussen bewoog NUP153 opnieuw naar plaatsen met viraal RNA en verminderde verwijdering ervan consequent zowel het aandeel geïnfecteerde cellen als het aantal geproduceerde nakomelingsdeeltjes. Omdat het G-rijke RNA-motief dat NUP153 aantrekt geconserveerd is binnen deze virusfamilie, en omdat NUP153’s rol is de eiwitmix die nodig is voor de deeltje-assemblage fijn af te stemmen, suggereert de studie een gemeenschappelijke, benutbare kwetsbaarheid. Het richten op de interactie tussen NUP153, viraal RNA en virale eiwitten — zonder per se de essentiële huishoudelijke rollen van NUP153 te vernietigen — zou een nieuwe, gastheergerichte strategie voor breed-spectrum antivirale middelen kunnen opleveren.
Waarom dit ertoe doet voor toekomstige behandelingen
In eenvoudige bewoordingen laat dit werk zien dat deze virussen een cellulaire poortwachter kapen en herbestemmen als productiechef, die de cel stuurt om op het juiste moment meer van de buitenste onderdelen te maken die nodig zijn om nieuwe virusdeeltjes te bouwen. Wanneer NUP153 wordt verwijderd of geblokkeerd, raakt de "onderdelenlijst" uit balans: er zijn veel interne hulpmiddelen, maar niet genoeg mantelstukken, waardoor veel minder infectieuze deeltjes ontstaan, vooral vroeg in de infectie wanneer timing cruciaal is. Omdat deze strategie bij veel medisch belangrijke flavivirussen lijkt te zijn behouden, kan het zorgvuldig verstoren van deze gekaapte samenwerking tussen virus en NUP153 mogelijk in de toekomst helpen ernstige infecties door een hele familie van momenteel moeilijk te behandelen ziekteverwekkers te voorkomen of te beperken.
Bronvermelding: Peters, M.B.A., Lindqvist, R., Kassa, E. et al. Proviral NUP153 binding to viral proteins and RNA regulates structural–nonstructural protein ratios in orthoflavivirus infection. Nat Commun 17, 3402 (2026). https://doi.org/10.1038/s41467-026-71449-1
Trefwoorden: orthoflavivirus, NUP153, vertaling van virale eiwitten, gastheer–virusinteractie, breed-spectrum antivirale middelen