Clear Sky Science · es
La unión pro-viral de NUP153 a proteínas y ARN virales regula las proporciones de proteínas estructurales y no estructurales en la infección por ortoflavivirus
Cómo los virus convierten al guardián de la célula en un ayudante
Muchos virus peligrosos transmitidos por mosquitos y garrapatas, incluidos los que causan dengue, Zika, fiebre del Nilo Occidental y encefalitis transmitida por garrapatas, todavía no tienen tratamientos específicos. Este estudio revela cómo estos virus secuestran una proteína humana llamada NUP153—normalmente parte del sistema de control alrededor del núcleo celular—para aumentar su propia producción. Entender esta apropiación a nivel molecular podría abrir la puerta a nuevas estrategias antivirales de amplio espectro que apunten al huésped en lugar del virus.
Una familia de virus sin cura
Los ortoflavivirus son virus de ARN pequeños transmitidos por mosquitos y garrapatas que pueden causar infecciones cerebrales graves, enfermedades hemorrágicas y complicaciones crónicas. Su genoma es una sola hebra larga de ARN que se traduce en una única poliproteína gigante, la cual se escinde después en diez piezas: tres que forman la cápside del virus y siete que actúan como herramientas internas para copiar y ensamblar nuevas partículas. Para multiplicarse, estos virus remodelan el retículo endoplásmico (RE)—una red de membranas cerca del núcleo—en un “sitio de amplificación” especializado donde se copia el ARN viral, se sintetizan proteínas y se ensamblan nuevas partículas virales. Dado que no existen fármacos antivirales aprobados para este grupo, los investigadores buscan cada vez más factores esenciales del huésped de los que dependen los virus como posibles dianas terapéuticas.
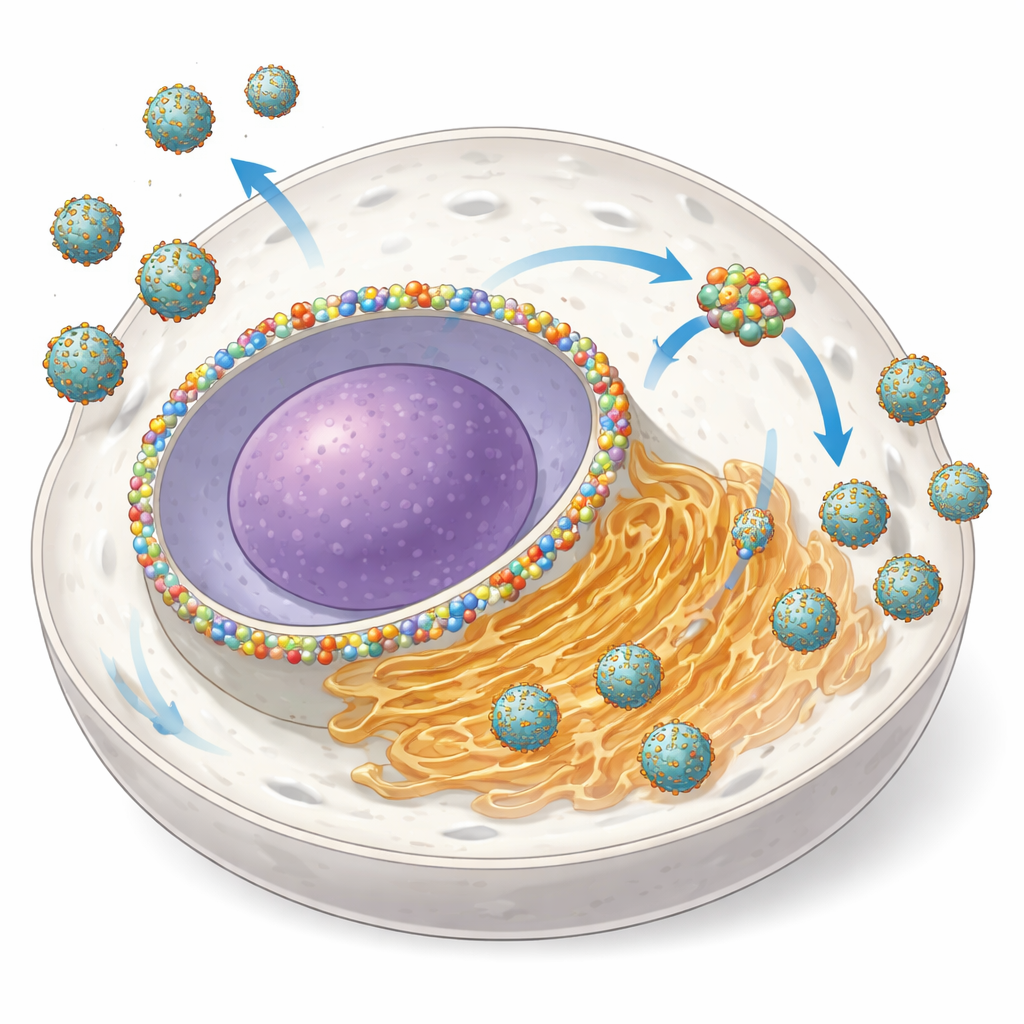
Convertir una puerta nuclear en un taller viral
NUP153 suele ser un componente del complejo del poro nuclear, una estructura enorme que regula el tráfico de ARN y proteínas entre el núcleo y el citoplasma circundante. Los autores descubrieron que durante la infección con varios ortoflavivirus, las células aumentan la cantidad de NUP153 y redistribuyen parte de ella desde la envoltura nuclear hacia el sitio de amplificación viral basado en el RE. Mediante microscopía avanzada, mostraron que NUP153 se agrupa junto con las proteínas virales NS3 y NS5 y con ARN viral cerca de las membranas del RE, mientras permanece en gran medida separado de las pequeñas vesículas donde ocurre la replicación del ARN. Cuando degradaron rápidamente NUP153 en células modificadas, el número de células infectadas disminuyó y la cantidad de virus liberado se redujo hasta un 80–95%, especialmente en etapas tempranas de la infección—signos claros de que NUP153 actúa como un ayudante “proviral”.
Contacto directo con proteínas y ARN virales
Para entender cómo NUP153 ayuda al virus, los investigadores aislaron NUP153 de células infectadas e identificaron sus asociados mediante espectrometría de masas y secuenciación de ARN. Encontraron que NUP153 se une directamente a dos enzimas virales clave, NS3 y NS5, sin necesitar al ARN como puente, y también se fija a regiones específicas del ARN viral. Una de estas regiones se sitúa al final del segmento génico que codifica la proteína de la envoltura externa E y es rica en la nucleótido guanina. Este tramo está fuertemente conservado entre muchos ortoflavivirus, lo que sugiere una función compartida importante. Ensayos biofísicos mostraron que el dominio de unión a ARN de NUP153 reconoce esta secuencia rica en G, especialmente cuando no está plegada en una estructura compacta de cuatro cadenas llamada “G-quadruplex”. El mismo dominio también es necesario para que NUP153 se traslade desde el núcleo al sitio de amplificación viral y para que el virus replique de manera eficiente.
Reequilibrando la lista de piezas virales
Las nuevas partículas virales solo pueden formarse si la célula produce la mezcla adecuada de proteínas estructurales y no estructurales a partir de la única poliproteína viral. El equipo probó si NUP153 influye en ese equilibrio. En experimentos de traducción in vitro usando ARN similar al viral, añadir el dominio de unión a ARN de NUP153 cambió qué productos proteicos se sintetizaban: redujo la producción de un reportero situado aguas abajo mientras favorecía productos más cortos correspondientes a las proteínas estructurales. En células infectadas sin NUP153, los niveles totales de proteínas virales disminuyeron, pero las proporciones cambiaron: proteínas estructurales como E quedaron relativamente subrepresentadas, mientras que varias proteínas no estructurales (incluyendo NS1, NS2B, NS3 y NS5) fueron más abundantes en comparación con E. Este desplazamiento no se debió a una degradación proteica más rápida, sino a una alteración en la traducción de la poliproteína viral. Como resultado, al principio de la infección, los virus en células deficientes en NUP153 tuvieron dificultades para ensamblar y liberar partículas completas, retrasando la propagación a células vecinas.
Un punto débil compartido entre múltiples virus
Los autores extendieron sus observaciones más allá de un solo virus. Durante la infección por Zika, encefalitis japonesa, Nilo Occidental, fiebre amarilla y dengue, NUP153 nuevamente se desplazó hacia los sitios de ARN viral y su eliminación redujo de forma consistente tanto la fracción de células infectadas como el número de partículas progenies producidas. Dado que el motivo rico en G del ARN que recluta NUP153 está conservado en esta familia de virus, y porque la función de NUP153 es ajustar la mezcla proteica necesaria para el ensamblaje de partículas, el estudio sugiere una vulnerabilidad común y explotable. Apuntar a la interacción entre NUP153, el ARN viral y las proteínas virales—sin necesariamente destruir las funciones esenciales de mantenimiento de NUP153—podría proporcionar una nueva estrategia dirigida al huésped para antivirales de amplio espectro.
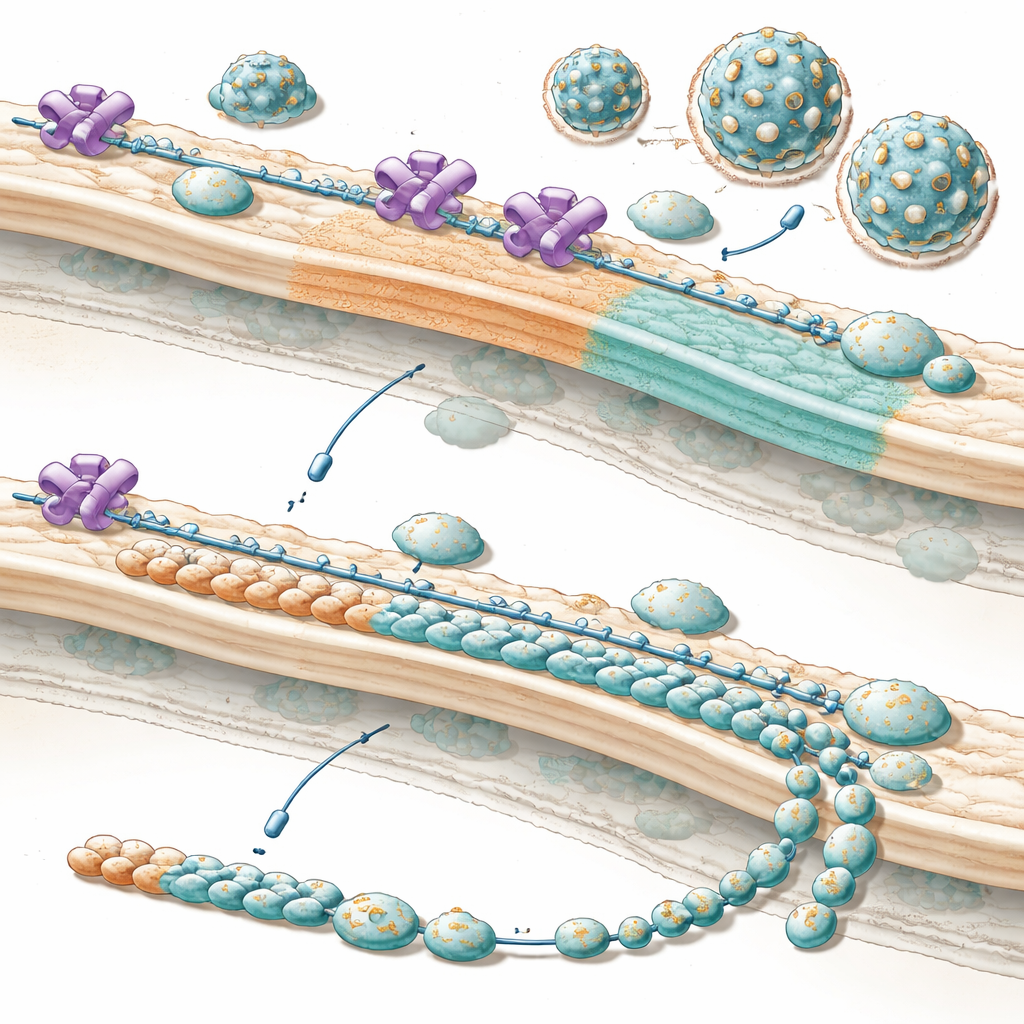
Por qué esto importa para tratamientos futuros
En términos cotidianos, el trabajo muestra que estos virus cooptan a un guardián celular y lo reconvierten en un gestor de producción, orientando a la célula para fabricar más las piezas externas necesarias para construir nuevas partículas virales en el momento oportuno. Cuando NUP153 se elimina o bloquea, la “lista de piezas” se desequilibra: abundan las herramientas internas, pero no hay suficientes piezas de la envoltura, por lo que emergen muchas menos partículas infecciosas, especialmente al inicio de la infección cuando el tiempo es crucial. Dado que esta estrategia parece estar conservada entre muchos flavivirus médicamente relevantes, interrumpir con precisión esta asociación usurpada entre el virus y NUP153 podría algún día ayudar a prevenir o limitar infecciones graves de toda una familia de patógenos actualmente difíciles de tratar.
Cita: Peters, M.B.A., Lindqvist, R., Kassa, E. et al. Proviral NUP153 binding to viral proteins and RNA regulates structural–nonstructural protein ratios in orthoflavivirus infection. Nat Commun 17, 3402 (2026). https://doi.org/10.1038/s41467-026-71449-1
Palabras clave: ortoflavivirus, NUP153, traducción de proteínas virales, interacción huésped–virus, antivirales de amplio espectro