Clear Sky Science · ja
プロウイルス性のNUP153がウイルス蛋白およびRNAに結合してオルトフラビウイルス感染における構造蛋白−非構造蛋白比を制御する
ウイルスはどうやって細胞の門番を手先に変えるのか
デング熱、ジカ熱、ウエストナイル熱、および重症化することのあるマダニ媒介性脳炎など、多くの危険な蚊・ダニ媒介ウイルスには依然として特異的な治療法がありません。本研究は、これらのウイルスが本来は核周囲の門番システムの一部であるヒトタンパク質NUP153をどのように乗っ取り、自らの増殖を助けるのかを明らかにします。こうした分子レベルでの把握は、ウイルスではなく宿主側を標的にする広域の新しい抗ウイルス戦略を切り開く可能性があります。
治療法のないウイルス科
オルトフラビウイルスは蚊やダニが媒介する小型のRNAウイルスで、重篤な脳感染、出血性疾患、そして生涯にわたる合併症を引き起こすことがあります。彼らのゲノムは一本の長いRNA鎖で、これが一つの巨大なポリタンパク質として翻訳され、その後10個の断片に切断されます:外殻を構成する3つと、複製や粒子組立の内部機能を担う7つです。増殖のために、これらのウイルスは核近傍の膜ネットワークである小胞体(ER)を改造して、ウイルスRNAの複製、タンパク質合成、新しいウイルス粒子の組立が行われる特殊な「増幅サイト」を作り出します。このウイルス群に対する承認済みの抗ウイルス薬が存在しないため、研究者たちはウイルスが依存する必須の宿主因子を新たな薬剤標的として注目しています。
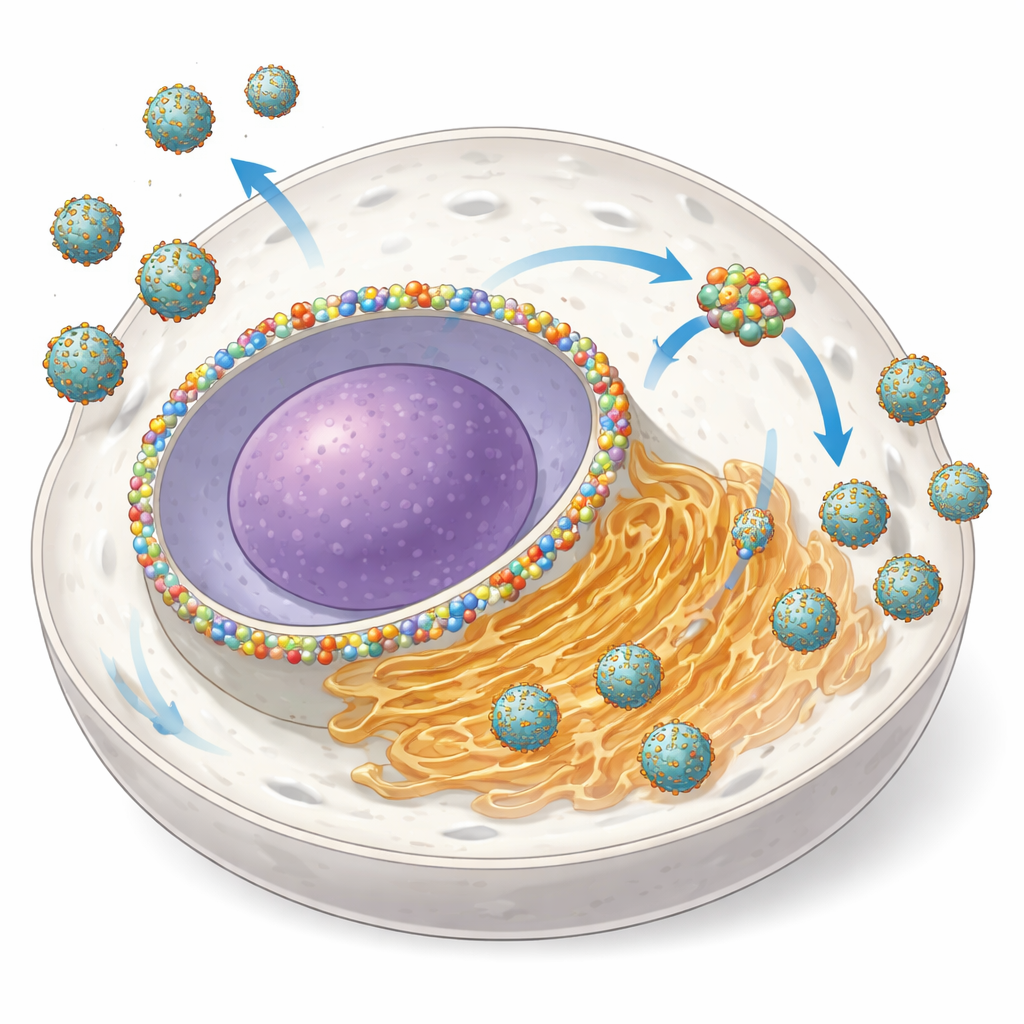
核の門をウイルスの作業場に変える
NUP153は通常、核膜孔複合体の構成要素であり、核と細胞質の間でRNAやタンパク質の輸送を調節する巨大な構造体です。著者らは、複数のオルトフラビウイルス感染時に細胞がNUP153の量を増やし、その一部を核膜からERに基づくウイルス増幅サイトへ再配置することを発見しました。高解像度顕微鏡解析により、NUP153がER膜近傍でウイルス蛋白質のNS3およびNS5、さらにウイルスRNAとともに凝集する一方、RNAの複製そのものが行われる小胞とは大部分が分離していることが示されました。設計された細胞でNUP153を速やかに分解すると、感染細胞の割合が減少し、放出されるウイルス量は特に感染初期において最大80〜95%減少しました。これはNUP153が“プロウイルス”な補助因子として働く明確な証拠です。
ウイルス蛋白およびRNAとの直接接触
NUP153がウイルスをどのように助けるかを理解するため、研究者たちは感染細胞からNUP153を引き出し、質量分析とRNAシーケンシングでその結合相手を同定しました。彼らはNUP153がRNAを介さずに主要なウイルス酵素であるNS3およびNS5に直接結合し、さらにウイルスRNAの特定領域にも結びつくことを見出しました。そのRNA領域の一つは外殻蛋白Eをコードする遺伝子セグメントの末端に位置し、グアニンに富む配列でした。この配列は多くのオルトフラビウイルスで強く保存されており、重要な共通機能を示唆します。生物物理学的アッセイでは、NUP153のRNA結合ドメインがこのGリッチ配列を認識すること、特にそれが四本鎖の「G-四重鎖」構造に折りたたまれていない状態で顕著であることが示されました。同じドメインは、NUP153が核からウイルス増幅サイトへ移動するため、そしてウイルスが効率的に複製するためにも必要でした。
ウイルス部品の比率を再調整する
新しいウイルス粒子が形成されるには、単一のウイルス性ポリタンパク質から適切な割合の構造蛋白と非構造蛋白が産生される必要があります。研究チームはNUP153がこのバランスに影響を与えるかどうかを試験しました。ウイルス様RNAを用いた試験管内翻訳実験で、NUP153のRNA結合ドメインを加えると産生されるタンパク産物のパターンが変わりました:下流のレポーターの産生は減少し、構造蛋白に対応するより短い産物が優勢になりました。NUP153を欠く感染細胞では総ウイルス蛋白量は低下しましたが、比率が変化しました:Eなどの構造蛋白は相対的に不足し、一方でNS1、NS2B、NS3、NS5を含むいくつかの非構造蛋白はEに比べて相対的に増加しました。この変化はタンパク質分解が速くなったためではなく、ポリタンパク質の翻訳が変化したことに起因しています。その結果、感染初期にはNUP153欠損細胞のウイルスは完全な粒子を組み立てて放出するのに苦労し、隣接細胞への拡散が遅れました。
複数ウイルスに共通する弱点
著者らは観察を単一ウイルスに留めず拡張しました。ジカウイルス、日本脳炎ウイルス、ウエストナイルウイルス、黄熱ウイルス、デングウイルスの感染でも、NUP153は再びウイルスRNAの存在する部位へ移動し、その除去は感染細胞の割合と産生される子孫粒子数の両方を一貫して減少させました。NUP153を呼び寄せるGリッチなRNAモチーフがこのウイルス科で保存されていること、そして粒子組立に必要なタンパク質の比率を微調整するNUP153の役割から、この研究は共通して利用可能な脆弱性を示唆します。NUP153、ウイルスRNA、およびウイルス蛋白間の相互作用を標的にすることは、NUP153の必須なハウスキーピング機能を必ずしも破壊することなく、広域抗ウイルス薬の宿主指向戦略を提供する可能性があります。
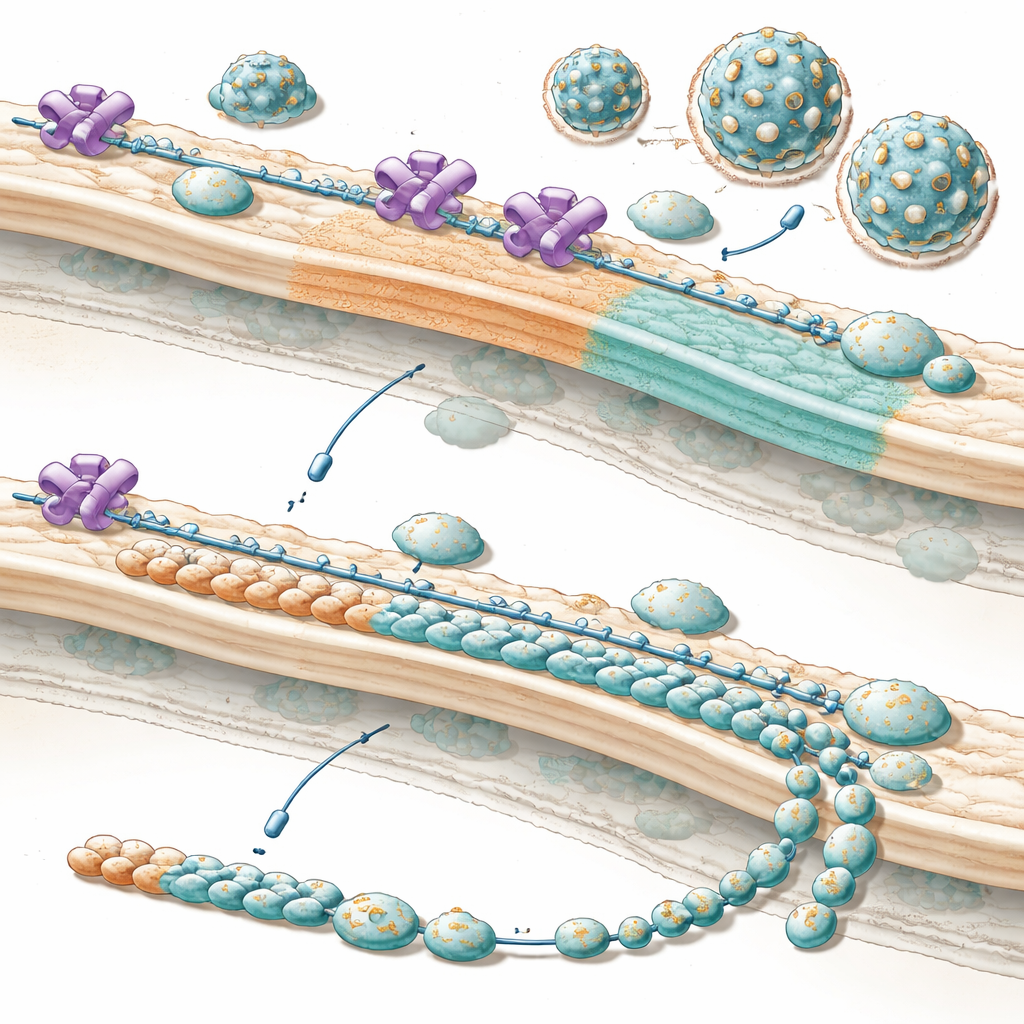
将来の治療に関してなぜ重要か
日常的な言い方をすれば、本研究はこれらのウイルスが細胞の門番を乗っ取り、生産管理者として再利用し、新しいウイルス粒子を作るために必要な外殻部品を適切なタイミングでより多く作らせることを示しています。NUP153が除去または阻害されると「部品表」は不均衡になり、内部のツールは多くても外殻部品が不足するため、感染初期のタイミングが重要な段階で感染性粒子は大幅に減少します。この戦略が多くの医学的に重要なフラビウイルスで保存されている可能性があるため、ウイルスとNUP153の乗っ取り関係を慎重に遮断することは、現在治療が難しいウイルス科全体による重篤な感染症の予防や抑制に寄与するかもしれません。
引用: Peters, M.B.A., Lindqvist, R., Kassa, E. et al. Proviral NUP153 binding to viral proteins and RNA regulates structural–nonstructural protein ratios in orthoflavivirus infection. Nat Commun 17, 3402 (2026). https://doi.org/10.1038/s41467-026-71449-1
キーワード: オルトフラビウイルス, NUP153, ウイルス蛋白翻訳, 宿主–ウイルス相互作用, 広域抗ウイルス薬