Clear Sky Science · it
Il legame provirale di NUP153 con proteine e RNA virali regola i rapporti tra proteine strutturali e non strutturali nelle infezioni da ortoflavivirus
Come i virus trasformano il guardiano della cellula in un collaboratore
Molti virus pericolosi trasmessi da zanzare e zecche, tra cui quelli responsabili della dengue, dello Zika, della febbre del Nilo occidentale e dell’encefalite trasmessa da zecche, sono ancora privi di terapie specifiche. Questo studio mostra come questi virus dirottino una proteina umana chiamata NUP153—normalmente parte del sistema di controllo attorno al nucleo—per aumentare la propria produzione. Comprendere questo controllo a livello molecolare potrebbe aprire la strada a nuove strategie antivirali ad ampio spettro che colpiscono l’ospite anziché il virus.
Una famiglia di virus senza cura
Gli ortoflavivirus sono piccoli virus a RNA trasmessi da zanzare e zecche che possono causare gravi infezioni cerebrali, malattie emorragiche e complicazioni croniche. Il loro genoma è un singolo filamento lungo di RNA che viene tradotto in una grande poliproteina, poi scissa in dieci frammenti: tre che formano l’involucro virale e sette che fungono da strumenti interni per copiare e assemblare nuove particelle. Per moltiplicarsi, questi virus rimodellano il reticolo endoplasmatico (ER)—una rete membranosa vicino al nucleo—creando un «sito di amplificazione» specializzato dove l’RNA virale viene copiato, le proteine sintetizzate e le nuove particelle assemblate. Poiché non esistono farmaci antivirali approvati per questo gruppo, i ricercatori guardano sempre più ai fattori ospite essenziali di cui i virus dipendono come possibili bersagli farmacologici.
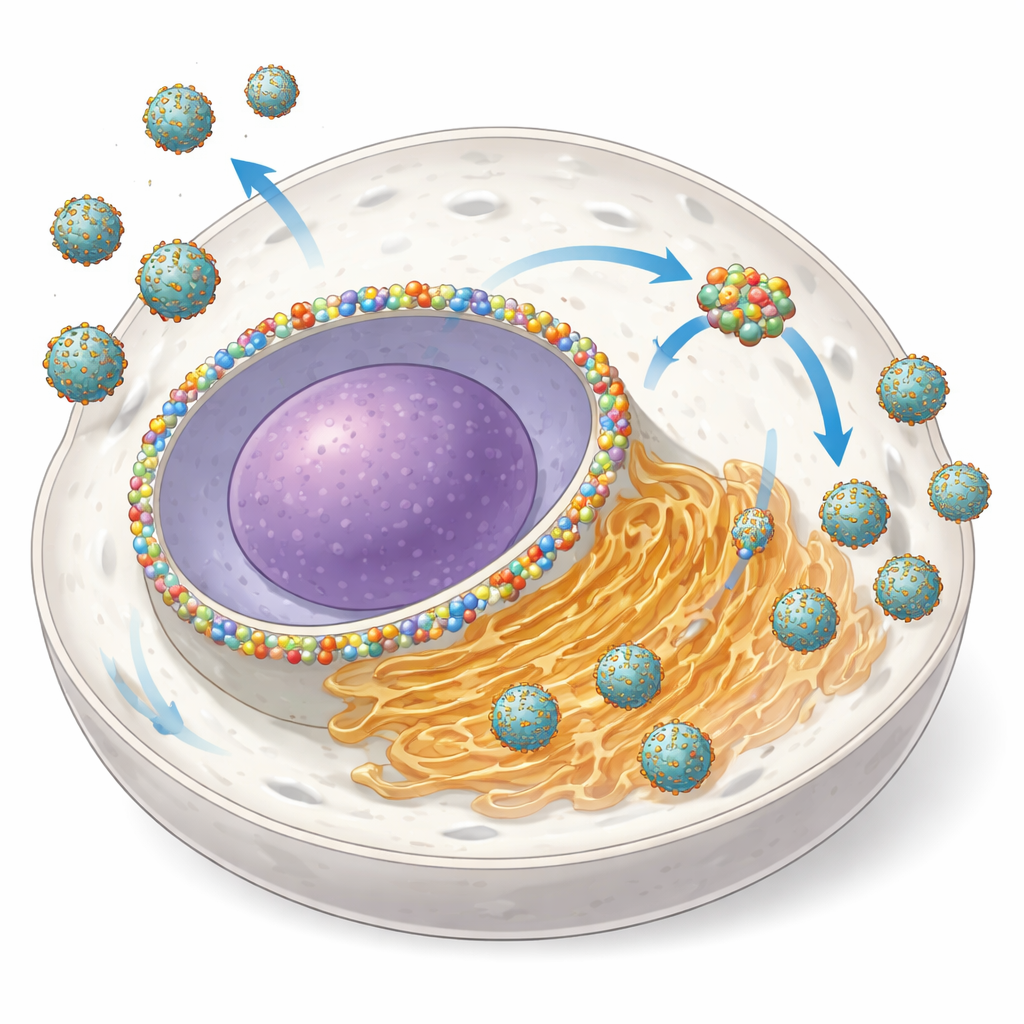
Trasformare una porta nucleare in una officina virale
NUP153 è normalmente una componente del complesso del poro nucleare, una struttura enorme che regola il traffico di RNA e proteine tra il nucleo e il citoplasma circostante. Gli autori hanno scoperto che durante l’infezione con diversi ortoflavivirus, le cellule aumentano la quantità di NUP153 e redistribuiscono parte di essa dall’involucro nucleare al sito di amplificazione virale basato sull’ER. Con microscopia avanzata hanno mostrato che NUP153 si raggruppa insieme alle proteine virali NS3 e NS5 e all’RNA virale vicino alle membrane dell’ER, pur rimanendo per lo più separata dalle piccole vescicole dove avviene la copia dell’RNA. Quando hanno degradato rapidamente NUP153 in cellule ingegnerizzate, il numero di cellule infette è diminuito e la quantità di virus rilasciata è calata fino all’80–95%, soprattutto nelle fasi iniziali dell’infezione—chiari segnali che NUP153 agisce come un fattore «provirale» di supporto.
Contatto diretto con proteine e RNA virali
Per capire come NUP153 aiuta il virus, i ricercatori hanno isolato NUP153 da cellule infette e identificato i suoi partner con spettrometria di massa e sequenziamento dell’RNA. Hanno scoperto che NUP153 lega direttamente due enzimi virali chiave, NS3 e NS5, senza bisogno che l’RNA faccia da ponte, e si lega anche a regioni specifiche dell’RNA virale stesso. Una di queste regioni si trova alla fine del segmento genico che codifica la proteina di involucro esterno E ed è ricca di guanina. Questo tratto è fortemente conservato in molti ortoflavivirus, suggerendo una funzione condivisa importante. Saggi biofisici hanno mostrato che il dominio di NUP153 che lega l’RNA riconosce questa sequenza ricca di G, soprattutto quando non è ripiegata in una compatta struttura a quattro filamenti detta G-quadruplex. Lo stesso dominio è necessario anche per il trasporto di NUP153 dal nucleo al sito di amplificazione virale e per la replicazione efficiente del virus.
Riequilibrare la lista delle parti virali
Le nuove particelle virali possono formarsi solo se la cellula produce la giusta miscela di proteine strutturali e non strutturali a partire dalla singola poliproteina virale. Il gruppo ha verificato se NUP153 influenzi questo equilibrio. In esperimenti di traduzione in vitro con RNA simil-virale, l’aggiunta del dominio legante l’RNA di NUP153 ha cambiato i prodotti proteici: ha ridotto la produzione di un reporter a valle favorendo prodotti più corti corrispondenti alle proteine strutturali. In cellule infette prive di NUP153, i livelli totali di proteine virali sono diminuiti, ma i rapporti sono cambiati: le proteine strutturali come E sono risultate relativamente sottorappresentate, mentre diverse proteine non strutturali (inclusi NS1, NS2B, NS3 e NS5) sono diventate più abbondanti rispetto a E. Questo spostamento non derivava da una degradazione proteica più rapida, ma piuttosto da una traduzione alterata della poliproteina virale. Di conseguenza, nelle fasi iniziali dell’infezione i virus nelle cellule carenti di NUP153 hanno avuto difficoltà ad assemblare e rilasciare particelle complete, ritardando la diffusione alle cellule vicine.
Un punto debole condiviso tra più virus
Gli autori hanno esteso le loro osservazioni oltre un singolo virus. Durante l’infezione da Zika, encefalite giapponese, West Nile, febbre gialla e dengue, NUP153 si è nuovamente spostata verso i siti dell’RNA virale e la sua rimozione ha ridotto in modo consistente sia la frazione di cellule infette sia il numero di particelle progenie prodotte. Poiché il motivo di RNA ricco di G che recluta NUP153 è conservato in questa famiglia di virus, e poiché il ruolo di NUP153 è di regolare finemente la miscela proteica necessaria per l’assemblaggio delle particelle, lo studio suggerisce una vulnerabilità comune e sfruttabile. Mirare all’interazione tra NUP153, l’RNA virale e le proteine virali—senza necessariamente distruggere i ruoli essenziali di NUP153 nella manutenzione cellulare—potrebbe fornire una nuova strategia diretta sull’ospite per antivirali ad ampio spettro.
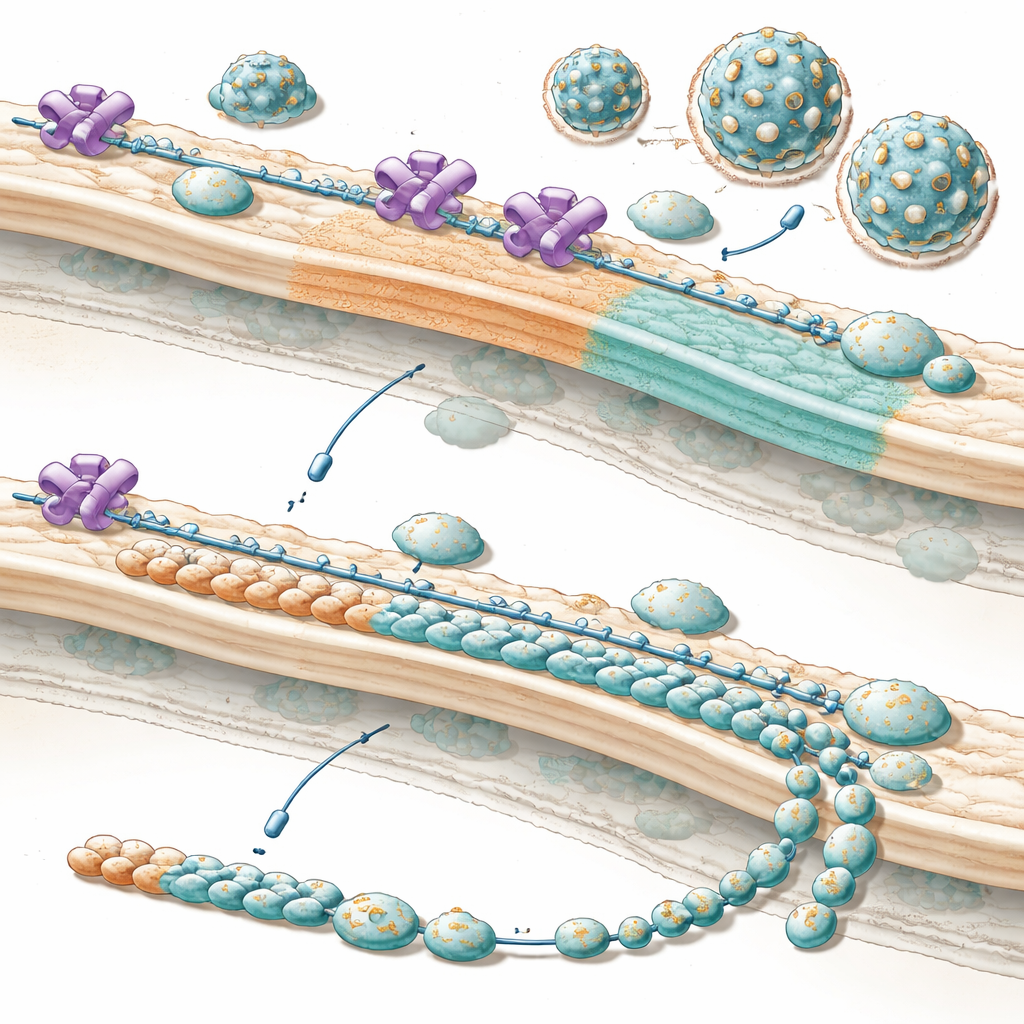
Perché questo è importante per i trattamenti futuri
In termini semplici, il lavoro mostra che questi virus sottraggono un guardiano cellulare e lo riconvertono in un responsabile della produzione, indirizzando la cellula a fabbricare più parti esterne necessarie per costruire nuove particelle virali al momento giusto. Quando NUP153 viene rimosso o bloccato, la «lista delle parti» si sbilancia: abbondano gli strumenti interni, ma mancano i pezzi dell’involucro, così emergono molte meno particelle infettive, soprattutto nelle fasi iniziali dell’infezione quando il tempismo è cruciale. Poiché questa strategia sembra conservata in molti flavivirus di rilevanza medica, interrompere con cura questa partnership dirottata tra virus e NUP153 potrebbe un giorno aiutare a prevenire o limitare infezioni gravi da un’intera famiglia di patogeni oggi difficili da trattare.
Citazione: Peters, M.B.A., Lindqvist, R., Kassa, E. et al. Proviral NUP153 binding to viral proteins and RNA regulates structural–nonstructural protein ratios in orthoflavivirus infection. Nat Commun 17, 3402 (2026). https://doi.org/10.1038/s41467-026-71449-1
Parole chiave: orthoflavivirus, NUP153, traduzione delle proteine virali, interazione ospite–virus, antivirali ad ampio spettro