Clear Sky Science · sv
INSIG1/2-succinering medierad av ADSL:s mångfunktion främjar lipogenes och levertumorigenes
Hur socker matar levertumörer
Varför törstar cancerceller efter socker, och hur omvandlar de det till byggmaterialet som krävs för att växa? Denna studie avslöjar en dold koppling inne i levercancerceller som länkar högt blodsocker direkt till fettproduktion och tumörtillväxt. Genom att spåra en kedja av händelser från glukos utanför cellen till fettbildande brytare inne i cellen visar forskarna också hur ett befintligt HIV-läkemedel skulle kunna omdisponeras för att bromsa levercancer.
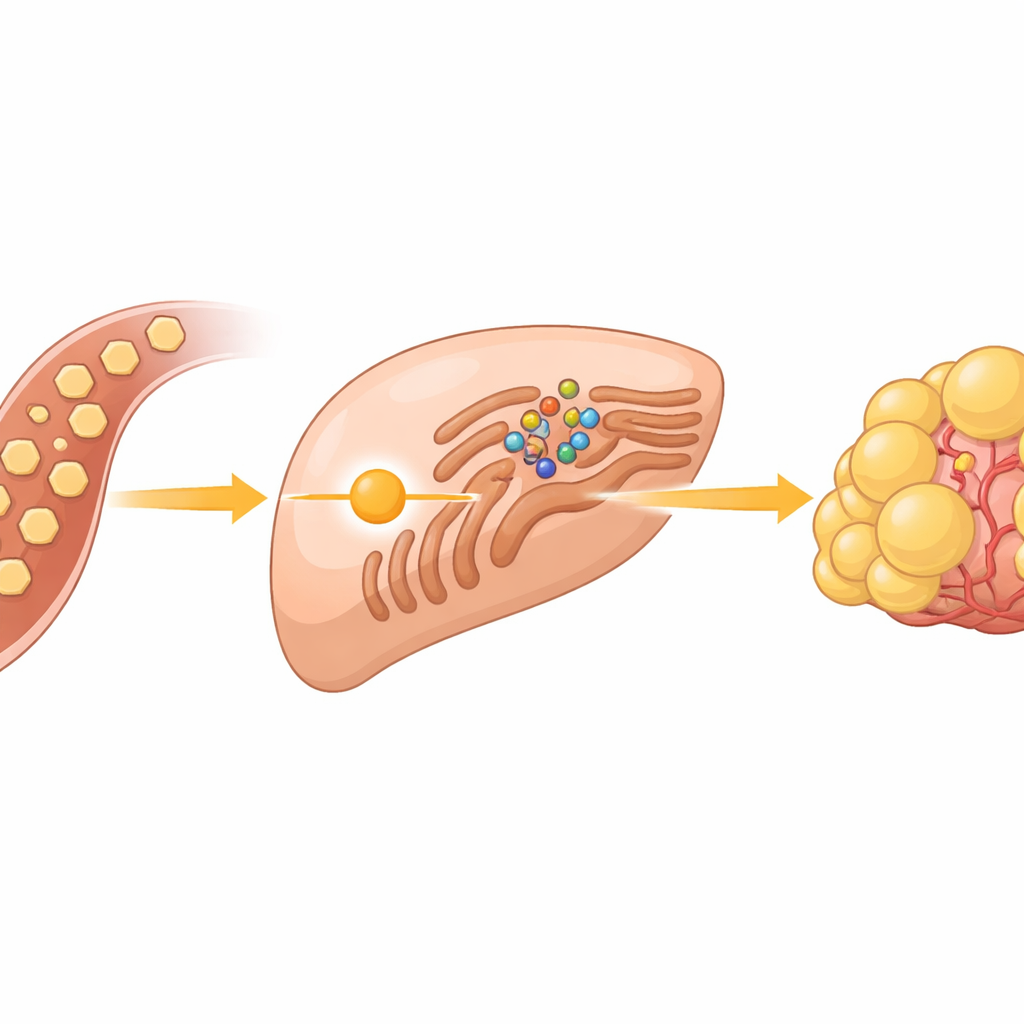
En dold sockersensor inne i cancerceller
Cancerceller är kända för att förbränna socker snabbt, även när syre finns tillgängligt, ett beteende känt som Warburg-effekten. I levertumörer gör detta sockerrus mer än att bara ge energi; det förser också byggstenar för fetter som bygger nya cellmembran. Forskarna fokuserade på en grupp proteiner kallade SREBPer, huvudbrytare som slår på gener för att tillverka fetter och kolesterol. Under normala förhållanden hålls dessa brytare tillbaka vid en cellstruktur som kallas endoplasmatiskt nätverk, där de låses på plats av ett sensorprotein som heter INSIG och dess partner SCAP. Den stora gåtan har varit hur överskott av glukos talar om för detta system att släppa SREBP och starta fettproduktionen.
Ett enzym med ett andra uppdrag
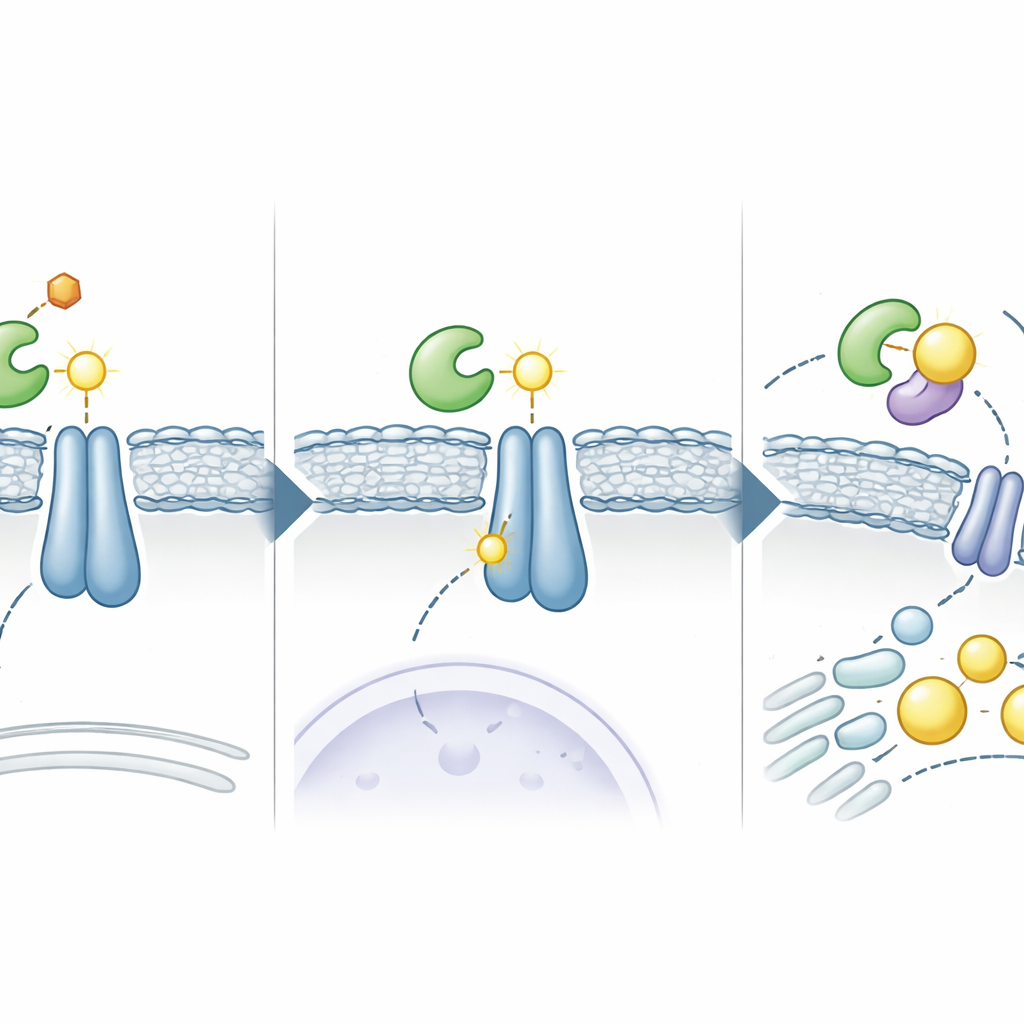
Forskarna upptäckte att ett enzym kallat ADSL, mest känt för att hjälpa celler bygga DNA-byggstenar, har ett överraskande andra jobb i levercancer. När glukosnivåerna är höga aktiverar det ett signaleringsenzym kallat PKCε. PKCε tillsätter sedan en fosfatgrupp till ADSL vid en specifik position, vilket får ADSL att förflytta sig från cellens vattenrika inre till ytan av det endoplasmatiska nätverket. Där binder ADSL fysiskt till INSIG-proteiner. Denna omlokalisering förvandlar ADSL från en enkel metabolisk arbetsmyra till en lokal kemisk fabrik som direkt kan påverka de fettbildande brytarna.
Kemisk ärrbildning som låser upp fettproduktion
När ADSL har parkerat intill INSIG genererar det en liten molekyl kallad fumarat som en del av sin vanliga kemi. I denna nya miljö reagerar fumarat med en särskild aminosyra på INSIG och bildar ett permanent kemiskt ”ärr” känt som succinering. Detta ärr bildas vid en nyckelcystein (C167 i INSIG1 och C111 i INSIG2) som normalt hjälper INSIG att binda oxysteroler, kolesterol-liknande budbärare som håller SCAP–SREBP-komplexet förankrat. Succineringen försvagar INSIG:s grepp om dessa budbärare och om SCAP, vilket tillåter SCAP–SREBP-komplexet att lämna det endoplasmatiska nätverket och resa till Golgi-kompartmentet. Där klyvs SREBP och dess aktiva fragment flyttar in i kärnan och slår på en svit gener som driver fett- och kolesterolproduktion, vilket ger bränsle åt snabb tumörcelltillväxt.
Från cellkretsar till läkemedelsomdisponering
För att undersöka om denna väg kunde vändas mot cancern använde forskarna datorbaserad screening av godkända läkemedel för att hitta molekyler som kunde kilas in i gränssnittet mellan ADSL och INSIG. De identifierade Elsulfavirine, ett HIV-läkemedel, som en stark kandidat. I laboratorieförsök och datorsimuleringar störde Elsulfavirine bindningen mellan ADSL och INSIG, minskade INSIG-succinering och blockerade SREBP-aktivering i levercancerceller. Som ett resultat tillverkade cellerna mindre fetter, lagrade färre lipidkärnor och växte långsammare. I musmodeller av levercancer krympte tumörerna med Elsulfavirine, och det fungerade ännu bättre i kombination med det standardläkemedlet mot levercancer, Lenvatinib, vilket antyder ett kraftfullt slag-påslag som riktar både tillväxtsignaler och metaboliska behov.
Vad detta betyder för patienter
För att knyta dessa fynd till verklig sjukdom undersökte teamet mänskliga levertumörprover. Tumörer med höga nivåer av fosforylerat ADSL, kraftigt succinerat INSIG och rikligt med SREBP i kärnan var kopplade till sämre patientöverlevnad. Med andra ord verkar samma sockersensoriska krets som kartlagts i celler och möss vara aktiv i aggressiva mänskliga levertumörer. Arbetet visar att levertumörer direkt kan känna av extra glukos och omvandla det till ett tillväxtfrämjande fettprogram genom ADSL:s "månfunktion". Det framhäver också Elsulfavirine som en lovande kandidat för omdisponering och öppnar en möjlig ny strategi för att stänga av den fetttillförsel som levertumörer behöver för att frodas.
Citering: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
Nyckelord: levercancer, cancermetabolism, lipogenes, SREBP-vägen, läkemedelsomdisponering