Clear Sky Science · pl
INSIG1/2 uleganie sukcynacji pośredniczone przez „moonlightingową” funkcję ADSL sprzyja lipogenezie i nowotworzeniu w wątrobie
Jak cukier karmi nowotwory w wątrobie
Dlaczego komórki nowotworowe pożądają cukru i jak przekształcają go w substraty niezbędne do wzrostu? To badanie odsłania ukrytą sieć w komórkach raka wątroby, która łączy wysoki poziom glukozy bezpośrednio z produkcją tłuszczów i rozwojem guza. Śledząc łańcuch zdarzeń od glukozy na zewnątrz komórki po przełączniki produkcji lipidów głęboko wewnątrz niej, naukowcy ujawniają też, jak istniejący lek przeciw HIV mógłby zostać przerobiony, by spowolnić raka wątroby.
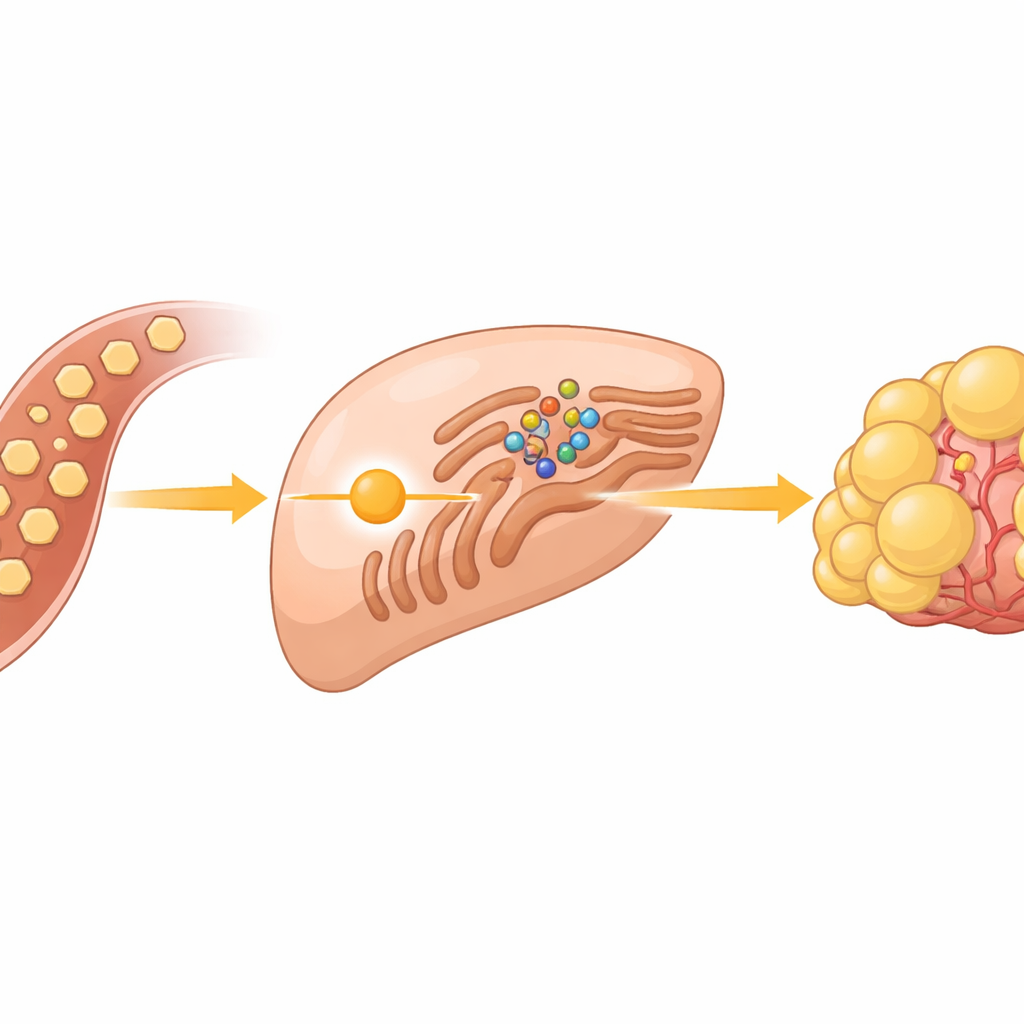
Ukryty czujnik cukru wewnątrz komórek nowotworowych
Komórki nowotworowe są znane z szybkiego spalania cukru, nawet gdy tlen jest dostępny — zachowanie to znane jest jako efekt Warburga. W guzach wątroby ten napływ cukru robi więcej niż dostarcza energii; zasila też tworzenie tłuszczów potrzebnych do budowy nowych błon komórkowych. Zespół skupił się na grupie białek zwanych SREBP, głównych regulatorach włączających geny odpowiedzialne za syntezę lipidów i cholesterolu. W normalnych warunkach te przełączniki są utrzymywane w stanie nieaktywności w strukturze komórkowej zwanej retikulum endoplazmatycznym, gdzie są unieruchomione przez białko-czujnik INSIG i jego partnera SCAP. Wielką zagadką było, w jaki sposób nadmiar glukozy nakazuje temu systemowi uwolnić SREBP i rozpocząć produkcję tłuszczów.
Enzym z drugą rolą
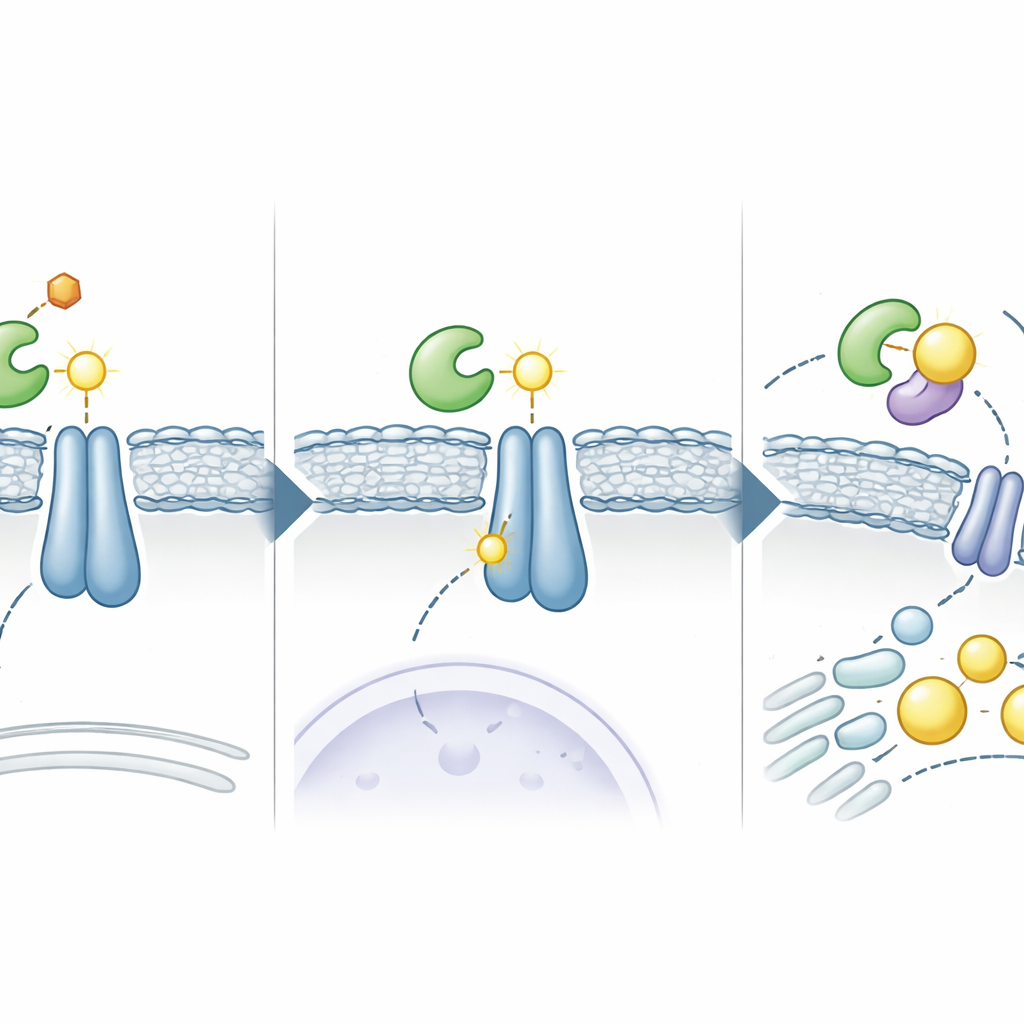
Naukowcy odkryli, że enzym o nazwie ADSL, znany przede wszystkim z udziału w syntezie elementów budulcowych DNA, ma zaskakującą drugą funkcję w raku wątroby. Gdy poziomy glukozy są wysokie, aktywuje się kinaza PKCε. PKCε następnie przyłącza grupę fosforanową do ADSL w określonym miejscu, co powoduje przemieszczenie ADSL z wodnego wnętrza komórki na powierzchnię retikulum endoplazmatycznego. Tam ADSL fizycznie wiąże się z białkami INSIG. To przemieszczanie przekształca ADSL z prostego enzymu metabolicznego w lokalną „fabrykę chemiczną”, która może bezpośrednio wpływać na przełączniki produkcji lipidów.
Chemiczne bliznowacenie, które odblokowuje produkcję tłuszczu
Gdy ADSL przylega obok INSIG, wytwarza jako część swojej standardowej reakcji małą cząsteczkę — fumaran. W tym nowym otoczeniu fumaran reaguje z określonym aminokwasem w INSIG, tworząc trwałą chemiczną „bliznę” zwaną sukcynacją. Blizna powstaje w kluczowym reszcie cysteinowej (C167 w INSIG1 i C111 w INSIG2), która normalnie pomaga INSIG wiązać oksysterole — związki podobne do cholesterolu, które utrzymują kompleks SCAP–SREBP przyłączony w retikulum endoplazmatycznym. Sukcynacja osłabia przyczepność INSIG do tych sygnałowych cząsteczek i do SCAP, pozwalając kompleksowi SCAP–SREBP opuścić retikulum endoplazmatyczne i przemieścić się do aparatu Golgiego. Tam SREBP zostaje przecięty, a jego aktywny fragment wchodzi do jądra, aktywując zestaw genów napędzających produkcję tłuszczów i cholesterolu, co zasila szybki wzrost komórek nowotworowych.
Od obwodów komórkowych do repurposingowania leków
Aby sprawdzić, czy tę ścieżkę można obrócić przeciwko nowotworowi, naukowcy użyli komputerowego przeszukiwania zatwierdzonych leków, by znaleźć molekuły mogące wciskać się w interfejs między ADSL a INSIG. Zidentyfikowali Elsulfawirynę, lek przeciw HIV, jako obiecujący kandydat. W eksperymentach laboratoryjnych i symulacjach komputerowych Elsulfawiryna zaburzała wiązanie między ADSL a INSIG, zmniejszała sukcynację INSIG i blokowała aktywację SREBP w komórkach raka wątroby. W efekcie komórki wytwarzały mniej tłuszczów, gromadziły mniej kropli lipidowych i rosły wolniej. W modelach mysich raka wątroby Elsulfawiryna zmniejszała guzy, a działanie było jeszcze silniejsze, gdy łączono ją ze standardowym lekiem na raka wątroby, lenvatynibem, sugerując potężne dwutorowe uderzenie, które celuje zarówno w sygnały wzrostu, jak i zapotrzebowanie metaboliczne.
Co to oznacza dla pacjentów
Aby powiązać te odkrycia z rzeczywistą chorobą, zespół przeanalizował próbki ludzkich guzów wątroby. Guzy z wysokim poziomem fosforylowanego ADSL, silnie sukcynowanym INSIG i obfitą obecnością SREBP w jądrze wiązały się z gorszym przeżyciem pacjentów. Innymi słowy, ten sam układ wykrywania cukru zmapowany w komórkach i myszach wydaje się być aktywny w agresywnych nowotworach wątroby u ludzi. Praca pokazuje, że guzy wątroby potrafią bezpośrednio wykrywać nadmiar glukozy i przekształcać go w program pro-wzrostowy oparty na tłuszczach dzięki „moonlightingowej” funkcji ADSL. Wyróżnia też Elsulfawirynę jako obiecujący kandydat do ponownego zastosowania, otwierając potencjalną nową strategię odcięcia dostaw tłuszczu, których guzy wątroby potrzebują do rozwoju.
Cytowanie: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
Słowa kluczowe: rak wątroby, metabolizm nowotworów, lipogeneza, szlak SREBP, repurposing leków