Clear Sky Science · ar
تخثُّر INSIG1/2 بوساطة وظيفة ADSL الثانوية يعزز تكوّن الدهون وتسرطن الكبد
كيف يغذي السكر أورام الكبد
لماذا تتوق خلايا السرطان إلى السكر، وكيف تحوّله إلى المواد الخام اللازمة للنمو؟ تكشف هذه الدراسة عن دارة خفية داخل خلايا سرطان الكبد تربط ارتفاع السكر في الدم مباشرةً بإنتاج الدهون ونمو الورم. عبر تتبع سلسلة من الأحداث من الجلوكوز خارج الخلية إلى مفاتيح صناعة الدهون العميقة داخلها، يكشف الباحثون أيضاً كيف يمكن إعادة توظيف دواء مضاد للـ HIV لتباطؤ تقدم سرطان الكبد.
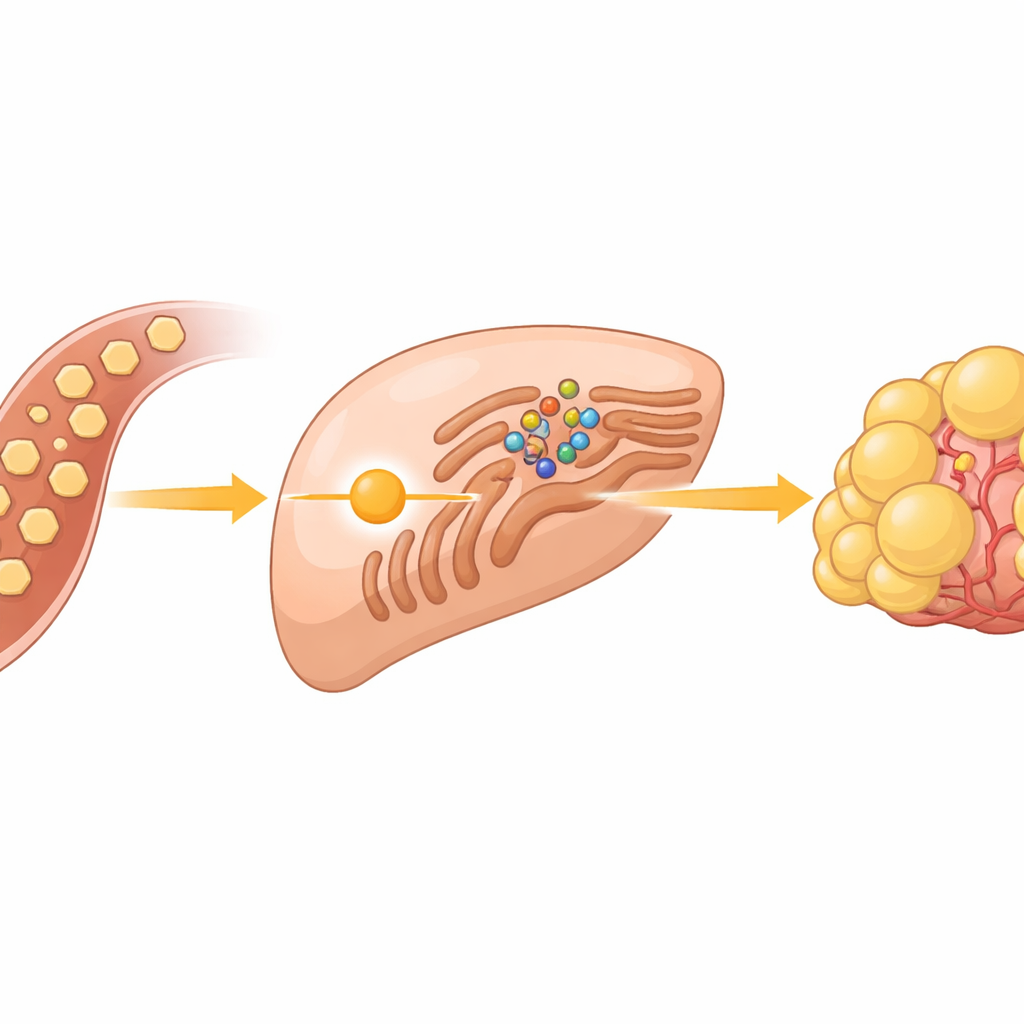
مستشعر سُكّري خفي داخل خلايا السرطان
تشتهر خلايا السرطان بإحراق السكر بسرعة، حتى عندما يتوفر الأكسجين بكثرة، وهو سلوك معروف بتأثير واربورغ. في أورام الكبد، لا يقتصر هذا الطوفان السكري على توفير الطاقة فحسب؛ بل يمد أيضاً تصنيع الدهون اللازمة لبناء أغشية الخلايا الجديدة. ركز الفريق على مجموعة بروتينات تُدعى SREBPs، وهي مفاتيح رئيسية تشغّل جينات تكوين الدهون والكولسترول. في الظروف الطبيعية، تُكبَح هذه المفاتيح في بنية خلوية تُسمى الشبكة الإندوبلازمية، حيث تُثبَّت بواسطة بروتين مستشعر يُدعى INSIG وشريكه SCAP. وكان اللغز الكبير كيف يخبر جلوكوز زائد هذا النظام أن يطلق SREBPs ويشرع في إنتاج الدهون.
إنزيم ذو وظيفة ثانية
اكتشف الباحثون أن إنزيمًا يُدعى ADSL، المعروف أساسًا بمساعدته للخلايا على تصنيع لبنات بناء الحمض النووي، يقوم بوظيفة ثانية مفاجئة في سرطان الكبد. عندما ترتفع مستويات الجلوكوز، ينشّط ذلك إنزيم إشاري يُدعى PKCε. يقوم PKCε بعد ذلك بإضافة مجموعة فوسفات إلى ADSL في موقع محدد، مما يدفع ADSL للانتقال من السيتوسول إلى سطح الشبكة الإندوبلازمية. هناك، يرتبط ADSL جسدياً ببروتينات INSIG. هذا الانتقال يحول ADSL من عامل أيضي بسيط إلى مصنع كيميائي محلي يمكنه التأثير مباشرة على مفاتيح صناعة الدهون.
ندوب كيميائية تفتح إنتاج الدهون
عندما يتموضع ADSL بجانب INSIG، ينتج جزيئاً صغيراً يُدعى الفومارات كجزء من تفاعلاته الاعتيادية. في هذا الموضع الجديد، يتفاعل الفومارات مع حمض أميني معين على INSIG، مكونًا "ندبة" كيميائية دائمة تُعرف بالتخثّر (succination). تتكون هذه الندبة عند موقع سيستيين حاسم (C167 في INSIG1 وC111 في INSIG2) الذي يساعد عادة INSIG على الارتباط بالأوكسستيرولات، وهي رسل تشبه الكولسترول تبقي مركب SCAP–SREBP مثبتًا في مكانه. يضعف التخثّر قبضة INSIG على هذه الرسل وعلى SCAP، مما يسمح لمركب SCAP–SREBP بمغادرة الشبكة الإندوبلازمية والانتقال إلى جهاز جولجي. هناك يُقصّ SREBP وينتقل شِظيه الفعّال إلى النواة، ليشغّل مجموعة جينات تدفع إنتاج الدهون والكولسترول، مما يغذي النمو السريع لخلايا الورم.
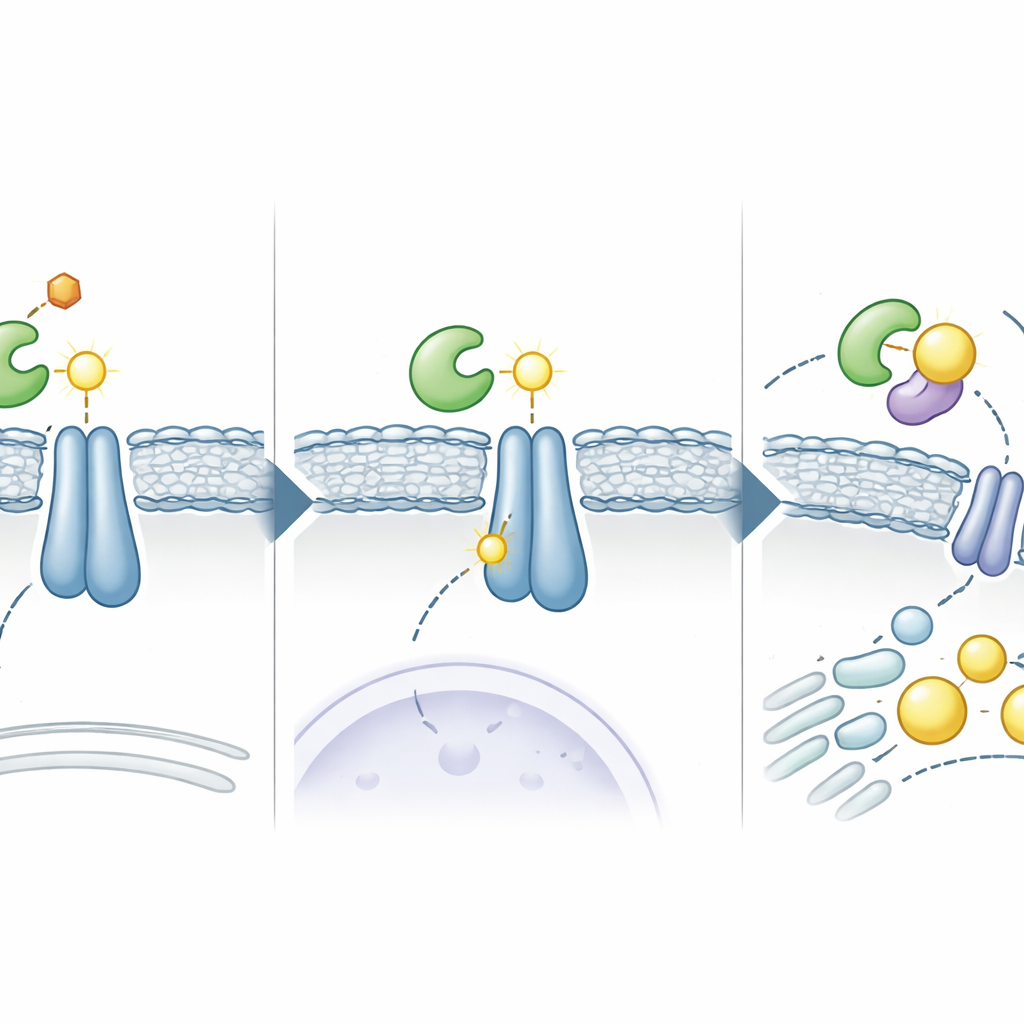
من دوائر خلوية إلى إعادة توظيف الأدوية
لاختبار ما إذا كان يمكن تحويل هذا المسار ضد السرطان، استخدم العلماء فحصًا حاسوبيًا للأدوية المعتمدة للعثور على جزيئات قد تعرقل واجهة الارتباط بين ADSL وINSIG. حدّدوا الإلسولفافيرين (Elsulfavirine)، دواءً مضادًا لفيروس HIV، كمرشح قوي. في تجارب مخبرية ومحاكاة حاسوبية، قطَع الإلسولفافيرين رابطة ADSL–INSIG، قلّل من تخثّر INSIG، ومنع تنشيط SREBP في خلايا سرطان الكبد. ونتيجة لذلك، أنتجت الخلايا دهونًا أقل، وخزّنت قطيرات دهنية أقل، ونمت ببطء أكبر. في نماذج فأرية لسرطان الكبد، قلّل الإلسولفافيرين من حجم الأورام، وكان تأثيره أفضل عند جمعه مع دواء سرطان الكبد القياسي لِنفاتينيب، مما يشير إلى ضربة مزدوجة قوية تستهدف إشارات النمو والاحتياجات الأيضية معًا.
ماذا يعني هذا للمرضى
لربط هذه النتائج بالمرض الحقيقي، فحص الفريق عينات أورام كبد بشرية. ارتبطت الأورام ذات المستويات العالية من ADSL فسفوریل، وINSIG متخثّر بشدة، ووجود وفير لـ SREBP في النواة بتدهور بقاء المرضى. بعبارة أخرى، يبدو أن نفس دائرة استشعار السكر المرسومة في الخلايا والفئران نشطة في حالات سرطان الكبد البشري العدوانية. تُظهر الدراسة أن أورام الكبد يمكنها استشعار الجلوكوز الزائد وتحويله مباشرة إلى برنامج دهني محفز للنمو عبر وظيفة ADSL الثانوية. كما تبرز الإلسولفافيرين كمرشح واعد لإعادة التوظيف، فاتحةً استراتيجية محتملة لقطع تزويد الدهون الذي تحتاجه أورام الكبد لتزدهر.
الاستشهاد: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
الكلمات المفتاحية: سرطان الكبد, تمثيل الأورام الغذائي, تكوّن الدهون, مسار SREBP, إعادة توظيف الأدوية