Clear Sky Science · it
La succinazione di INSIG1/2 mediata dalla funzione moonlighting di ADSL promuove la lipogenesi e la tumorigenesi epatica
Come lo zucchero nutre i tumori del fegato
Perché le cellule tumorali bramano lo zucchero e come lo trasformano nelle materie prime necessarie per crescere? Questo studio svela un circuito nascosto nelle cellule del carcinoma epatico che collega direttamente l'iperglicemia alla produzione di lipidi e alla crescita tumorale. Tracciando una catena di eventi dal glucosio esterno alla cellula fino agli interruttori della sintesi lipidica all'interno, i ricercatori mostrano anche come un farmaco già impiegato contro l'HIV potrebbe essere riproposto per rallentare il cancro del fegato.
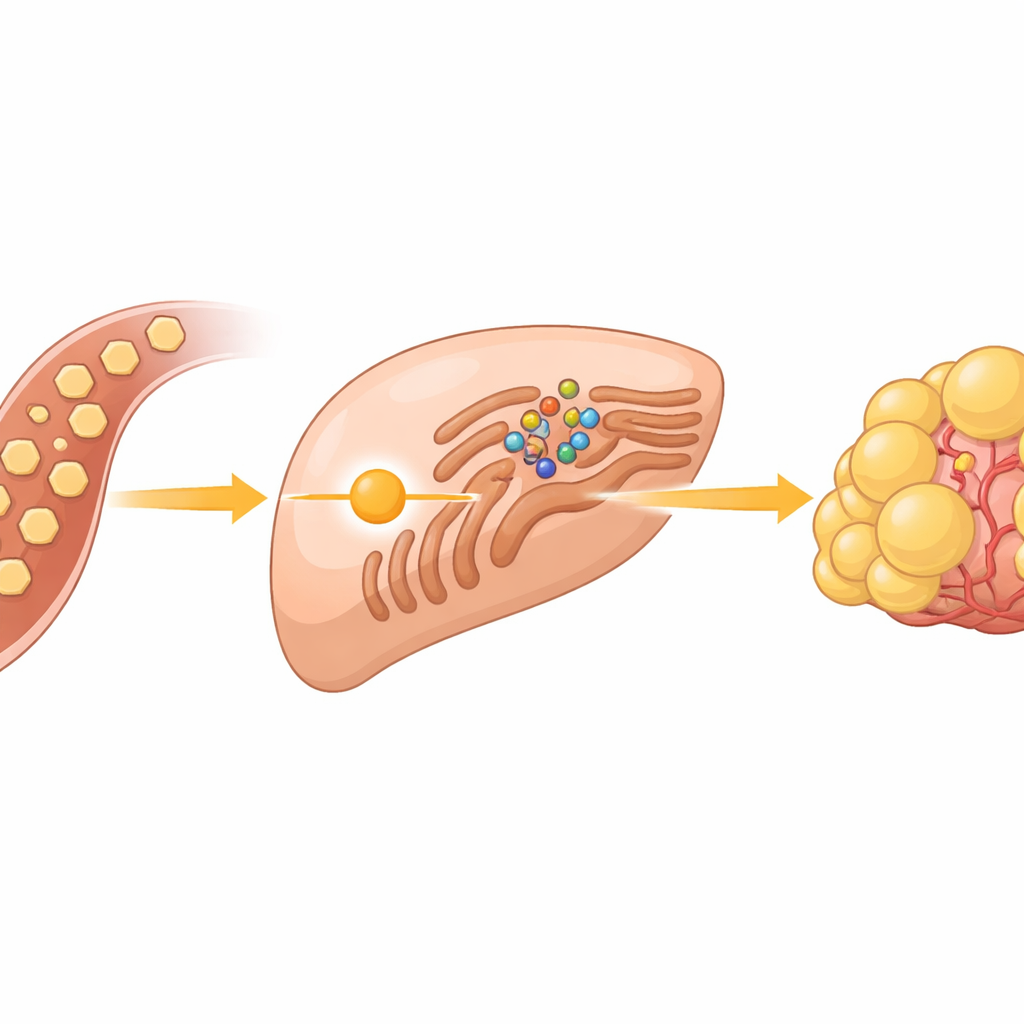
Un sensore di zucchero nascosto nelle cellule tumorali
Le cellule tumorali sono famose per consumare rapidamente zucchero, anche quando l'ossigeno è abbondante, un comportamento noto come effetto Warburg. Nei tumori epatici questa corsa allo zucchero fa più che fornire energia: alimenta anche la sintesi di lipidi necessari per costruire nuove membrane cellulari. Il gruppo si è concentrato su una famiglia di proteine chiamate SREBP, interruttori principali che attivano i geni per la produzione di grassi e colesterolo. In condizioni normali questi interruttori sono trattenuti in uno spazio cellulare chiamato reticolo endoplasmatico, dove sono fissati da una proteina sensore chiamata INSIG e dal suo partner SCAP. Il grande mistero era come il glucosio in eccesso comunicasse a questo sistema di rilasciare le SREBP e avviare la produzione lipidica.
Un enzima con un secondo lavoro
I ricercatori hanno scoperto che un enzima chiamato ADSL, noto soprattutto per il suo ruolo nella sintesi dei mattoni del DNA, svolge un sorprendente secondo mestiere nel cancro epatico. Quando i livelli di glucosio sono alti, viene attivata una chinasi di segnalazione chiamata PKCε. PKCε aggiunge quindi un gruppo fosfato su ADSL in una posizione specifica, inducendo il trasferimento di ADSL dal citosol alla superficie del reticolo endoplasmatico. Lì ADSL si lega fisicamente alle proteine INSIG. Questo riposizionamento trasforma ADSL da semplice enzima metabolico in una fabbrica chimica locale in grado di influenzare direttamente gli interruttori della sintesi lipidica.
Cicatrici chimiche che sbloccano la produzione di lipidi
Una volta che ADSL è posizionata accanto a INSIG, genera una piccola molecola chiamata fumarato come parte della sua normale attività. In questo nuovo contesto il fumarato reagisce con un amminoacido specifico di INSIG, formando una “cicatrice” chimica permanente nota come succinazione. Questa modifica avviene in un sito critico di cisteina (C167 in INSIG1 e C111 in INSIG2) che normalmente facilita il legame di INSIG con gli ossisteroli, messaggeri simili al colesterolo che mantengono il complesso SCAP–SREBP ancorato. La succinazione indebolisce l’affinità di INSIG per questi messaggeri e per SCAP, permettendo al complesso SCAP–SREBP di lasciare il reticolo endoplasmatico e migrare al Golgi. Lì SREBP viene scisso e il frammento attivo entra nel nucleo, attivando una serie di geni che guidano la sintesi di lipidi e colesterolo e alimentano la rapida crescita delle cellule tumorali.
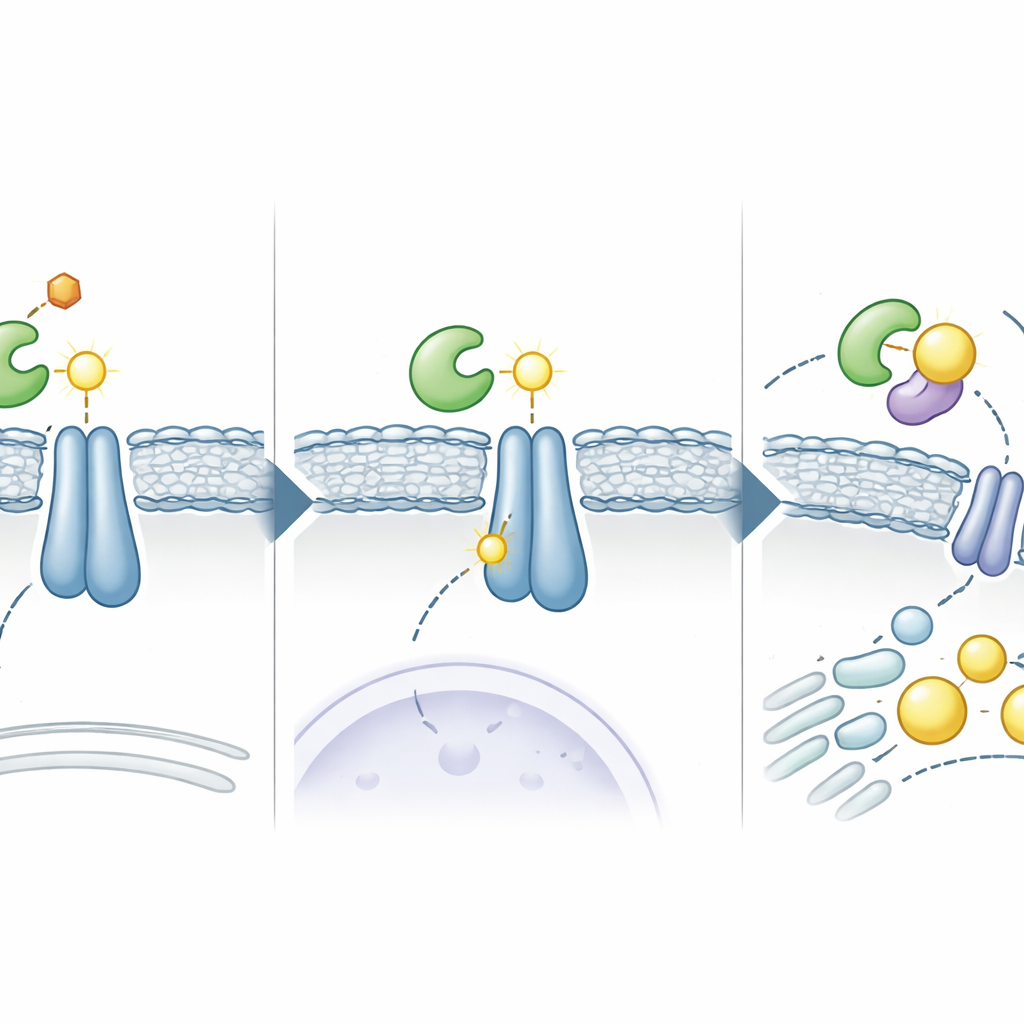
Dal circuito cellulare al riutilizzo di farmaci
Per verificare se questa via potesse essere sfruttata contro il tumore, gli scienziati hanno eseguito uno screening computazionale su farmaci approvati per individuare molecole in grado di inserirsi nell’interfaccia tra ADSL e INSIG. Hanno identificato l’Elsulfavirina, un farmaco per l'HIV, come candidato promettente. In esperimenti in vitro e tramite simulazioni al computer, l’Elsulfavirina ha disturbato il legame tra ADSL e INSIG, ridotto la succinazione di INSIG e bloccato l’attivazione di SREBP nelle cellule di carcinoma epatico. Di conseguenza le cellule hanno sintetizzato meno lipidi, accumulato meno goccioline lipidiche e presentato una crescita più lenta. In modelli murini di tumore epatico, l’Elsulfavirina ha ridotto le dimensioni dei tumori, con un’efficacia ancora maggiore se combinata con il farmaco standard per il carcinoma epatico Lenvatinib, suggerendo una potente combinazione che colpisce sia i segnali di crescita sia le esigenze metaboliche.
Cosa significa per i pazienti
Per collegare questi risultati alla malattia umana, il team ha analizzato campioni di tumori epatici umani. I tumori con alti livelli di ADSL fosforilata, INSIG fortemente succinata e abbondante SREBP nucleare erano associati a una sopravvivenza peggiore dei pazienti. In altre parole, lo stesso circuito sensibile allo zucchero mappato nelle cellule e nei topi sembra essere attivo nei carcinomi epatici umani più aggressivi. Il lavoro dimostra che i tumori del fegato possono percepire direttamente l’eccesso di glucosio e convertirlo in un programma pro‑crescita di sintesi lipidica tramite la funzione “moonlighting” di ADSL. Evidenzia inoltre l’Elsulfavirina come candidato promettente per il riposizionamento farmacologico, aprendo una strategia potenziale per tagliare l’approvvigionamento lipidico di cui i tumori epatici hanno bisogno per prosperare.
Citazione: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
Parole chiave: cancro del fegato, metabolismo del cancro, lipogenesi, via SREBP, riutilizzo di farmaci