Clear Sky Science · ru
Сукинация INSIG1/2, опосредованная «второй» функцией ADSL, способствует липогенезу и опухолеобразованию в печени
Как сахар подпитывает опухоли печени
Почему раковые клетки так «жаждут» сахара и как они превращают его в сырьё, необходимое для роста? В этом исследовании выявлена скрытая связь внутри клеток рака печени, которая напрямую связывает высокий уровень глюкозы в крови с образованием жиров и ростом опухоли. Проследив цепочку событий от глюкозы снаружи клетки до переключателей липогенеза глубоко внутри, учёные также показали, как уже существующий препарат от ВИЧ можно перепрофилировать, чтобы замедлить рак печени.
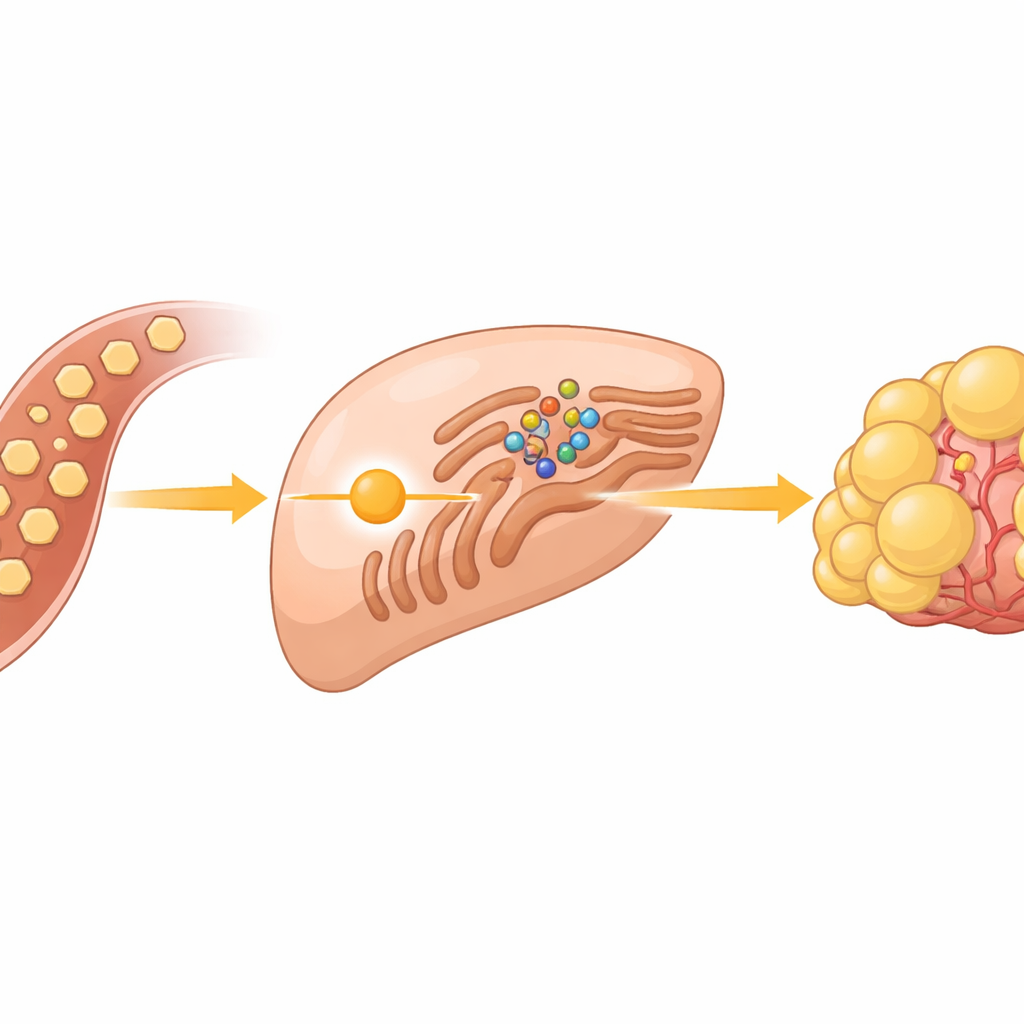
Скрытый сенсор сахара внутри раковых клеток
Раковые клетки известны тем, что быстро «сжигают» сахар, даже при наличии кислорода — поведение, известное как эффект Варбурга. В опухолях печени этот прилив сахара делает больше, чем просто даёт энергию: он также питает синтез жиров, необходимых для строительства новых клеточных мембран. Группа сосредоточилась на белках SREBP — главных переключателях, которые включают гены, отвечающие за синтез жиров и холестерина. В норме эти переключатели удерживаются в клеточной структуре, называемой эндоплазматическим ретикулумом, где их фиксирует сенсорный белок INSIG и его партнёр SCAP. Большая загадка заключалась в том, как избыток глюкозы заставляет эту систему отпускать SREBP и запускать синтез жиров.
Фермент с «второй работой»
Исследователи обнаружили, что фермент ADSL, широко известный своей ролью в синтезе строительных блоков ДНК, выполняет удивительную вторую функцию при раке печени. При высоком уровне глюкозы активируется сигнальный фермент PKCε. PKCε фосфорилирует ADSL в определённой позиции, что побуждает ADSL переместиться из водной цитоплазмы на поверхность эндоплазматического ретикулума. Там ADSL физически связывается с белками INSIG. Это перемещение превращает ADSL из простого метаболического «трудяги» в локальную химическую фабрику, способную напрямую влиять на переключатели липогенеза.
Химические «шрамы», которые разблокируют синтез жиров
Попав рядом с INSIG, ADSL производит малую молекулу фумарат в рамках своей обычной реакции. В этом новом окружении фумарат реагирует с определённой аминокислотой в INSIG, образуя постоянный химический «шрам», известный как сукинация. Этот «шрам» возникает в ключевом остатке цистеина (C167 в INSIG1 и C111 в INSIG2), который обычно помогает INSIG связывать оксистеролы — молекулы, похожие на холестерин, удерживающие комплекс SCAP–SREBP на месте. Сукинация ослабляет сцепление INSIG с этими посланниками и с SCAP, позволяя комплексу SCAP–SREBP покинуть эндоплазматический ретикулум и отправиться в комплекс Гольджи. Там SREBP расщепляется, а его активный фрагмент попадает в ядро, включая набор генов, ведущих к синтезу жиров и холестерина и стимулируя быстрый рост опухолевых клеток.
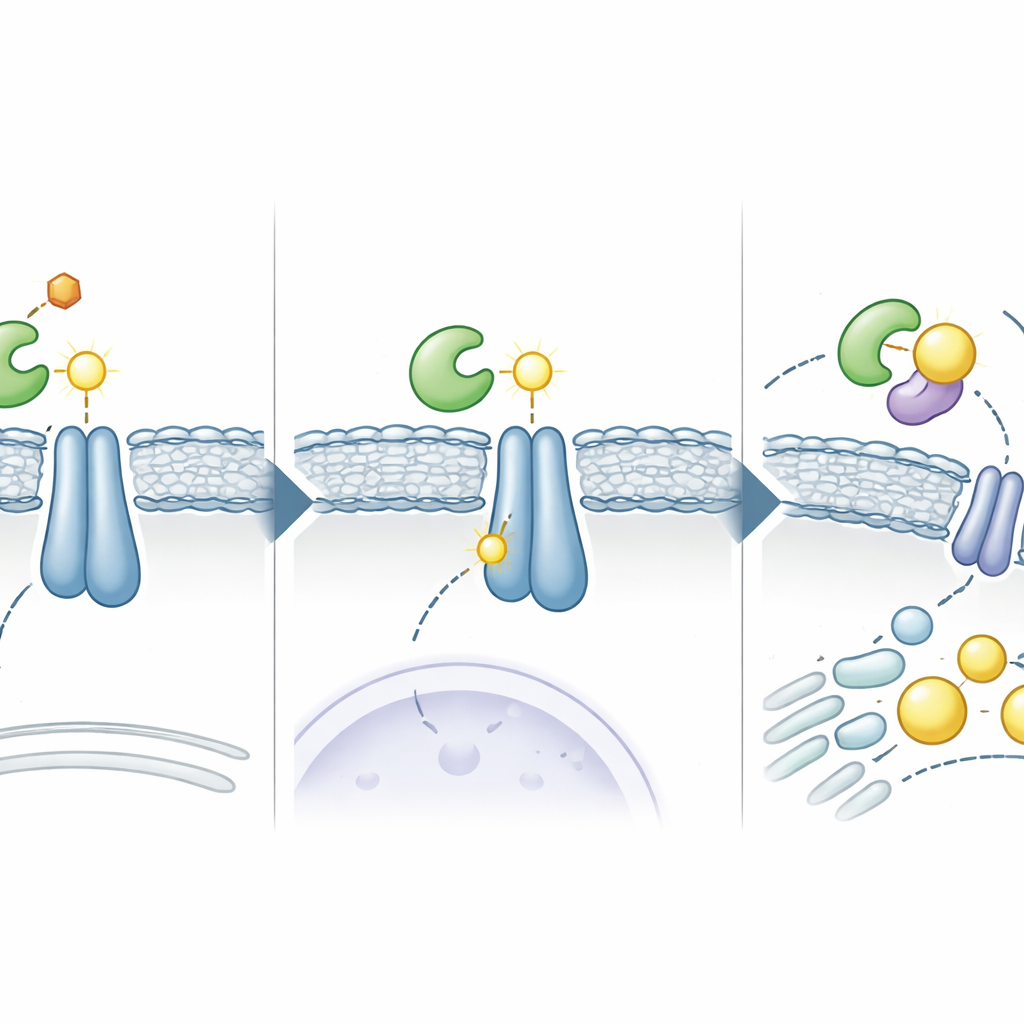
От клеточных схем к переназначению препаратов
Чтобы проверить, можно ли использовать этот путь против рака, учёные провели компьютерный скрининг одобренных препаратов в поисках молекул, которые могли бы внедриться в интерфейс между ADSL и INSIG. Они выделили эсульфавирин (Elsulfavirine), препарат от ВИЧ, как сильный кандидат. В лабораторных опытах и компьютерных моделях эсульфавирин нарушал связывание между ADSL и INSIG, снижал сукинацию INSIG и блокировал активацию SREBP в клетках рака печени. В результате клетки синтезировали меньше жиров, накапливали меньше липидных капель и росли медленнее. В моделях рака печени на мышах эсульфавирин уменьшал опухоли, а в комбинации со стандартным препаратом для лечения рака печени ленватинибом эффект был ещё сильнее, что указывает на мощное сочетание, направленное и на сигнальные пути, и на метаболические потребности.
Что это значит для пациентов
Чтобы связать эти результаты с клинической практикой, команда изучила образцы опухолей печени человека. Опухоли с высоким уровнем фосфорилированного ADSL, выраженной сукинацией INSIG и обилием SREBP в ядре были связаны с худшим выживанием пациентов. Иными словами, та же схема чувствования сахара, показанная в клеточных и мышиных моделях, по‑видимому, активна и в агрессивных опухолях печени у людей. Работа демонстрирует, что опухоли печени могут напрямую ощущать избыток глюкозы и превращать его в провоспалительную программу синтеза жиров через «вторую» функцию ADSL. Исследование также выделяет эсульфавирин как перспективного кандидата для переназначения, открывая потенциально новую стратегию перекрытия жирового снабжения, необходимого опухолям печени для процветания.
Цитирование: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
Ключевые слова: рак печени, метаболизм рака, липодогенез, путь SREBP, переназначение препаратов