Clear Sky Science · nl
INSIG1/2-succinatie gemedieerd door de moonlighting-functie van ADSL bevordert lipogenese en levertumorigenese
Hoe suiker levertumoren voedt
Waarom verlangen kankercellen naar suiker en hoe zetten ze die om in de bouwstoffen die nodig zijn om te groeien? Deze studie onthult een verborgen schakeling in leverkankercellen die hoge bloedsuikers direct koppelt aan vetvorming en tumorgroei. Door een keten van gebeurtenissen te volgen van glucose buiten de cel tot de vetmakende schakelaars diep vanbinnen, laten de onderzoekers ook zien hoe een bestaand hiv-middel mogelijk kan worden hergebruikt om leverkanker te remmen.
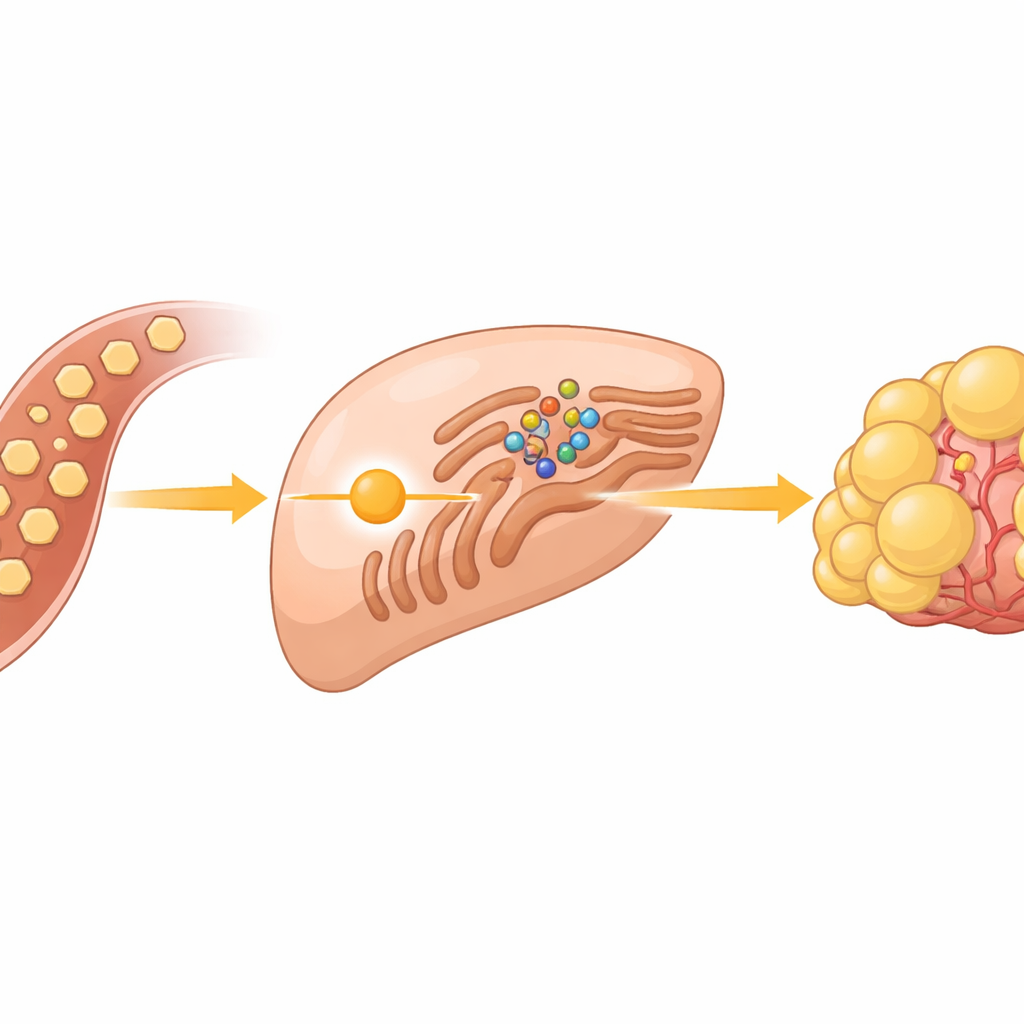
Een verborgen suikersensor binnen kankercellen
Kankercellen staan erom bekend suiker razendsnel te verbranden, zelfs als er genoeg zuurstof is—een gedrag dat bekendstaat als het Warburg-effect. In levertumoren doet deze suikerstroom meer dan alleen energie leveren; ze voedt ook de aanmaak van vetten die nieuwe celmembranen bouwen. Het team concentreerde zich op een groep eiwitten genaamd SREBPs, meesterregelaars die genen voor vet- en cholesterolproductie inschakelen. Onder normale omstandigheden worden deze schakelaars in toom gehouden in een cellulair compartiment, het endoplasmatisch reticulum, waar ze op hun plaats worden gehouden door een sensor-eiwit genaamd INSIG en diens partner SCAP. De grote vraag was hoe extra glucose dit systeem aangeeft om SREBPs los te laten en vetproductie te starten.
Een enzym met een tweede taak
De onderzoekers ontdekten dat een enzym genaamd ADSL, vooral bekend om zijn rol bij de opbouw van DNA-voorlopers, een verrassende tweede taak heeft in leverkanker. Wanneer de glucosespiegels hoog zijn, activeert dat een signaalenzym genaamd PKCε. PKCε voegt vervolgens een fosfaatlabel toe aan ADSL op een specifieke positie, wat ADSL ertoe aanzet van het waterige binnenste van de cel naar het oppervlak van het endoplasmatisch reticulum te verplaatsen. Daar hecht ADSL zich fysiek aan INSIG-eiwitten. Deze herlokalisatie verandert ADSL van een eenvoudige metabole werkpaard in een lokale chemische fabriek die direct invloed kan uitoefenen op de vetmakende schakelaars.
Chemische littekens die vetproductie ontgrendelen
Zodra ADSL naast INSIG is gepositioneerd, genereert het een klein molecuul genaamd fumaraat als onderdeel van zijn gebruikelijke chemie. In deze nieuwe omgeving reageert fumaraat met een specifiek aminozuur op INSIG en vormt een permanent chemisch “litteken” dat bekendstaat als succinatie. Dit litteken ontstaat op een belangrijk cysteïne-residu (C167 in INSIG1 en C111 in INSIG2) dat normaal helpt INSIG te binden aan oxysterolen, cholesterolachtige boodschappers die het SCAP–SREBP-complex verankerd houden. Succinatie verzwakt INSIGs greep op deze boodschappers en op SCAP, waardoor het SCAP–SREBP-complex het endoplasmatisch reticulum kan verlaten en naar het Golgi-compartiment kan reizen. Daar wordt SREBP geknipt en gaat het actieve fragment de kern in, waar het een reeks genen activeert die vet- en cholesterolproductie aanjagen en zo snelle tumorgroei voeden.
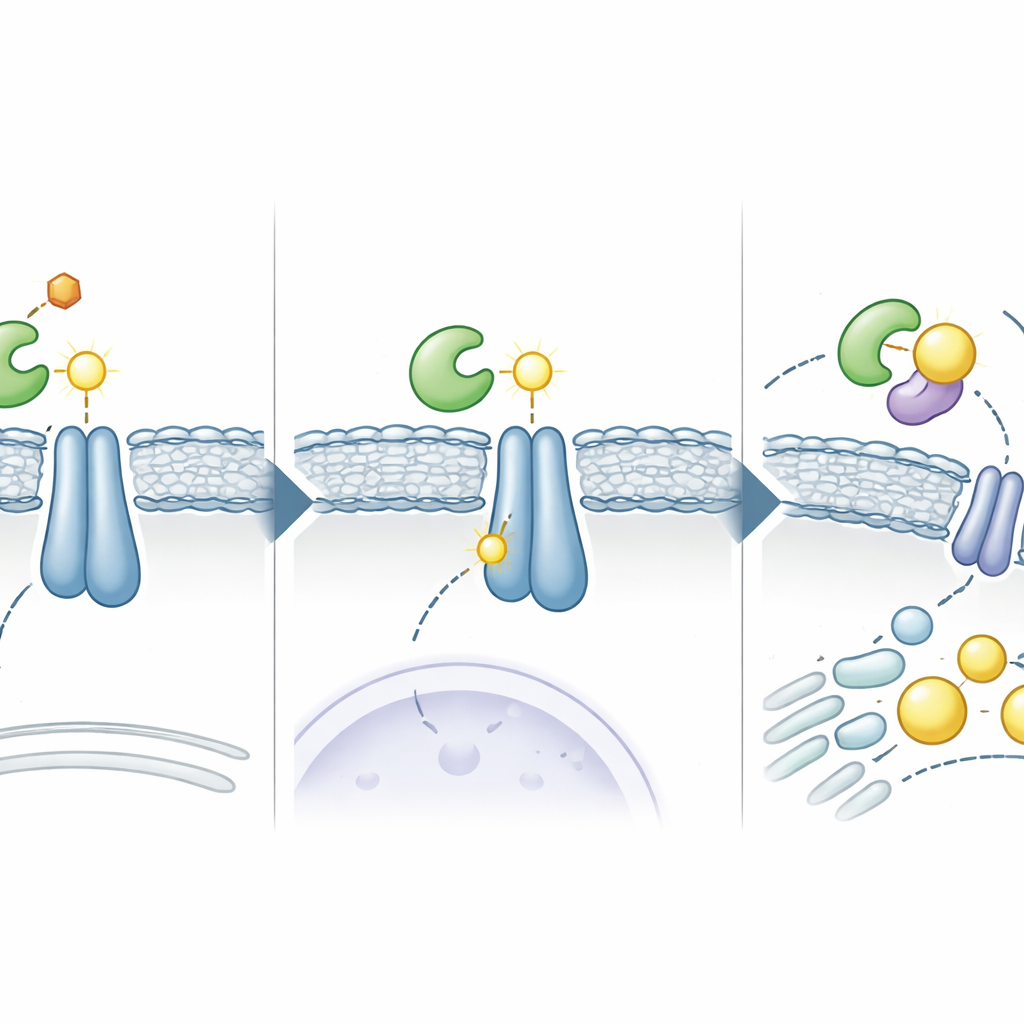
Van celcircuits naar hergebruik van geneesmiddelen
Om te onderzoeken of dit pad tegen de kanker kan worden ingezet, gebruikten de wetenschappers computergestuurde screening van goedgekeurde medicijnen om moleculen te vinden die zich tussen ADSL en INSIG in zouden kunnen klemmen. Ze identificeerden elsulfavirine, een hiv-medicatie, als sterke kandidaat. In laboratoriumexperimenten en computersimulaties verstoorde elsulfavirine de binding tussen ADSL en INSIG, verminderde INSIG-succinatie en blokkeerde SREBP-activatie in leverkankercellen. Daardoor maakten de cellen minder vetten, lagen er minder lipidedruppels opgeslagen en groeiden ze langzamer. In muismodellen van leverkanker krompen tumoren onder elsulfavirine, en het werkte nog beter in combinatie met de standaard leverkankermedicatie lenvatinib, wat wijst op een krachtige combinatie die zowel groeisignalen als metabole behoeften aanpakt.
Wat dit betekent voor patiënten
Om deze bevindingen aan echte ziekte te koppelen, onderzocht het team menselijke levertumormonsters. Tumoren met hoge niveaus van gefosforyleerd ADSL, sterk gesuccineerd INSIG en overvloedig SREBP in de kern waren geassocieerd met slechtere overleving van patiënten. Met andere woorden, dezelfde suikersensorische schakeling die in cellen en muizen is afgebeeld, lijkt actief te zijn in agressieve menselijke levertumoren. Het werk toont aan dat levertumoren extra glucose direct kunnen waarnemen en omzetten in een groeibevorderend vetprogramma via de “moonlighting”-functie van ADSL. Het benadrukt ook elsulfavirine als veelbelovende kandidaat voor hergebruik, en opent een potentiële nieuwe strategie om de vettoevoer waar levertumoren van afhankelijk zijn af te snijden.
Bronvermelding: Duan, Y., Wang, S., Liu, J. et al. INSIG1/2 succination mediated by the moonlighting function of ADSL promotes lipogenesis and liver tumorigenesis. Nat Commun 17, 4002 (2026). https://doi.org/10.1038/s41467-026-70583-0
Trefwoorden: leverkanker, kankermetabolisme, lipogenese, SREBP-pad, hergebruik van geneesmiddelen